oct
21
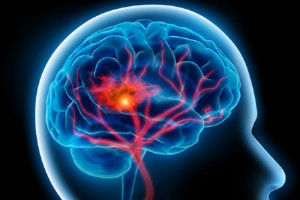
 Es una condición hereditaria que afecta la circulación sanguínea por vasoespasmo.
Es una condición hereditaria que afecta la circulación sanguínea por vasoespasmo.
Los investigadores Investigadores del Instituto de Investigación Universitaria Precision Healthcare (PHURI) de la Universidad Queen Mary de Londres y del Instituto de Salud de Berlín (BIH) en Charité – Universitätsmedizin Berlin han identificado las causas genéticas del fenómeno de Raynaud. Sus hallazgos, publicados en Nature Communications, podrían conducir a los primeros tratamientos eficaces para las personas con enfermedad de Raynaud.
El fenómeno de Raynaud (PR) es una condición hereditaria que afecta la circulación sanguínea. Es una afección vasoespástica, lo que significa que los pequeños vasos sanguíneos cerca de la superficie de la piel tienen espasmos que pueden limitar el flujo sanguíneo. Las personas con Raynaud a menudo experimentan dolor en los dedos de manos y pies, a menudo junto con cambios de color en la piel, debido a la falta de flujo sanguíneo durante los ataques cuando tienen frío o estrés emocional. En casos más graves, puede provocar dolores intensos o úlceras.
Alrededor del 2-5 % de la población se ve afectada por la enfermedad de Raynaud.
A pesar de ser una afección común, está poco investigada y se sabe poco sobre la causa genética de la afección. Hay tratamientos limitados disponibles para RP. Los médicos suelen aconsejar al paciente que utilice estrategias de «autocuidado», como mantenerse abrigado y evitar los desencadenantes de los ataques. En casos graves, se pueden recetar medicamentos, que son «reutilizados», generalmente medicamentos para reducir la presión arterial alta. Estos suelen causar efectos secundarios graves en los pacientes. Se necesita una mejor comprensión de los mecanismos genéticos subyacentes que causan la ER para desarrollar tratamientos seguros y eficaces.
Investigadores dirigidos por la profesora Claudia Langenberg y el profesor Maik Pietzner, que trabajan en PHURI y BIH, llevaron a cabo el estudio genético más amplio del fenómeno de Raynaud. El equipo utilizó registros médicos electrónicos del Biobanco del Reino Unido, una base de datos biomédica a gran escala y un recurso de investigación que contiene información genética y de salud de medio millón de participantes del Reino Unido, para identificar a más de 5.000 personas afectadas por la enfermedad de Raynaud. El equipo también utilizó registros médicos electrónicos del estudio Genes & Health de Queen Mary.
Los resultados
Los investigadores descubrieron variaciones en dos genes que predisponían a los participantes al fenómeno de Raynaud: uno era el receptor alfa-2A-adrenérgico para la adrenalina, ADRA2A, un receptor de estrés clásico que hace que los pequeños vasos sanguíneos se contraigan.
«Esto tiene sentido cuando hace frío o es peligroso, porque el cuerpo tiene que suministrar sangre al interior del cuerpo», explica Maik Pietzner, profesor de modelado de datos de salud en PHURI y líder del grupo en BIH.”
«En los pacientes de Raynaud, este receptor parecía ser particularmente activo, lo que podría explicar los vasoespasmos, especialmente en combinación con el segundo gen que encontramos: este gen es el factor de transcripción IRX1, que puede regular la capacidad de dilatación de los vasos sanguíneos.”
“Si se aumenta su producción, puede activar genes que impiden que los vasos constreñidos se relajen como lo harían normalmente. Esto, junto con el receptor de adrenalina hiperactivo, puede provocar que los vasos sanguíneos no suministren suficiente sangre durante un período de tiempo más largo, lo que provoca que se observen dedos blancos en las manos y los pies”.
Los investigadores replicaron algunos de sus hallazgos utilizando datos de participantes de origen británico, bangladesí y paquistaní del estudio Queen Mary’s Genes & Health. Los hallazgos de los investigadores ayudan a comprender por primera vez por qué los pequeños vasos reaccionan con tanta fuerza en los pacientes, incluso aparentemente sin estímulos externos, como la exposición al frío.
La Dra. Emma Blamont, jefa de investigación de Esclerodermia y Raynaud en el Reino Unido (SRUK), dijo: «La enfermedad de Raynaud es una enfermedad crónica y dolorosa que afecta aproximadamente a una de cada seis personas en el Reino Unido. Sabemos que ciertos desencadenantes como el frío y el estrés pueden provocar ataques, pero se sabe relativamente poco acerca de por qué algunas personas experimentan la enfermedad de Raynaud y otras no». Para los millones de personas que viven con esta afección, las tareas cotidianas simples pueden ser un desafío, por lo que una investigación como esta, que avanza significativamente nuestra comprensión sobre la enfermedad de Raynaud y el papel que la genética puede desempeñar en su causa, es crucial.”
“El siguiente paso es confirmar estos importantes hallazgos en grupos de población más diversos y validar los resultados mediante estudios funcionales. Si tienen éxito, estos hallazgos podrían ayudarnos a desbloquear más vías terapéuticas nuevas para que Raynaud conduzca a tratamientos mejores, más específicos y más amables».
Los hallazgos podrían conducir a recomendaciones para que los pacientes ayuden a controlar la afección o sus síntomas. Por ejemplo, los investigadores demostraron que las personas con una predisposición genética a niveles bajos de azúcar en sangre tienen un mayor riesgo de sufrir el fenómeno de Raynaud, lo que sugiere que los pacientes posiblemente deberían evitar episodios más prolongados de niveles bajos de azúcar en sangre.
Para Claudia Langenberg, directora de PHURI y profesora de Medicina Computacional en BIH, este estudio ejemplifica que la integración de datos de registros médicos genómicos y electrónicos puede ayudar rápidamente a comprender mejor las enfermedades cuya etiología sigue siendo desconocida. “Por supuesto, en última instancia esperamos que nuestros hallazgos apunten a nuevas opciones de tratamiento. Ya existen medicamentos aprobados que inhiben más o menos específicamente la función de ADRA2A, como el antidepresivo mirtazapina, y nuestros resultados sugieren que pueden presentar opciones de tratamiento alternativas para los pacientes que padecen los síntomas de la enfermedad de Raynaud”.
Referencia
Hartmann S, Yasmeen S, Jacobs BM, Denaxas S, Pirmohamed M, Gamazon ER, et al. ADRA2A and IRX1 are putative risk genes for Raynaud’s phenomenon. Nat Commun[Internet]. 2023[citado 20 oct 2023]; 14, 6156 (2023). https://doi.org/10.1038/s41467-023-41876-5
21 octubre 2023 | Fuente: IntraMed| Tomado de Noticias médicas
oct
6
 Una nueva investigación encuentra un posible vínculo entre ciertos genes y la adopción de una dieta vegetariana estricta.
Una nueva investigación encuentra un posible vínculo entre ciertos genes y la adopción de una dieta vegetariana estricta.
Su genética podría ayudarle a cambiar sus hábitos de comer vegetales, sugiere una nueva investigación realizada el miércoles. El estudio encontró una posible asociación entre la adopción de una dieta vegetariana estricta y hasta 34 genes diferentes. Algunos de estos genes afectan la función cerebral y cómo nuestros cuerpos procesan las grasas que obtenemos de nuestra comida, ofreciendo una explicación plausible para una relación de causa y efecto, pero se necesitará más investigación para confirmar y comprender mejor este enlace potencial.
Alrededor del 4 % de los estadounidenses identificar actualmente como vegetarianos, según los datos de la encuesta Gallup. Es un número que no ha cambiado mucho en las últimas dos décadas, aunque otros datos sugiere que la gente en general come menos carne que antes. Al mismo tiempo, muchos vegetarianos comerán carne al menos ocasionalmente. Un estudio de 2015, por ejemplo, encontró que el 48 % de los autoidentificados vegetarianos admitieron haber comido recientemente carne, aves o mariscos.
La dificultad para poder mantener este estilo de vida, a pesar de las fuertes motivaciones morales y de salud que llevan a muchas personas a volverse vegetarianas, hizo Los autores de este nuevo estudio sienten curiosidad. Y dado que otras investigaciones han descubierto que la genética puede influir nuestras elecciones de alimentos En general, querían ver si lo mismo era cierto para el vegetarianismo específicamente.
Para hacer esto, los investigadores recurrieron al Biobanco del Reino Unido, un proyecto de investigación de larga duración que recopila datos genéticos y de salud de cientos de personas de miles de residentes del país. Luego realizaron un estudio de asociación de todo el genoma (GWAS), un tipo de análisis que busca genes o Variantes genéticas vinculadas estadísticamente a enfermedades o rasgos en un grupo grande de personas.
El equipo comparó la genética de más de 5 000 personas que se identificaron como estrictamente vegetarianas (lo que significa que informaron que no comían pescado, carne o aves de corral).) a más de 320 000 controles. En general, identificaron tres genes con una asociación claramente significativa con el vegetarianismo y otros 31 genes que tenían una potencial asociación al el rasgo.
La investigación, publicado El miércoles en PLOS-One es el primero de su tipo, según el autor del estudio Nabeel Yaseen, profesor emérito de patología en la Facultad de Medicina Feinberg de la Universidad Northwestern.
“Nuestro estudio es el primer estudio completamente indexado y revisado por pares que aborda la genética del vegetarianismo”, le dijo a Gizmodo en un correo electrónico.
Los estudios GWAS ayudan a los científicos a identificar las muchas maneras en que la genética puede afectar nuestras vidas, pero tienen advertencias. Al igual que otros tipos de investigación observacional, Por ejemplo, sólo pueden mostrar una correlación entre dos variables, no probar una relación causal directa. Y en este caso, hay Todavía hay mucho que desconocemos sobre los posibles fundamentos genéticos del vegetarianismo.
“Hemos demostrado que los vegetarianos presentan diferencias genéticas significativas con respecto a los no vegetarianos e identificados varios genes candidatos. Sin embargo, no sabemos cuál de los genes que identificamos y qué variantes de esos genes son fundamentales para el vegetarianismo», dijo Yaseen.
Dicho esto, los hallazgos deberían proporcionar a los científicos algunas pistas sobre dónde buscar a continuación. Algunos de los genes que el equipo encontró son conocidos afectar la forma en que metabolizamos los lípidos (grasas) en nuestros alimentos, por ejemplo. Los alimentos cárnicos también tienden a tener lípidos complejos que son diferentes de lo que generalmente está disponible en los productos vegetales. Es posible, teoriza Yaseen, que nuestra fuerte preferencia por la carne esté influenciada por nuestra necesidad inconsciente de estos lípidos, y que los vegetarianos estrictos tienden a poseer variantes genéticas que les permiten producir estos lípidos por sí solos. Pero en este Punto, eso es sólo especulación, añade.
Otras preguntas importantes que el equipo espera que ellos u otros científicos puedan explorar en el futuro incluyen si estos genes y variantes relacionados con los vegetarianos pueden encontrarse en grupos étnicos distintos de los caucásicos blancos (para evitar posibles factores de confusión, el equipo centró su análisis solo en este grupo). En última instancia, lo que aprendamos de esta investigación algún día podría permitirnos personalizar mejor las recomendaciones dietéticas o incluso producir mejores sustitutos de la carne.
Este contenido ha sido traducido automáticamente del material original. Debido a los matices de la traducción automática, pueden existir ligeras diferencias.
Referencia
Yaseen N, Barnes CL, Sun L, Takeda A, Rice JP. Genetics of vegetarianism: A genome-wide association study. PLOS One[Internet].2023[citado 5 oct 2023]; 18(10): e0291305. https://doi.org/10.1371/journal.pone.0291305
6 octubre 2023 |Fuente: Gizmodo| Tomado de Ciencia
sep
23
 La identificación de nuevos genes relacionados con la resistencia quimioterapia en pacientes con carcinoma de células escamosas de cabeza y cuello (CECyC) abre nuevas vías para la medicina de precisión en este tipo de cáncer.
La identificación de nuevos genes relacionados con la resistencia quimioterapia en pacientes con carcinoma de células escamosas de cabeza y cuello (CECyC) abre nuevas vías para la medicina de precisión en este tipo de cáncer.
El cáncer de cabeza y cuello (CECyC) engloba un grupo de cánceres que se forman en los tejidos del tracto digestivo superior o en los senos y cavidad nasal. La mayoría derivan de las células escamosas que forman estos tejidos, de donde reciben su nombre.
Cuando el CECyC no está muy avanzado existen opciones de tratamiento efectivas con una elevada tasa de supervivencia a cinco años. En el caso de enfermedad avanzada, sin embargo, existen menos oportunidades de tratamiento. Una de las causas de esta situación es que todavía se desconoce en gran medida la variabilidad genética del CECyC. Como resultado, todos los pacientes reciben un tratamiento similar sin tener en cuenta el perfil genético de su cáncer. No existen opciones de tratamientos de precisión que permitan definir el mejor tratamiento para el tumor de cada paciente y, en muchos casos, las combinaciones de quimioterapia estándar derivan en toxicidad o resistencia al tratamiento.
Con el objetivo de mejorar esta situación, investigadores de la Universidad Queen Mary de Londres han utilizado diferentes aproximaciones bioinformáticas y genéticas dirigidas a identificar genes que puedan estar relacionados con la enfermedad y permitan clasificar mejor a los pacientes. Los resultados apuntan a dos nuevos genes de interés y dos moléculas con potencial terapéutico.
“Estos resultados son un paso prometedor para que en el futuro los pacientes de cáncer reciban un tratamiento personalizado basado en sus genes y su tipo de tumor que les proporcione una mejor tasa de supervivencia y mejores resultados terapéuticos”, ha señalado Muy-Teck Teh, investigador en la Universidad Queen Mary de Londres y uno de los responsables del estudio.
Identificando los genes que confieren resistencia a la quimioterapia en carcinoma escamoso de cabeza y cuello
En primer lugar, los investigadores utilizaron minería de datos para identificar genes que se expresan de forma diferente en muestras sanas y tumorales de pacientes con CECyC. De esta forma identificaron 40 genes candidatos.
A continuación, el equipo analizó la expresión de los 40 genes seleccionados en ocho líneas de células orales, así como en 10 líneas de CECyC. De esta forma, acotaron el número de candidatos a 28 genes con expresión diferencial entre células normales y células tumorales. Los candidatos, además, participan en procesos relacionados con el cáncer, como la modulación del sistema inmunitario o la proliferación.
Por último, el equipo evaluó en diferentes experimentos qué genes de los que mostraban diferente actividad podían influir en la resistencia a la quimioterapia en el CECyC. En este paso identificaron 10 genes relacionados, y seleccionaron los cuatro más significativos (TOP2A, DNMT1, INHBA y NEK2) para realizar estudios más detallados.
Finalmente, a partir de ensayos más precisos con los cuatro genes más prometedores, los investigadores concluyen que la expresión de NEK2 confiere quimioresistencia al cisplatino, al 5-fluorouracilo, al paclitaxel, y al docetaxel. Por otra parte, los genes INHBA y TOP2A confieren la resistencia a la mayoría de líneas celulares resistentes a fármacos. Y en cuanto a DNMT1, los investigadores señalan que ejerce efectos heterogéneos en cuanto a la quimiorresistencia.
Nuevas perspectivas para hacer frente a la resistencia a la quimioterapia
Una vez identificados los genes cuya activación está relacionada con la resistencia a los multitratamientos que se utilizan para hacer frente al CECyC, el siguiente paso de los investigadores fue identificar fármacos o sustancias que pudieran regular su actividad.
El equipo utilizó una librería de fármacos para rastrear posibles interacciones fármaco-gen y encontró dos compuestos de origen natural muy interesantes. Tanto la Sirodesmina A, de origen fúngico, como el fármaco anticáncer Carfilzomib, bloquean la expresión de NEK2 e INHBA y devuelven la sensibilidad al cisplatino a las células resistentes.
Los investigadores plantean que tanto la Sirodesmina A como el Carfilzomib podrían reposicionarse para contrarrestar la resistencia al cisplatino en tumores con expresión elevada de NEK2 y/o INHBA.
Resultados prometedores para la medicina de precisión
El trabajo identifica dos genes relacionados con la resistencia al tratamiento en el CECyC, cuya expresión podría servir para clasificar mejor a los pacientes. Además, también presenta dos compuestos que podrían ayudar a hacer frente a la aparición de resistencias.
Estudios futuros deberán investigar en mayor detalle las interacciones entre la Sirodesmina A y el Carfilzomib y los genes NEK2 y INHBA, así como su potencial en un entorno clínico.
“Por desgracia, hay muchas personas que no responden a la quimioterapia ni a la radioterapia”, indica Muy-Teck Teh, investigador en la Universidad Queen Mary de Londres y director del estudio. “Pero nuestro estudio ha demostrado que, al menos en los cánceres de cabeza y cuello, son estos dos genes concretos los que podrían estar detrás de esta situación, y que se pueden atacar para luchar contra la quimiorresistencia”.
Referencia científica
Khera N, Soodhalaagunta Rajkumar A, Abdulkader M Alkurdi K, Liu Z, Ma H, et al. Identification of multidrug chemoresistant genes in head and neck squamous cell carcinoma cells. Mol Cancer. 2023; 146. doi: http://dx.doi.org/10.1186/s12943-023-01846-3
19/09/2023
Fuente: (genotipia) Tomado de Noticias Genética Médica News
Copyright 2023 © Genotipia
sep
11
 Un reciente estudio internacional ha identificado nuevos genes y variantes genéticas que aumentan el riesgo a desarrollar cáncer de mama.
Un reciente estudio internacional ha identificado nuevos genes y variantes genéticas que aumentan el riesgo a desarrollar cáncer de mama.
Pese a los relevantes avances en diagnóstico y tratamiento, el cáncer de mama sigue siendo la principal causa de muerte en mujeres. Según datos de la Organización Mundial de la Salud, solo en 2020, fallecieron alrededor de 685 000 mujeres por esta enfermedad.
Los factores genéticos juegan un papel importante en el cáncer de mama. Estudios realizados en los últimos años han identificado tanto variantes genéticas concretas, poco frecuentes, que confieren un riesgo elevado a la enfermedad, como variantes más comunes que tienen un menor peso. Sin embargo, todavía no está disponible el mapa completo de susceptibilidad genética a la enfermedad, información con la que podría estimarse mejor la probabilidad de cada persona a tener la enfermedad.
A partir del análisis del exoma completo de 26 368 mujeres con cáncer de mama y 217 673 mujeres control, un reciente estudio, publicado en Nature Genetics, amplia el mapa genético de la enfermedad al aportar evidencias de nuevos genes de susceptibilidad.
“Que sepamos, éste es el mayor estudio de este tipo. Ha sido posible gracias al uso de datos de múltiples colaboradores de muchos países, así como de datos de acceso público del Biobanco del Reino Unido”, ha señalado Douglas Easton, director del Centro de Epidemiología Genética del Cáncer de la Universidad de Cambridge, y codirector del estudio.
Análisis de exomas para identificar contribuyentes genéticos al cáncer de mama
Para identificar nuevas variantes poco frecuentes, los investigadores analizaron los datos genómicos de tres grandes proyectos internacionales y compararon los exomas (regiones codificantes del genoma) de las pacientes con cáncer de mama respecto al de mujeres no diagnosticadas. Especialmente analizaron la variación genética que lleva a proteínas truncadas y la variación genética que da lugar a cambios de aminoácidos en las proteínas que derivaran en un efecto deletéreo.
Además de detectar variantes genéticas relacionadas con el cáncer de mama en genes de susceptibilidad ya conocidos como ATM, BRCA1, BRCA2, CHEK2 y PALB2, los investigadores encontraron evidencias de nuevos genes relacionados con la enfermedad: LZTR1, ATR, BARD1, CDKN2A y MAP3K1.
Aplicaciones en predicción de riesgo y desarrollo de tratamientos
La información obtenida en el estudio, podría mejorar las predicciones de riesgo del cáncer de mama. En la actualidad, la mayor parte de pruebas genéticas para el cáncer de mama en el ámbito clínico están dirigidas a detectar variantes en los genes más conocidos, pero disponer de mayor información a nivel genético podría aportar más precisión.
“Aunque la mayoría de las variantes identificadas en estos nuevos genes son poco frecuentes, los riesgos pueden ser importantes para las mujeres portadoras”, ha destacado Jacques Simard de la Universidad Laval, codirector del trabajo. “Por ejemplo, las alteraciones en uno de los nuevos genes, MAP3K1, parecen dar lugar a un riesgo especialmente elevado de cáncer de mama.”
“Necesitamos datos adicionales para determinar con mayor precisión los riesgos de cáncer asociados a las variantes de estos genes, estudiar las características de los tumores y comprender cómo se combinan estos efectos genéticos con otros factores del estilo de vida que afectan a los riesgos de cáncer de mama”, ha señalado también Douglas Easton.
En paralelo a su utilidad predictiva, la identificación de nuevos genes con potencial implicación en el cáncer de mama, amplía el conocimiento de los mecanismos que participan en la enfermedad. Esta información podría contribuir a detectar nuevas dianas de tratamiento.
Por último, los resultados del trabajo también apuntan a que una parte importante de los genes relacionados con la enfermedad deben encontrarse en regiones no codificantes. Estudios futuros deberán evaluar esta cuestión.
Referencia
Wilcox N, Dumont M, González-Neira A, Carvalho S, Beauparlant CH , Crotti M, et al. Exome sequencing identifies breast cancer susceptibility genes and defines the contribution of coding variants to breast cancer risk. Nat Genet (2023). https://doi.org/10.1038/s41588-023-01466-z
https://www.nature.com/articles/s41588-023-01466-z
07/09/2023 (Genotipia.com) Genética Médica Copyright 2023 © Genotipia
ago
11
Un estudio internacional con participación de investigadores de Barcelona ha llevado a cabo un análisis del genoma completo de más de 1,5 millones de personas, de las cuales más de 110.000 habían experimentado un ictus.
Investigadores del Instituto de Investigación del Hospital de la Santa Creu i Sant Pau – IIB Sant Pau (Barcelona) han participado en un estudio internacional en el que ha encontrado 89 genes implicados en el riesgo de desarrollar un ictus, de los que 61 no se habían descrito previamente.
Los resultados del trabajo se publican en Nature, donde los autores explican que han analizado datos por medio de estudios de asociación del genoma completo de más de 1,5 millones de pacientes, de los que más de 100.000 habían sufrido un ictus.
El ictus es una de las principales causas de muerte, pero hasta ahora los estudios de factores de riesgo genéticos de la enfermedad habían analizado principalmente muestras de personas de origen europeo y, según los autores, el trabajo más extenso tenía datos de 67.000 pacientes y 500.000 controles sanos.
El equipo investigador destaca que han elaborado el estudio «más amplio y completo» hasta la fecha: han realizado el análisis de asociación del genoma completo en 1.503.898 participantes, de los que 110.182 han sufrido un ictus de cinco ascendencias diferentes.
Han realizado este trabajo con la participación del International Stroke Genetics Consortium, del que forma parte el consorcio español GeneStroke Consortium y la cohorte española GCAT Genomes for Life.
Los investigadores también han demostrado que la suma de los factores de riesgo genético predicen el riesgo futuro de ictus, independientemente de los factores de riesgo clínicos, después de analizar los datos de 52.600 personas con enfermedad cardiometabólica.
Al conocer mejor los mecanismos implicados en el desarrollo del ictus, se pueden buscar nuevos tratamientos dirigidos, evaluar la eficacia de fármacos ya aprobados para otras enfermedades que puedan servir para tratar a este tipo de paciente y hacer prevención en aquellas personas con alto riesgo por sus características genéticas.
10 de Agosto del 2023 Jano.es
may
19
El aprendizaje automático es una rama de la IA por la que los sistemas informáticos mejoran y aprenden continuamente en función de los datos y la experiencia, algo que los biólogos están utilizando para investigar las funciones centrales de los genes.
En este sentido, investigadores de la Universidad de California en San Diego (EEUU) que investigan las secuencias de ADN que activan los genes usaron inteligencia artificial para identificar una enigmática pieza del rompecabezas relacionada con la activación de genes. Este es un proceso fundamental involucrado en el crecimiento, el desarrollo y la enfermedad. Mediante aprendizaje automático, el profesor de la Facultad de Ciencias Biológicas James T. Kadonaga y su equipo descubrieron la región promotora del núcleo (DPR) aguas abajo , un código de activación de ADN de «puerta de enlace» que está involucrado en la operación de hasta un tercio de nuestros genes.
A partir de este descubrimiento, el prof.Kadonaga y los investigadores Long Vongoc y Torrey E. Rhyne han utilizado, recientemente, el aprendizaje automático para identificar secuencias de ADN «extremas sintéticas» con funciones diseñadas específicamente en la activación de genes, tal como publican en la revista ´Genes & Development´.
Los investigadores probaron millones de diferentes secuencias de ADN a través del aprendizaje automático (IA) comparando el elemento de activación del gen DPR en humanos versus moscas de la fruta ( Drosophila ). Al usar IA, pudieron encontrar secuencias DPR raras y personalizadas que están activas en humanos pero no en moscas de la fruta y viceversa. De manera más general, este enfoque ahora podría usarse para identificar secuencias de ADN sintético con actividades que podrían ser útiles en biotecnología y medicina.
«Hemos demostrado el uso de IA para el diseño de elementos de ADN personalizados en la activación de genes. Hay innumerables aplicaciones prácticas de este enfoque basado en IA. Las secuencias de ADN extremas sintéticas pueden ser muy raras, tal vez una en un millón; si existen, podrían encontrarse mediante el uso de IA. Este método debería tener aplicaciones prácticas en biotecnología e investigación biomédica», concluyó el prof. Kadonaga.
Mayo 19/2023 (IMMédico) – Tomado de Enfermedades Raras, Oncología Copyright 2023 Copyright: Publimas Digital.