sep
19
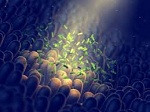 Una bacteria intestinal que contiene ácido sulfúrico puede proteger al organismo de la salmonella, entre otros patógenos, revela un estudio publicado este lunes en la revista científica Nature Communications.
Una bacteria intestinal que contiene ácido sulfúrico puede proteger al organismo de la salmonella, entre otros patógenos, revela un estudio publicado este lunes en la revista científica Nature Communications.
La investigación, liderada por el microbiólogo austríaco Alexander Loy del centro de Microbiología de la Universidad de Viena, demuestra que esta bacteria, a la que llamó ‘devorador de taurina del ratón’ por su alta absorción de taurina (presente en muchas bebidas energéticas), tiene pequeñas cantidades de sulfuro de hidrógeno que son esenciales en el intestino para muchos procesos fisiológicos.
La utilidad principal de esta bacteria es la protección del intestino contra enfermedades como la salmonella, causada principalmente por la ingesta de huevos o carne en mal estado, pero también contra gérmenes hospitalarios, cada vez más extendidos.
‘En los gérmenes hospitalarios, el sulfuro de hidrógeno bloquea el sitio de unión para el oxígeno en el centro activo de las enzimas de la cadena respiratoria’, explicó Loy a la agencia austríaca APA.
No obstante, el ácido sulfúrico, un gas que provoca flatulencias de muy mal olor y es el principal culpable del mal aliento, es peligroso en grandes cantidades, pues llevan a los humanos a perder la capacidad de olerlo y se vuelve venenoso.
Se encuentra, además de en nuestro sistema digestivo en muy pequeñas cantidades, entre los gases de volcanes, en manantiales de azufre, pantanos, aguas estancadas y en el petróleo crudo.
Referencia
Ye H, Borusak S, Eberl CE, Krasenbrink J, Weiss AS, Can chen S, et al. Ecophysiology and interactions of a taurine-respiring bacterium in the mouse gut. Nat Communications. 2023; 5533. https://doi.org/10.1038/s41467-023-41008-z
https://www.nature.com/articles/s41467-023-41008-z
Fuente: (Prensa Latina) – Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
sep
5
Investigadores dirigidos por Hiroshi Ohno en el Centro RIKEN de Ciencias Médicas Integrativas (IMS) en Japón han descubierto un tipo de bacteria intestinal que podría ayudar a mejorar la resistencia a la insulina y, por tanto, proteger contra el desarrollo de la obesidad y la diabetes tipo 2. El estudio, publicado el 30 de agosto en la revista científica Nature, implicó un análisis genético y metabólico de microbiomas fecales humanos y luego corroboró experimentos en ratones obesos.
 La resistencia a la insulina es la fisiopatología principal que subyace al síndrome metabólico y a la diabetes tipo 2. Estudios metagenómicos anteriores han descrito las características de la microbiota intestinal y su papel en la metabolización de los principales nutrientes en la resistencia a la insulina. En particular, se ha propuesto que el metabolismo de los carbohidratos de los comensales contribuye con hasta el 10 % de la extracción total de energía del huésped desempeñando así un papel en la patogénesis de la obesidad y la prediabetes. Sin embargo, el mecanismo subyacente sigue sin estar claro. Aquí investigamos esta relación utilizando una estrategia multiómica integral en humanos.
La resistencia a la insulina es la fisiopatología principal que subyace al síndrome metabólico y a la diabetes tipo 2. Estudios metagenómicos anteriores han descrito las características de la microbiota intestinal y su papel en la metabolización de los principales nutrientes en la resistencia a la insulina. En particular, se ha propuesto que el metabolismo de los carbohidratos de los comensales contribuye con hasta el 10 % de la extracción total de energía del huésped desempeñando así un papel en la patogénesis de la obesidad y la prediabetes. Sin embargo, el mecanismo subyacente sigue sin estar claro. Aquí investigamos esta relación utilizando una estrategia multiómica integral en humanos.
Combinamos la metabolómica fecal con la metagenómica, la metabolómica del huésped y los datos de transcriptómica para perfilar la participación del microbioma en la resistencia a la insulina. Estos datos revelan que los carbohidratos fecales, particularmente los monosacáridos accesibles al huésped, aumentan en individuos con resistencia a la insulina y están asociados con el metabolismo microbiano de los carbohidratos y las citocinas inflamatorias del huésped. Identificamos bacterias intestinales asociadas con la resistencia a la insulina y la sensibilidad a la insulina que muestran un patrón distinto de metabolismo de los carbohidratos y demostramos que las bacterias asociadas con la sensibilidad a la insulina mejoran los fenotipos de resistencia a la insulina del huésped en un modelo de ratón. Nuestro estudio, que proporciona una visión integral de las relaciones huésped-microorganismo en la resistencia a la insulina, revela el impacto del metabolismo de los carbohidratos en la microbiota, lo que sugiere un posible objetivo terapéutico para mejorar la resistencia a la insulina.
Comentarios
La insulina es una hormona liberada por el páncreas en respuesta al azúcar en sangre. Normalmente, ayuda a que la glucosa llegue a los músculos y al hígado para que puedan utilizar la energía. Cuando alguien desarrolla resistencia a la insulina, significa que la insulina no puede hacer su trabajo y, como resultado, permanece más azúcar en la sangre y el páncreas continúa produciendo más insulina. La resistencia a la insulina puede provocar obesidad, prediabetes y diabetes tipo 2 en toda regla.
Nuestros intestinos contienen billones de bacterias, muchas de las cuales descomponen los carbohidratos que comemos cuando, de otro modo, no serían digeridos. Si bien muchos han propuesto que este fenómeno está relacionado con la obesidad y la prediabetes, los hechos aún no están claros porque hay muchas bacterias diferentes y faltan datos metabólicos. Ohno y su equipo en RIKEN IMS abordaron esta carencia con su estudio integral y, en el proceso, descubrieron un tipo de bacteria que podría ayudar a reducir la resistencia a la insulina.
En primer lugar, examinaron tantos metabolitos como pudieron detectar en las heces proporcionadas por más de 300 adultos en sus controles médicos habituales. Compararon este metaboloma con los niveles de resistencia a la insulina obtenidos de las mismas personas. «Descubrimos que una mayor resistencia a la insulina se asociaba con un exceso de carbohidratos en la materia fecal», dice Ohno, «especialmente monosacáridos como glucosa, fructosa, galactosa y manosa».
A continuación, caracterizaron la microbiota intestinal de los participantes del estudio y su relación con la resistencia a la insulina y los carbohidratos fecales. Los intestinos de las personas con mayor resistencia a la insulina contenían más bacterias del orden taxonómico Lachnospiraceae que de otros órdenes. Además, los microbiomas que incluían Lachnospiraceae se asociaron con un exceso de carbohidratos fecales. Así, una microbiota intestinal dominada por Lachnospiraceae se relacionó tanto con la resistencia a la insulina como con las heces con exceso de monosacáridos. Al mismo tiempo, la resistencia a la insulina y los niveles de monosacáridos fueron más bajos en los participantes cuyos intestinos contenían más bacterias de tipo Bacteroidales que otros tipos.
Luego, el equipo se propuso observar el efecto directo de las bacterias sobre el metabolismo en cultivos y luego en ratones. En cultivo, las bacterias Bacteroidales consumieron los mismos tipos de monosacáridos que se encontraron en las heces de personas con alta resistencia a la insulina, siendo la especie Alistipes indistinctus la que consumió la mayor variedad. En ratones obesos, el equipo observó cómo el tratamiento con diferentes bacterias afectaba los niveles de azúcar en sangre. Descubrieron que A. indistinctus reducía el azúcar en sangre y reducía la resistencia a la insulina y la cantidad de carbohidratos disponibles para los ratones.
Estos resultados fueron compatibles con los hallazgos de pacientes humanos y tienen implicaciones para el diagnóstico y el tratamiento. Como explica Ohno, “debido a su asociación con la resistencia a la insulina, la presencia de la bacteria intestinal Lachnospiraceae podría ser un buen biomarcador de la prediabetes. Asimismo, el tratamiento con probióticos que contienen A. indistinctus podría mejorar la intolerancia a la glucosa en personas con prediabetes”.
Aunque la mayoría de los probióticos de venta libre actualmente no contienen las bacterias identificadas en este estudio, Ohno recomienda precaución en caso de que estén disponibles. «Estos hallazgos deben verificarse en ensayos clínicos en humanos antes de que podamos recomendar cualquier probiótico como tratamiento para la resistencia a la insulina».
Referencia. Takeuchi T, Kubota T, Nakanishi Y, Tsugawa Y, Suda W, Jun Kwon AT, et al. Gut microbial carbohydrate metabolism contributes to insulin resistance. Nature (2023). https://doi.org/10.1038/s41586-023-06466-x https://www.nature.com/articles/s41586-023-06466-x
03/09/2023(IntraMed) Tomado-Noticias médicas Copyright 1997-2023
ago
28
 Este trabajo, para el que se requiere una importante potencia informática, podría ayudar contra otras enfermedades causadas por virus similares, como el zika y la fiebre amarilla.
Este trabajo, para el que se requiere una importante potencia informática, podría ayudar contra otras enfermedades causadas por virus similares, como el zika y la fiebre amarilla.
Los flavivirus (dengue, zika, virus del Nilo Occidental, fiebre amarilla…) infectan las células humanas por un proceso llamado endocitosis (fusionan su membrana con la pared celular en función de la acidez que detectan). Conocer este mecanismo es clave para obtener fármacos antivirales que eviten la infección y, dado que la interacción entre los virus y las células sanas se produce a través de proteínas muy complejas, para entender el proceso es necesario simular por ordenador cómo se produce la interacción química entre sus moléculas.
Con este enfoque, un estudio de la Universidad Miguel Hernández (UMH) de Elche, publicado en la revista Biochimica Biophysica Acta Biomembranes, ha revelado la secuencia específica de la proteína E del virus del dengue donde se produce la interacción con las células humanas y, por tanto, hacia dónde deberían dirigirse los fármacos para prevenir la infección, según destaca José Villalaín, líder del estudio y profesor de Bioquímica y Biología Molecular de la UMH.
¿Cuál es el punto de partida del proyecto? El virus del dengue ya es endémico en nuestro país, al detectarse casos autóctonos. Según Villalaín, investigador del Instituto de Desarrollo, Investigación e Innovación en Biotecnologías Sanitaria de la Universidad Miguel Hernández (IdiBE), es de esperar que se produzcan cada vez más casos debido a las altas temperaturas y a las inundaciones periódicas que favorecen la extensión y propagación de los mosquitos Aedes aegypti o Aedes albopictus, cuya picadura puede transmitir la enfermedad.
Anteriores publicaciones de Villalaín demostraron que la proteína E del virus del dengue, responsable de la entrada del virus en la célula huésped, tiene tres puntos de unión a las membranas biológicas. A partir de ese conocimiento, ya que la fusión de las membranas es el primer y más importante paso en la infección del virus del dengue, era necesario «afinar» aún más dónde podía producirse el proceso.
Primera vacuna que protege contra el dengue con independencia de infecciones previas
‘Luz verde’ de la EMA a la vacuna tetravalente contra el dengue de Takeda
Cataluña confirma un nuevo caso de dengue no importado en España
Este estudio se ha realizado mediante dinámica molecular, un proceso de «simulación virtual» de la interacción entre proteínas que requiere tanta potencia informática que resulta necesario un conjunto de ordenadores para llevar a cabo el experimento. En estas simulaciones, se puede ver cómo se comporta cada átomo que compone las proteínas del virus y, por tanto, estudiar en detalle tanto la interacción entre moléculas como lo que ocurre dentro de las mismas.
Para este tipo de investigaciones, la UMH cuenta con un clúster de computación científica, un grupo de ordenadores unidos mediante una red de alta velocidad, gestionada por el Servicio de Innovación y Planificación Tecnológica. Según Villalaín, «se analizaron diversas conformaciones proteicas del sensor de pH y su interacción con diferentes lípidos de la membrana. Debido a la complejidad de los sistemas la toma de datos duró unos seis meses».
Gracias a esa labor, se ha demostrado que existe una secuencia específica de la proteína E del virus del dengue que es responsable tanto de la interacción proteína-proteína como proteína-membrana, fundamental en el proceso de activación proteica y en la consecuente fusión de las membranas viral y celular. Ese segmento, además de funcionar como sensor de pH, es decir, ser capaz de detectar la entrada del virus dentro del endosoma tardía, se une a la biomembrana de la célula con una alta afinidad y gran especificidad, lo que lo convierte en una diana terapéutica fundamental con la cual atacar al virus. Respecto al resultado, Villalaín destaca que «no se sabía si solo funcionaba como sensor de pH y/o además interaccionaba con la membrana de un modo específico, como así se ha demostrado».
Aplicación a otros virus similares
La importancia adicional del trabajo radica en que este segmento, encontrado también en otros tipos similares de virus, podría ayudar a encontrar moléculas antivirales que también serían efectivas contra las infecciones de virus similares al dengue, como el zika o la fiebre amarilla. Ese hallazgo, en definitiva, «nos descubre una nueva diana para poder inhibir la entrada del virus del dengue y, posiblemente, la de otros flavivirus». En todas estas patologías, recuerda, «no existen vacunas, son ineficientes o incluso producen efectos secundarios a determinados tipos de paciente». Todo ello podría ayudar a «conseguir un antiviral de efecto genérico contra los flavivirus», además de «estar preparados para nuevos tipos de virus emergentes de la misma familia que, posiblemente, a medio y largo plazo puedan ser generadores de nuevas enfermedades».
Fuente: Diario Médico
ago
23
 Hace mucho tiempo que se sabe que la lactancia materna ayuda a mantener a los recién nacidos sanos y protegidos frente a diversas enfermedades. Pero ciertos azúcares presentes en la leche materna también podrían ayudar a prevenir infecciones antes del nacimiento del bebé. Los investigadores que publican informes en ACS Central Science han descubierto que estos azúcares pueden detener una infección prenatal habitual que afecta a los tejidos humanos y a ratones preñados. Esto podría ayudar a evitar partos prematuros u otras complicaciones sin necesidad de suministrar antibióticos en el futuro.
Hace mucho tiempo que se sabe que la lactancia materna ayuda a mantener a los recién nacidos sanos y protegidos frente a diversas enfermedades. Pero ciertos azúcares presentes en la leche materna también podrían ayudar a prevenir infecciones antes del nacimiento del bebé. Los investigadores que publican informes en ACS Central Science han descubierto que estos azúcares pueden detener una infección prenatal habitual que afecta a los tejidos humanos y a ratones preñados. Esto podría ayudar a evitar partos prematuros u otras complicaciones sin necesidad de suministrar antibióticos en el futuro.
Algunas bacterias que pueden afectar los embarazos de forma más frecuente son los estreptococos del grupo B (EGB). Las infecciones por EGB no tratadas pueden provocar efectos adversos, como neumonía neonatal o parto prematuro. Los tratamientos existentes se basan principalmente en antibióticos, que pueden dar lugar a cepas resistentes. Sin embargo, muchos de los compuestos ya presentes en la leche materna humana, como los oligosacáridos de la leche materna (HMO, por sus siglas en inglés), tienen efectos antibacterianos.
Steven Townsend, Jennifer Gaddy y sus colegas previamente exploraron los efectos antibacterianos de los HMO y descubrieron que podían inhibir el crecimiento de los EGB in vitro y en determinadas células reproductoras. Sin embargo, los investigadores debían demostrar cómo funcionan los azúcares en diferentes tejidos e in vivo antes de poder utilizar estos compuestos para potenciar los antibióticos existentes, o considerarlos como una nueva opción de tratamiento. Los investigadores pasaron entonces a estudiar la actividad de los HMO en las infecciones por EGB en ratones preñados y en tejidos humanos.
En primer lugar, analizaron los efectos protectores de los HMO en tejidos humanos infectados por EGB, utilizando tanto tejidos fetales vivos como un modelo organoide de la vagina. Al añadir un compuesto de HMO diseñado para imitar la composición de los azúcares de la leche materna, las bacterias no pudieron adherirse ni formar colonias.
A continuación, probaron el compuesto de HMO en ratones preñados infectados con EGB. Los ratones tratados presentaron un nivel de inflamación relativamente típico, cantidades reducidas de bacterias en distintos tejidos reproductivos y no hubo casos de partos prematuros, rotura de membranas ni muertes maternas. En su conjunto, estos resultados demuestran que los HMO pueden tener efectos antimicrobianos sin la administración de antibióticos adicionales. Los investigadores afirman que este trabajo podría permitir el uso de estos azúcares como opción viable de tratamiento para las infecciones por EGB y para prevenir resultados adversos en el embarazo.
Fuente: EurekaAlert
Referencia: Rebecca E. Moore, Sabrina K. Spicer, Jacky Lu, Schuyler A. Chambers, Kristen N. Noble, Jonathan Lochner, Rebecca C. Christofferson, Karla A. Vasco, Shannon D. Manning, Steven D. Townsend, and Jennifer A. Gaddy. The Utility of Human Milk Oligosaccharides against Group B Streptococcus Infections of Reproductive Tissues and Cognate Adverse Pregnancy Outcomes. ACS Central Science Article ASAP. Aug 2023. DOI: 10.1021/acscentsci.3c00101
ago
23
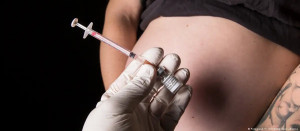 La única dosis podrá ser administrada entre las semanas 32 y 36 de gestación y garantiza una protección de seis meses. Las infecciones por el virus son la principal causa de hospitalizaciones de lactantes en EE. UU.
La única dosis podrá ser administrada entre las semanas 32 y 36 de gestación y garantiza una protección de seis meses. Las infecciones por el virus son la principal causa de hospitalizaciones de lactantes en EE. UU.
Según la FDA, se trata de una inyección única que se administra en un músculo entre las semanas 32 y 36 de gestación, garantizando una protección contra el llamado virus respiratorio sincitial (VRS, por sus siglas en inglés) durante los primeros seis meses de vida del bebé.
La misma vacuna está autorizada desde mayo en Estados Unidos para personas mayores de 60 años. Asimismo, un preparado similar llamado Arexvy fue aprobado en julio por la Agencia Europea del Medicamento (EMA), tanto para bebés como para personas de la tercera edad, pero la Comisión Europea debe decidir ahora si aprueba su comercialización en la Unión Europea.
Principal causa de hospitalización de lactantes
Este virus «es una causa común de enfermedad en los niños, y los lactantes se encuentran entre los que corren más riesgo de sufrir una enfermedad grave, lo que puede llevar a la hospitalización», recordó Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA.
El ensayo clínico, en el que participaron unas 7.000 embarazadas, demostró que la vacuna, denominada Abrysvo, reducía la variante grave de la enfermedad en un 82% en los bebés de 0 a 3 meses y en un 69% de 0 a 6 meses. El VRS suele causar síntomas leves como los de un resfriado en lactantes y niños pequeños, pero también neumonía y bronquiolitis.
Se calcula que entre 58.000 y 80.000 niños de menos de cinco años son hospitalizados debido a una infección por VRS, según los Centros para el Control y la Prevención de Enfermedades (CDC), lo que la convierte en la principal causa de hospitalización entre los lactantes.
Efectos secundarios y posteriores estudios
Entre los efectos secundarios más frecuentes en las embarazadas vacunadas con Abrysvo figuran molestias en el lugar de la inyección, dolor de cabeza o muscular y náuseas.
Un peligroso trastorno de la tensión arterial, conocido como preeclampsia, se produjo en el 1,8% de los casos frente al 1,4 % de las que recibieron un placebo. La FDA observó además un desequilibrio en los nacimientos prematuros entre el grupo que recibió la vacuna y el del placebo (5,7 % frente a 4,7 %).
Como consecuencia, la agencia ha pedido a Pfizer que siga estudiando el riesgo de parto prematuro y preeclampsia. Tras la aprobación, el producto debe recibir el visto bueno de los CDC, de modo que no está claro si estará disponible a tiempo para la temporada de VRS de este otoño e invierno.
Referencia: FDA Approves First Vaccine for Pregnant Individuals to Prevent RSV in Infants
Fuente: DW.COM
ago
21
 Alrededor de 55 millones de personas en todo el mundo tienen la enfermedad de Alzheimer y otras demencias.
Alrededor de 55 millones de personas en todo el mundo tienen la enfermedad de Alzheimer y otras demencias.
Dado que los científicos esperan que ese número siga creciendo cada año, se ha prestado mucha atención al desarrollo de nuevos tratamientos para la afección. Read more