ago
23
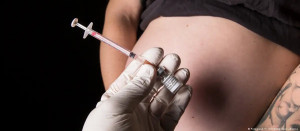 La única dosis podrá ser administrada entre las semanas 32 y 36 de gestación y garantiza una protección de seis meses. Las infecciones por el virus son la principal causa de hospitalizaciones de lactantes en EE. UU.
La única dosis podrá ser administrada entre las semanas 32 y 36 de gestación y garantiza una protección de seis meses. Las infecciones por el virus son la principal causa de hospitalizaciones de lactantes en EE. UU.
Según la FDA, se trata de una inyección única que se administra en un músculo entre las semanas 32 y 36 de gestación, garantizando una protección contra el llamado virus respiratorio sincitial (VRS, por sus siglas en inglés) durante los primeros seis meses de vida del bebé.
La misma vacuna está autorizada desde mayo en Estados Unidos para personas mayores de 60 años. Asimismo, un preparado similar llamado Arexvy fue aprobado en julio por la Agencia Europea del Medicamento (EMA), tanto para bebés como para personas de la tercera edad, pero la Comisión Europea debe decidir ahora si aprueba su comercialización en la Unión Europea.
Principal causa de hospitalización de lactantes
Este virus «es una causa común de enfermedad en los niños, y los lactantes se encuentran entre los que corren más riesgo de sufrir una enfermedad grave, lo que puede llevar a la hospitalización», recordó Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA.
El ensayo clínico, en el que participaron unas 7.000 embarazadas, demostró que la vacuna, denominada Abrysvo, reducía la variante grave de la enfermedad en un 82% en los bebés de 0 a 3 meses y en un 69% de 0 a 6 meses. El VRS suele causar síntomas leves como los de un resfriado en lactantes y niños pequeños, pero también neumonía y bronquiolitis.
Se calcula que entre 58.000 y 80.000 niños de menos de cinco años son hospitalizados debido a una infección por VRS, según los Centros para el Control y la Prevención de Enfermedades (CDC), lo que la convierte en la principal causa de hospitalización entre los lactantes.
Efectos secundarios y posteriores estudios
Entre los efectos secundarios más frecuentes en las embarazadas vacunadas con Abrysvo figuran molestias en el lugar de la inyección, dolor de cabeza o muscular y náuseas.
Un peligroso trastorno de la tensión arterial, conocido como preeclampsia, se produjo en el 1,8% de los casos frente al 1,4 % de las que recibieron un placebo. La FDA observó además un desequilibrio en los nacimientos prematuros entre el grupo que recibió la vacuna y el del placebo (5,7 % frente a 4,7 %).
Como consecuencia, la agencia ha pedido a Pfizer que siga estudiando el riesgo de parto prematuro y preeclampsia. Tras la aprobación, el producto debe recibir el visto bueno de los CDC, de modo que no está claro si estará disponible a tiempo para la temporada de VRS de este otoño e invierno.
Referencia: FDA Approves First Vaccine for Pregnant Individuals to Prevent RSV in Infants
Fuente: DW.COM
sep
25
Una mutación genética explica por qué algunas personas contraen herpes labial y otras no, según un estudio reciente. Read more

