abr
18
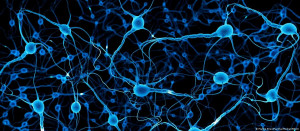 Expertos han conseguido observar y describir la proteína Asc-1 que actúa como una ‘compuerta’ que se abre y se cierra para determinados aminoácidos claves para el aprendizaje.
Expertos han conseguido observar y describir la proteína Asc-1 que actúa como una ‘compuerta’ que se abre y se cierra para determinados aminoácidos claves para el aprendizaje.
Un equipo de investigadores ha logrado observar en una escala atómica la «compuerta» de una proteína que es esencial para el aprendizaje y la memoria, un descubrimiento que podría servir para diseñar fármacos contra la esquizofrenia, el ictus y otras enfermedades neurológicas.
Lo han logrado investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO) de España y otros centros y universidades españoles, y los resultados se han publicado en la revista Nature Communications.
El CNIO señala en una nota difundida este miércoles que todo el comportamiento humano -aprender de una experiencia, recordar una anécdota o modificar una actitud- es el resultado del intercambio de compuestos químicos entre neuronas, los llamados neurotransmisores.
Desentrañar qué ocurre exactamente a escala molecular cuando las neuronas se comunican entre sí, en un proceso llamado «sinapsis», es indispensable para entender el cerebro humano en general, y en particular para contribuir a solucionar problemas de salud mental.
Los investigadores han conseguido observar y describir la estructura de una proteína (la Asc-1) presente en la membrana de las neuronas, una proteína que actúa como una «compuerta» que se abre y se cierra y que actúa como transportador específico para determinados aminoácidos claves para el aprendizaje y la memoria.
La actividad de esa proteína ha recordado el CNIO, se ha relacionado con distintos tipos de enfermedad mental, y conocer su forma tridimensional permitirá el desarrollo de nuevos fármacos para estas patologías.
El científico Óscar Llorca, del CNIO, explica que modular la actividad de esa proteína puede ser una estrategia terapéutica en afecciones como el ictus y la esquizofrenia, y ha precisado que la determinación de su estructura a resolución atómica es importante «porque puede ayudar en la búsqueda de compuestos que modifiquen su actividad».
La colaboración entre los diferentes centros de investigación ha sido clave para desentrañar los misterios de esta proteína y ha ofrecido a los investigadores una visión sin precedentes de su estructura y funcionamiento.
«Este descubrimiento no solo arroja luz sobre la compleja maquinaria celular subyacente a procesos cognitivos fundamentales, sino que también nos acerca al desarrollo de intervenciones terapéuticas más precisas para una gama de trastornos neurológicos», señala Manuel Palacín, jefe del laboratorio de Transportadores de Aminoácidos y Enfermedad del IRB Barcelona y catedrático del Departamento de Bioquímica y Biomedicina Molecular de la Facultad de Biología de la Universidad de Barcelona.
Todas las células del organismo tienen en su membrana «compuertas» para intercambiar sustancias con el medio exterior: proteínas que están continuamente abriéndose y cerrándose según las necesidades de la célula.
Esta proteína (Asc-1) está principalmente en las neuronas del hipocampo y la corteza cerebral, en el cerebro, y se especializa en introducir o sacar de la neurona dos aminoácidos fundamentales para las conexiones neuronales (las sinapsis) implicadas en el aprendizaje, la memoria y la plasticidad cerebral –la capacidad que tiene el sistema nervioso de modificar sus circuitos en respuesta a nuevos entornos–.
Las fluctuaciones en el suministro de esos aminoácidos se han asociado a la esquizofrenia, a los infartos cerebrales, a la ELA y otras enfermedades neurológicas, según el CNIO, que ha observado que desde hace tiempo que se intenta, de momento sin éxito, diseñar fármacos que regulen la actividad de esa enfermedad para tratar estas enfermedades, por lo que conocer con detalle su estructura atómica puede aportar información clave para lograrlo.
17 abril 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
ene
6
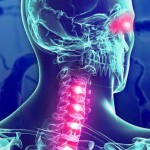 Los investigadores y colaboradores de Mayo Clinic han identificado una proteína expresada en células inmunitarias que podría desempeñar un rol clave en el desarrollo de la esclerosis lateral amiotrófica (ELA), también conocida como enfermedad de Lou Gehrig. El equipo también descubrió que un tratamiento inmunomodulatorio que bloquea la proteína era capaz de restaurar la función motriz en modelos preclínicos. Los hallazgos indican que la proteína, conocida como integrina α5 (pronunciado integrina alfa 5), es un posible blanco terapéutico para la ELA. Read more
Los investigadores y colaboradores de Mayo Clinic han identificado una proteína expresada en células inmunitarias que podría desempeñar un rol clave en el desarrollo de la esclerosis lateral amiotrófica (ELA), también conocida como enfermedad de Lou Gehrig. El equipo también descubrió que un tratamiento inmunomodulatorio que bloquea la proteína era capaz de restaurar la función motriz en modelos preclínicos. Los hallazgos indican que la proteína, conocida como integrina α5 (pronunciado integrina alfa 5), es un posible blanco terapéutico para la ELA. Read more
sep
14
 El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma.
El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma.
El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma, el cáncer cerebral más frecuente y agresivo, según publican los investigadores en la revista ´Nature Cancer´.
Las células del glioblastoma son muy invasivas y se extienden rápidamente desde la masa central del tumor, lo que hace muy difícil su erradicación total. Incluso con los tratamientos actuales, como la temozolomida, la quimioterapia estándar aprobada para tratar el glioblastoma, los tumores resistentes a la temozolomida recidivan en más del 50 % de los pacientes, y menos del 1 % sobrevive diez años después del diagnóstico.
Ahora un equipo de investigadores del Hospital para Niños Enfermos (SickKids), en Canadá, ha presentado un nuevo enfoque terapéutico para el glioblastoma denominado péptido de diseño, dirigido a una interacción proteína-proteína en las células del glioblastoma.
«Al descubrir el papel de una interacción proteína-proteína desconocida hasta ahora en el glioblastoma, hemos podido desarrollar un péptido de diseño que posee una sólida eficacia terapéutica en el tratamiento de los principales tipos de glioblastoma en modelos preclínicos –explica el doctor Xi Huang, científico principal del programa de Biología del Desarrollo y de las Células Madre–. Esto podría constituir la base de la terapia de glioblastoma de próxima generación».
El desarrollo del péptido de diseño comenzó cuando Huang y el primer autor, el doctor Weifan Dong, descubrieron que dos proteínas llamadas EAG2 y Kvbeta2, ambas muy presentes en las células del glioblastoma, interaccionaban en el lugar donde las células cancerosas se encuentran con el tejido cerebral sano.
«Examinamos de cerca estas dos proteínas y descubrimos que cuando interactuaban creaban un complejo de canales de potasio que es fundamental para la naturaleza agresiva del cáncer –explica Dong, antiguo estudiante de doctorado y actual becario posdoctoral en el laboratorio Huang–. Lo sorprendente es que este complejo de canales de potasio EAG2-Kvbeta2 parece formarse sólo en células de glioblastoma, no en células sanas».
Entusiasmado por sus hallazgos, el equipo de Huang empezó a investigar esta interacción específica como posible diana para el tratamiento del glioblastoma. Determinaron que la interacción EAG2-Kvbeta2 es necesaria para que las neuronas se comuniquen con las células del glioblastoma, facilitando el crecimiento tumoral, la invasión y la quimiorresistencia.
El péptido de diseño impide que se produzca la interacción proteína-proteína, frenando el crecimiento e impidiendo que el cáncer se extienda a las células circundantes. En modelos preclínicos, el péptido de diseño también provocó la muerte de células de glioblastoma de todos los subtipos.
«Incluso los tumores que habían desarrollado resistencia a la temozolomida respondieron al péptido de diseño», afirma Dong. «Pero no observamos ningún efecto secundario, probablemente debido a que la interacción EAG2-Kvbeta2 sólo parece estar presente en las células cancerosas».
Ahora, con el apoyo de Industry Partnerships & Commercialization (IP&C) en SickKids, el descubrimiento del péptido de diseño de Huang ha sido protegido mediante la presentación de una solicitud de Tratado de Cooperación en materia de Patentes (PCT), mientras que los esfuerzos de comercialización activos dirigidos por IP&C están en marcha. Juntos, el equipo tiene previsto completar los estudios preclínicos y llevar este péptido de diseño a ensayos clínicos lo antes posible.
Referencia
Dong W, Fekete A, Chen X, Liu H, Beilhartz GL, Chen X, et al. A designer peptide against the EAG2–Kvβ2 potassium channel targets the interaction of cancer cells and neurons to treat glioblastoma. Nat Cancer (2023). https://doi.org/10.1038/s43018-023-00626-8
12/09/2023
Fuente: (IMMedico) Tomado Noticia-Oncología © 2023 Copyright: Publimas Digital
sep
5
 Los investigadores han descubierto que una inyección de un factor sanguíneo específico puede replicar los beneficios del ejercicio en el cerebro. Han descubierto que las plaquetas secretan una proteína, exerkine CXCL4/factor plaquetario 4 o PF4, que rejuvenece las neuronas en ratones ancianos de forma similar al ejercicio físico. Esta proteína, que se libera de las plaquetas después del ejercicio, produce mejoras regenerativas y cognitivas cuando se inyecta en ratones de edad avanzada.
Los investigadores han descubierto que una inyección de un factor sanguíneo específico puede replicar los beneficios del ejercicio en el cerebro. Han descubierto que las plaquetas secretan una proteína, exerkine CXCL4/factor plaquetario 4 o PF4, que rejuvenece las neuronas en ratones ancianos de forma similar al ejercicio físico. Esta proteína, que se libera de las plaquetas después del ejercicio, produce mejoras regenerativas y cognitivas cuando se inyecta en ratones de edad avanzada.
Los efectos beneficiosos de la actividad física sobre el envejecimiento cerebral están bien reconocidos, y las exerquinas, factores que se secretan a la circulación en respuesta al ejercicio, emergen como probables mediadores de esta respuesta. Sin embargo, la fuente y la identidad de estas exerquinas siguen sin estar claras. Aquí proporcionamos evidencia de que las plaquetas secretan una exercina antigerónica.
Mostramos que las plaquetas se activan con el ejercicio y son necesarias para el aumento inducido por el ejercicio en la proliferación de células precursoras del hipocampo en ratones de edad avanzada. También demostramos que el aumento de los niveles sistémicos de la exercina CXCL4/factor plaquetario 4 (PF4) derivada de plaquetas mejora los deterioros cognitivos y regenerativos relacionados con la edad de una manera dependiente de la neurogénesis del hipocampo. En conjunto, estos hallazgos resaltan el papel de las plaquetas en la mediación de los efectos rejuvenecedores del ejercicio durante el envejecimiento fisiológico del cerebro.
Comentarios
Los ensayos preclínicos realizados por investigadores de la Universidad de Queensland han descubierto que una inyección de un factor sanguíneo específico puede replicar los beneficios del ejercicio en el cerebro.
La Dra. Odette Leiter y la Dra. Tara Walker del Queensland Brain Institute de la UQ dirigieron un equipo que descubrió que las plaquetas, las pequeñas células sanguíneas fundamentales para la coagulación de la sangre, secretan una proteína que rejuvenece las neuronas en ratones ancianos de forma similar al ejercicio físico.
«Sabemos que el ejercicio aumenta la producción de nuevas neuronas en el hipocampo, la parte del cerebro importante para el aprendizaje y la memoria, pero el mecanismo no ha quedado claro», afirmó el Dr. Leiter.
«Nuestra investigación anterior ha demostrado que las plaquetas están involucradas, pero este estudio muestra que en realidad se necesitan plaquetas para este efecto en los ratones de edad avanzada».
Los investigadores se centraron en las exercinas, los compuestos biológicos liberados en el torrente sanguíneo durante el ejercicio, que se cree que estimulan la respuesta inducida por el ejercicio en el cerebro.
«Descubrimos que la exerquina CXCL4/factor plaquetario 4 o PF4, que se libera de las plaquetas después del ejercicio, produce mejoras regenerativas y cognitivas cuando se inyecta en ratones de edad avanzada», afirmó el Dr. Leiter.
El Dr. Walker dijo que los hallazgos tienen implicaciones importantes para el desarrollo de intervenciones farmacológicas.
«Para muchas personas con problemas de salud, problemas de movilidad o de edad avanzada, el ejercicio no es posible, por lo que la intervención farmacológica es un área importante de investigación», afirmó.
«Ahora podemos apuntar a las plaquetas para promover la neurogénesis, mejorar la cognición y contrarrestar el deterioro cognitivo relacionado con la edad».
Los investigadores dijeron que el siguiente paso es probar la respuesta en ratones enfermos de Alzheimer, antes de pasar a los ensayos en humanos.
«Es importante tener en cuenta que esto no reemplaza el ejercicio», dijo el Dr. Walker. «Pero podría ayudar a las personas muy mayores o a alguien que haya sufrido una lesión cerebral o un derrame cerebral a mejorar la cognición».
El estudio se publica en Nature Communications.
Referencia
Leiter O, Brici D, Fletcher SJ, Hilary Yong XL, Widagfo J, et al. Platelet-derived exerkine CXCL4/platelet factor 4 rejuvenates hippocampal neurogenesis and restores cognitive function in aged mice. Nat Commun 14, 4375 (2023). https://doi.org/10.1038/s41467-023-39873-9
https://www.nature.com/articles/s41467-023-39873-9
ago
18
 Un factor plaquetario se une a la lista de componentes de la sangre que pueden tener efectos antienvejecimiento.
Un factor plaquetario se une a la lista de componentes de la sangre que pueden tener efectos antienvejecimiento.
Una proteína involucrada en la cicatrización de heridas puede mejorar el aprendizaje y la memoria en ratones envejecidos.
El factor plaquetario 4 (PF4) se conoce desde hace mucho tiempo por su papel en la promoción de la coagulación de la sangre y el sellado de los vasos sanguíneos rotos. Ahora, los investigadores se preguntan si esta molécula de señalización podría usarse para tratar trastornos cognitivos relacionados con la edad, como la enfermedad de Alzheimer. Read more
oct
3
Un equipo científico europeo con participación española ha inyectado a un grupo reducido de participantes con este síndrome la versión sintética de la hormona GnRH con resultados prometedores. Read more