jul
11
Cáncer de pulmón: tercera causa de muerte en España, enlazado al tabaco y detectado tras los 55 años
 Las neoplasias de pulmón se han convertido en la tercera causa de muerte en España, tanto en hombres como mujeres, con un diagnóstico mayoritario en las franjas de 55 a 64 años (30,4 %) y de 65 a 74 (36,1 %) y con un perfil principal de exfumador o fumador activo, según cifras del Grupo Español de Cáncer de Pulmón (GECP).
Las neoplasias de pulmón se han convertido en la tercera causa de muerte en España, tanto en hombres como mujeres, con un diagnóstico mayoritario en las franjas de 55 a 64 años (30,4 %) y de 65 a 74 (36,1 %) y con un perfil principal de exfumador o fumador activo, según cifras del Grupo Español de Cáncer de Pulmón (GECP).
El GECP ha creado el primer Observatorio Nacional en Cáncer de Pulmón con datos de 34 000 pacientes españoles de 90 hospitales, una plataforma de análisis, estudio, reflexión y divulgación sobre la realidad del tumor más mortal en España con el objetivo de avanzar en su supervivencia.
Segunda causa de muerte en hombres y aumenta la mortalidad femenina
De los datos del observatorio se desprende que el cáncer de pulmón causó en 2023 más de 22 700 fallecimientos, con un incremento del 4,2 % en la mortalidad femenina, y se ha convertido en la tercera causa de decesos en España.
En el caso de los hombres, es la segunda causa de fallecimiento por detrás de las enfermedades isquémicas de corazón, escalando así posiciones con respecto a ejercicios anteriores.
Solo el 13,3 % de diagnósticos se dan antes de los 55 años, de forma que el perfil mayoritario se encuentra por encima de esta franja de edad, con el agravante de que el 54,6 % de las detecciones se producen cuando el cáncer está en estadios avanzados, frente al 10,3 % en iniciales.
Cuáles son los principales síntomas del cáncer de pulmón
Los casos de neoplasias de pulmón se dan principalmente en exfumadores (46,5 %) y son mayores que los de fumadores en activo (40,5 %), mientras que en las personas que nunca han fumado la cota baja al 11,5 %.
Aunque el mayor número de diagnósticos se produce en hombres (20 368), la cantidad de mujeres con cáncer de pulmón va en aumento (7 564), según el GECP.
Registro nacional y unificado
El registro creado por el GEPC es la primera base de datos unificada sobre este tipo de tumor y que, a diferencia de otros, incluye información tan relevante como variables sociodemográficas, clínicas, moleculares, genéticas y de resultado al tratamiento de los pacientes.
Pretende ser un referente para los especialistas de cara a la próxima década.
El presidente del GECP, Mariano Provencio, ha explicado que en el abordaje de las neoplasias de pulmón son necesarios «datos de la vida real para tomar decisiones», ya que en España carecía de «un registro unificado de los casos de cáncer» que incluyera «información y variables relevantes».
Ha añadido Provencio, que también es jefe de Oncología del Hospital Puerta de Hierro de Madrid, que la iniciativa permitirá contar con «un enfoque multidisciplinar de los datos» que permitan «detectar a tiempo cualquier evolución».
Tumores con alta letalidad
Por su parte, Bartomeu Massuti, secretario del GECP y jefe de Oncología del Hospital Universitario Doctor Balmis de Alicante, ha apuntado que las neoplasias de pulmón se encuentran «por encima del resto de tumores en cuanto a letalidad».
Por ello, ha señalado que es necesaria más investigación e inversión para esta patología, así como ampliar el conocimiento del tumor para poder mejorar las estrategias de abordaje.
«Cada año se diagnostican en España aproximadamente 31 000 casos de cáncer de pulmón, que crece cada vez más en el sexo femenino, suponiendo ya 1 de cada 4 pacientes», ha zanjado Massuti.
09 julio 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
jul
9
 La Organización Mundial de la Salud (OMS) clasificó hoy al talco y al acrilonitrilo como productos probablemente cancerígenos, tras varios estudios realizados por expertos del Centro Internacional de Investigaciones sobre el Cáncer.
La Organización Mundial de la Salud (OMS) clasificó hoy al talco y al acrilonitrilo como productos probablemente cancerígenos, tras varios estudios realizados por expertos del Centro Internacional de Investigaciones sobre el Cáncer.
Tales resultados fueron publicados este viernes en la revista especializada The Lancet Oncology, el cual analiza dos entornos: el laboral donde los trabajadores están en contacto con el mineral durante la extracción, molienda o procesamiento del talco.
El segundo examina la población general expuesta al uso de cosméticos y polvos corporales que contienen talco.
Si bien las investigaciones no confirmaron una conexión estrictamente directa, la OMS decidió clasificar como probablemente cancerígeno al producto luego de una combinación de estudios parciales en seres humanos -apuntados a desentrañar el cáncer de ovario- y una serie de pruebas realizadas en animales de laboratorio.
El talco es un mineral extraído en muchas regiones del mundo y empleado para cientos de productos, sin embargo, los expertos no descartan ciertos sesgos en los estudios que mostraron un aumento en la incidencia de cáncer.
Uno de los primeros estudios se realizó en la década de 1970, al surgir una preocupación sobre la contaminación del talco con amianto, que a menudo se encuentra cerca de los minerales utilizados para fabricarlo. Posteriormente, se detectó un mayor riesgo de cáncer de ovario en las usuarias de ese polvo, apuntó la OMS.
La agencia sanitaria de la ONU también clasificó como cancerígeno para los humanos al acrilonitrilo, un compuesto orgánico volátil utilizado principalmente en la producción de polímeros, a partir de pruebas suficientes de cáncer de pulmón y pruebas limitadas de cáncer de vejiga.
Estos polímeros se utilizan en fibras para ropa, alfombras, plásticos para productos de consumo o piezas de automóviles, también están presentes en el humo del cigarrillo por lo que la contaminación del aire constituye otra fuente de exposición de la población.
05 julio 2024|Fuente: Prensa Latina |Tomado de |Noticia
jul
6
 Realizar ejercicios físicos sencillos junto con el tratamiento del cáncer puede prevenir en muchos casos los daños nerviosos que ocasiona la quimioterapia, para los cuales los medicamentos demuestran ser ineficaces, publicó hoy una revista especializada.
Realizar ejercicios físicos sencillos junto con el tratamiento del cáncer puede prevenir en muchos casos los daños nerviosos que ocasiona la quimioterapia, para los cuales los medicamentos demuestran ser ineficaces, publicó hoy una revista especializada.
Así lo demostró un estudio realizado por un grupo de investigadores de la Universidad de Basilea (Suiza), junto con un equipo interdisciplinario de Alemania, cuyos hallazgos aparecen divulgados en JAMA Internal Medicine.
En la pesquisa participaron 158 pacientes de cáncer, de ambos sexos, que recibían tratamiento con oxaliplatino o con alcaloides de la vinca, y fueron divididos al azar en tres grupos.
El primero fue un grupo de control, cuyos miembros recibieron la atención estándar, en tanto los otros dos completaron sesiones de ejercicio dos veces por semana, entre 15 y 30 minutos, en el periodo que duró su quimioterapia.
Uno de estos grupos realizó ejercicios que se centraron principalmente en el equilibrio sobre una superficie cada vez más inestable, mientras el otro entrenó en una plataforma vibratoria.
Los exámenes periódicos realizados durante los siguientes cinco años mostraron que en el grupo de control, aproximadamente el doble de participantes desarrollaron neuropatía periférica inducida por la quimioterapia que en cualquiera de los conjuntos que practicaron ejercicios.
Mientras, los ejercicios realizados junto con la quimioterapia pudieron reducir la incidencia de daño a los nervios entre un 50 y un 70 por ciento.
A la par aumentaron la calidad de vida percibida subjetivamente por los pacientes, hicieron menos necesario disminuir la dosis de medicamentos contra el cáncer y redujeron la mortalidad en los cinco años posteriores a la quimioterapia.
Los expertos detallaron que los participantes que recibieron alcaloides de la vinca y realizaron entrenamiento sensoriomotor tuvieron el mayor beneficio.
04 julio 2024|Fuente: Prensa Latina |Tomado de |Noticia
jul
6
 Agentes infecciosos virulentos como el coronavirus SARS-CoV-2 pueden inducir daño tisular y, ahora, un estudio liderado por la Universidad de California en San Diego (Estados Unidos) propone un nuevo enfoque para tratar la covid-19: usar un medicamento experimental contra el cáncer.
Agentes infecciosos virulentos como el coronavirus SARS-CoV-2 pueden inducir daño tisular y, ahora, un estudio liderado por la Universidad de California en San Diego (Estados Unidos) propone un nuevo enfoque para tratar la covid-19: usar un medicamento experimental contra el cáncer.
Hace doce años, investigadores oncológicos de este centro universitario identificaron una molécula que ayuda a las células cancerosas a sobrevivir transportando células inflamatorias nocivas al tejido tumoral.
En esta nueva investigación, demuestran que la misma molécula hace lo mismo en el tejido pulmonar infectado por covid-19, y que la molécula puede suprimirse con un fármaco contra el cáncer reorientado.
El trabajo, publicado en Science Translational Medicine, representa un nuevo enfoque para prevenir daños irreversibles en órganos en enfermedades como la covid-19 y el SARM (acrónimo de Staphylococcus aureus resistente a la meticilina), que no mejora con el tipo de antibióticos usados para las infecciones por estafilococos.
Los dos actores clave en este planteamiento son unas células inflamatorias llamadas células mieloides y la enzima PI3K gamma, explica un comunicado de la universidad.
Las células mieloides pertenecen al sistema inmunitario innato -la inmunidad con la que se nace antes de exponerse a los agentes patógenos del entorno- y actúan con gran rapidez para eliminar agentes mortales como el SARS-CoV-2, el virus causante de la covid-19.
El trabajo demuestra que los fármacos capaces de impedir el reclutamiento de células mieloides dañinas en tejidos infectados por agentes graves, como la covid-19 o el SARM, tienen un efecto beneficioso significativo en la preservación de la función tisular, si se administran en una fase suficientemente temprana de la infección, afirma la investigadora Judith Varner.
La mayoría de los fármacos covid se dirigen contra el virus, ya sea previniendo la infección o impidiendo que este produzca más de sí mismo después de esta. El enfoque actual se dirige al huésped, evitando que el sistema inmunitario reaccione de forma exagerada o que se acumulen fibras en los pulmones.
Las células mieloides protegen, pero también pueden hacer mucho daño, explica Varner. Si se tiene una pequeña infección, entran en acción, matan bacterias, liberan alertas que reclutan células inmunitarias asesinas aún más potentes y producen sustancias que pueden curar el daño.
Pero si la infección es demasiado fuerte, se produce una sobreproducción de estas señales de alerta y las sustancias que liberan para matar a los agentes infecciosos también pueden afectar al paciente; eso ocurre en la covid.
PI3K gamma promueve el movimiento de las células mieloides hacia los tejidos cancerosos, como descubrió el equipo hace doce años. El trabajo actual demuestra que esta enzima también ayuda a mover las células mieloides hacia tejidos infectados con SARS-CoV-2.
Esta constatación llevó al equipo a pensar que un fármaco contra el cáncer que inhibe PI3K gamma, llamado eganelisib, podría ser eficaz en la supresión de la inflamación en covid-19 mediante la anulación de la capacidad de la citada enzima para mover las células mieloides en el tejido infectado.
Los investigadores secuenciaron tejido pulmonar de pacientes con covid y vieron que muchas de sus células pulmonares mueren y hay un enorme aumento de células mieloides. También descubrieron lo mismo en ratones infectados.
El equipo comprobó que el eganelisib -aún no aprobado por la Administración de Alimentos y Medicamentos de Estados Unidos- impide la entrada de las células mieloides en el tejido para que no puedan hacer todo ese daño. Estudios posteriores determinarán si realmente puede revertir el daño, señalan los investigadores, que también obtuvieron los mismos resultados en ratones infectados con SARM.
04 julio 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
jun
14
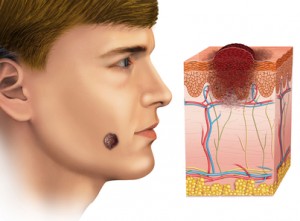 Protegerse del sol en edades tempranas, especialmente durante los primeros 30 años y no solo con crema, es clave para reducir el riesgo de cáncer de piel durante el resto de la vida, sobre todo en un contexto de cambio climático que aumenta los días de sol y la radiación.
Protegerse del sol en edades tempranas, especialmente durante los primeros 30 años y no solo con crema, es clave para reducir el riesgo de cáncer de piel durante el resto de la vida, sobre todo en un contexto de cambio climático que aumenta los días de sol y la radiación.
Así lo explica a EFE la doctora Susana Puig Sardá, jefa del Servicio de Dermatología del Hospital Clínic de Barcelona, con motivo del Día Mundial del Cáncer de Piel.
«Gracias a la cultura de las medidas de fotoprotección, la incidencia de estas enfermedades en poblaciones jóvenes está estabilizada y no se incrementa, a diferencia de los mayores de 60 años», sostiene la doctora Puig.
Esta diferencia entre generaciones se explica por los hábitos durante los años 60, cuando se popularizó la exposición solar recreacional sin medidas de fotoprotección, junto con el incremento de la esperanza de vida.
Así, es en la franja de los mayores de 60 años que de jóvenes no se protegieron entre los que los cánceres de piel están aumentando «exponencialmente», según la dermatóloga.
En cambio, para las nuevas generaciones la exposición al sol se ha visto agravada por el contexto del cambio climático, otro de los factores de riesgo a tener en cuenta que señala la dermatóloga y que debe tomarse en consideración para prevenir los problemas en la piel.
«En Barcelona, por ejemplo, el número de días soleados se ha visto incrementado en las últimas décadas, así como el Índice de Radiación Ultravioleta (IUV)», especifica la responsable de Dermatología del Clínic.
Es por eso que lamenta que la población solo haya aumentado el uso de las cremas fotoprotectoras para protegerse, cuando son necesarias a su juicio más medidas.
«Habría que cambiar los horarios de las actividades al aire libre, usar sombras naturales y usar más gorras y sombreros, por ejemplo», así como «fomentar los diagnósticos precoces», resalta.
Independientemente del tipo de piel, color del pelo y de los ojos, factores históricamente relacionados con un mayor o menor riesgo de contraer enfermedades de la piel, existen otros aspectos que inciden en la gravedad de la exposición al sol, como el momento del día o los productos de protección.
Sobre estos últimos, el presidente de la Federación de Asociaciones de Farmacias de Cataluña (FEFAC), Antoni Torres, advierte de que deben ser cremas solares con protección 50+ y preferiblemente de farmacias, donde «pueden asesorar al cliente en función de sus casos particulares».
«La cantidad del fotoprotector para estar protegido durante dos horas es de nueve cucharas medias (de café con leche), protegiendo cara, brazos, piernas, pecho, espalda, y la parte de detrás de ambas piernas», puntualiza a EFE el experto, quien añade una décima cuchara para la cabeza, sobre todo en casos de alopecia.
Torres hace hincapié en que, cuando llega el calor, hay que ponerse crema por la mañana y luego, cada dos horas, aunque en el caso de que la exposición se prolongue o haya una excesiva sudoración, debería ser cada hora, y así hasta que se vaya el sol.
«Acertar en la cantidad es esencial, porque si no es la correcta, no protege. Una protección que debería durar dos horas puede hacer efecto solo media hora o incluso menos», asevera el presidente de la FECAC.
Aparte de la herencia cultural que afecta a los más mayores y a la cantidad y calidad de los productos de fotoprotección, hay otro elemento que se añade a la lista de factores a tener en cuenta para evitar enfermedades dermatológicas: la presión estética.
«Uno de los grandes problemas que tenemos es la valoración estética. Debemos hacer un cambio y tener como modelos, por ejemplo, personas con pieles claras y cuidadas», revela la doctora Susana Puig.
La jefa del Servicio de Dermatología del Clínic vincula esta tendencia a la tanorexia o adicción al bronceado, una condición en la cual una persona genera una necesidad obsesiva para lograr un tono de piel más oscuro.
«El daño que hace la radiación ultravioleta produce la hormona alfa-MSH, que actúa a nivel de receptores opiáceos y crea esta adicción. Sin embargo, protegerse del sol es la mejor estrategia para protegerse de las arrugas y el envejecimiento cutáneo», concluye la doctora Puig. EFE
13 junio 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
jun
11
 Los primeros resultados de los estudios en fase preclínica de una vacuna contra el cáncer podrían presentarse ya a finales de este año, declaró hoy el ministro ruso de Salud, Mijaíl Murashko.
Los primeros resultados de los estudios en fase preclínica de una vacuna contra el cáncer podrían presentarse ya a finales de este año, declaró hoy el ministro ruso de Salud, Mijaíl Murashko.
El titular, quien intervino al margen del XXVII del Foro Económico Internacional de San Petersburgo (Spief por sus siglas en inglés) añadió que la vacuna se somete ahora a estudios preclínicos, cuyos primeros resultados esperan recibir a finales de año para pasar después a los ensayos clínicos.
Murashko explicó que la vacuna fue desarrollada conjuntamente por varios equipos científicos: el Centro Nacional de Investigación de Epidemiología y Microbiología Gamaleya, el Instituto de Investigación Oncológica Herzen de Moscú y el Centro de Investigación del Cáncer Blojin.
El Foro Económico Internacional de San Petersburgo se llevó a cabo del 5 al 8 de junio. El tema del encuentro de este año fue La base de un mundo multipolar: formación de nuevos puntos de crecimiento. El evento estuvo organizado por la Fundación Roscongress.
09 junio 2024|Fuente: Prensa Latina |Tomado de |Noticia

