oct
7
 El equipo de Carlos Simón abre la puerta a un diagnóstico más preciso y a enfoques terapéuticos más efectivos para las mujeres que padecen síndrome de Asherman.
El equipo de Carlos Simón abre la puerta a un diagnóstico más preciso y a enfoques terapéuticos más efectivos para las mujeres que padecen síndrome de Asherman.
«Por primera vez en la historia, hemos logrado decodificar los mecanismos celulares y moleculares del síndrome de Asherman durante la fase secretora del ciclo menstrual.
Este logro representa un hito de gran relevancia en el entendimiento de esta patología, con un potencial impacto significativo en la práctica médica», señala a DM Carlos Simón, catedrático de Obstetricia y Ginecología en la Universidad de Valencia.
Junto a su equipo investigador de la Universidad de Valencia, Instituto de Investigación Sanitaria (Incliva) y Fundación Carlos Simón, ha publicado los datos de un trabajo en Nature Communications que describe por primera vez las alteraciones celulares responsables del síndrome de Asherman a nivel de célula única.
Este síndrome constituye una enfermedad rara caracterizada por formación de tejido cicatricial intrauterino que causa alteraciones menstruales e infertilidad. En la mayoría de los casos, la enfermedad aparece después de una cirugía en el útero, aunque en otros casos, una infección pélvica grave no relacionada con procedimientos quirúrgicos puede conducir a su desarrollo.
Según Simón, «los biomarcadores identificados y la comprensión de las vías biológicas involucradas abren la puerta a un diagnóstico más preciso y a enfoques terapéuticos más efectivos para las mujeres que padecen esta enfermEnsayos con células madre de médula
El estudio titulado Decoding the endometrial niche of Asherman’s Syndrome at single-cell resolution, además de describir por primera vez las alteraciones celulares responsables del síndrome de Asherman a nivel de célula única, también identifica los perfiles de expresión génica que crean un entorno disfuncional, provocando la formación de tejido cicatricial, inflamación y alteraciones vasculares.
Para desarrollar este estudio se reclutaron pacientes diagnosticadas con síndrome de Asherman moderado o grave. Además, se contó con mujeres fértiles y donantes sanas como grupos de control.
Se analizaron más de 200.000 células provenientes del endometrio de pacientes con síndrome de Asherman y controles sanos.
Estas pacientes forman parte de un estudio clínico en curso, actualmente en fase I/II, que busca validar los efectos de la terapia con células madre procedentes de la médula ósea de las propias pacientes (CD133+) en sus resultados clínicos reproductivos.
- inculan el inicio precoz de la menstruación con más riesgo de problemas de conducta en la adultez
- La fluctuación hormonal de la menstruación afecta al mecanismo de recompensa
- Anticoncepción, menstruación y menopausia, los temas de salud que más preocupan a las mujeres
Los investigadores también se crearon organoides endometriales a partir de pacientes afectadas y mujeres sanas. Estos organoides -endometrios miniaturizados generados en el laboratorio- mostraron rasgos similares a los del tejido endometrial in vivo, «lo que sugiere que estos organoides son un buen modelo in vitro para estudiar el síndrome de Asherman», indican.
Además, mediante la incorporación de modelos de aprendizaje automático de vanguardia, el equipo de investigación descifró las diferencias transcriptómicas entre las células endometriales in vivo e in vitro de controles y pacientes, lo que proporcionó mayor información sobre las alteraciones del microambiente endometrial en la enfermedad
Ver texto completo:
Santamaria X, Roson B, Perez Moraga R, Venkatesan N, Pardo Figuerez M, Gonzalez Fernandez J, et al. Decoding the endometrial niche of Asherman’s Syndrome at single-cell resolution. Nat Commun[Internet]. 2023[6 oct 2023];14(1):5890. doi: 10.1038/s41467-023-41656-1.
7 0ctubre 2023 | Fuente: Diario Médico| Tomado de Medicina | Ginecología y Obstetricia
sep
14
 El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma.
El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma.
El descubrimiento de una diana molecular desconocida hasta ahora ha inspirado lo que podría convertirse en un gran avance terapéutico para los enfermos de glioblastoma, el cáncer cerebral más frecuente y agresivo, según publican los investigadores en la revista ´Nature Cancer´.
Las células del glioblastoma son muy invasivas y se extienden rápidamente desde la masa central del tumor, lo que hace muy difícil su erradicación total. Incluso con los tratamientos actuales, como la temozolomida, la quimioterapia estándar aprobada para tratar el glioblastoma, los tumores resistentes a la temozolomida recidivan en más del 50 % de los pacientes, y menos del 1 % sobrevive diez años después del diagnóstico.
Ahora un equipo de investigadores del Hospital para Niños Enfermos (SickKids), en Canadá, ha presentado un nuevo enfoque terapéutico para el glioblastoma denominado péptido de diseño, dirigido a una interacción proteína-proteína en las células del glioblastoma.
«Al descubrir el papel de una interacción proteína-proteína desconocida hasta ahora en el glioblastoma, hemos podido desarrollar un péptido de diseño que posee una sólida eficacia terapéutica en el tratamiento de los principales tipos de glioblastoma en modelos preclínicos –explica el doctor Xi Huang, científico principal del programa de Biología del Desarrollo y de las Células Madre–. Esto podría constituir la base de la terapia de glioblastoma de próxima generación».
El desarrollo del péptido de diseño comenzó cuando Huang y el primer autor, el doctor Weifan Dong, descubrieron que dos proteínas llamadas EAG2 y Kvbeta2, ambas muy presentes en las células del glioblastoma, interaccionaban en el lugar donde las células cancerosas se encuentran con el tejido cerebral sano.
«Examinamos de cerca estas dos proteínas y descubrimos que cuando interactuaban creaban un complejo de canales de potasio que es fundamental para la naturaleza agresiva del cáncer –explica Dong, antiguo estudiante de doctorado y actual becario posdoctoral en el laboratorio Huang–. Lo sorprendente es que este complejo de canales de potasio EAG2-Kvbeta2 parece formarse sólo en células de glioblastoma, no en células sanas».
Entusiasmado por sus hallazgos, el equipo de Huang empezó a investigar esta interacción específica como posible diana para el tratamiento del glioblastoma. Determinaron que la interacción EAG2-Kvbeta2 es necesaria para que las neuronas se comuniquen con las células del glioblastoma, facilitando el crecimiento tumoral, la invasión y la quimiorresistencia.
El péptido de diseño impide que se produzca la interacción proteína-proteína, frenando el crecimiento e impidiendo que el cáncer se extienda a las células circundantes. En modelos preclínicos, el péptido de diseño también provocó la muerte de células de glioblastoma de todos los subtipos.
«Incluso los tumores que habían desarrollado resistencia a la temozolomida respondieron al péptido de diseño», afirma Dong. «Pero no observamos ningún efecto secundario, probablemente debido a que la interacción EAG2-Kvbeta2 sólo parece estar presente en las células cancerosas».
Ahora, con el apoyo de Industry Partnerships & Commercialization (IP&C) en SickKids, el descubrimiento del péptido de diseño de Huang ha sido protegido mediante la presentación de una solicitud de Tratado de Cooperación en materia de Patentes (PCT), mientras que los esfuerzos de comercialización activos dirigidos por IP&C están en marcha. Juntos, el equipo tiene previsto completar los estudios preclínicos y llevar este péptido de diseño a ensayos clínicos lo antes posible.
Referencia
Dong W, Fekete A, Chen X, Liu H, Beilhartz GL, Chen X, et al. A designer peptide against the EAG2–Kvβ2 potassium channel targets the interaction of cancer cells and neurons to treat glioblastoma. Nat Cancer (2023). https://doi.org/10.1038/s43018-023-00626-8
12/09/2023
Fuente: (IMMedico) Tomado Noticia-Oncología © 2023 Copyright: Publimas Digital
sep
9
 Redacción Ciencia, 6 sep (EFE). – El cerebro está formado por dos grandes familias de células: las neuronas y las células gliales. Al menos hasta ahora, pues un grupo de científicos ha descubierto un nuevo tipo, lo que abre ‘inmensas perspectivas de investigación’ en enfermedades como el alzhéimer y el párkinson. Los detalles sobre el nuevo tipo de célula los publica Nature en un estudio coordinado por investigadores de la Universidad de Lausana (Suiza).
Redacción Ciencia, 6 sep (EFE). – El cerebro está formado por dos grandes familias de células: las neuronas y las células gliales. Al menos hasta ahora, pues un grupo de científicos ha descubierto un nuevo tipo, lo que abre ‘inmensas perspectivas de investigación’ en enfermedades como el alzhéimer y el párkinson. Los detalles sobre el nuevo tipo de célula los publica Nature en un estudio coordinado por investigadores de la Universidad de Lausana (Suiza).
Desde que existe la Neurociencia, se reconoce que el cerebro funciona principalmente gracias a las neuronas y a su capacidad para elaborar y transmitir rápidamente información a través de sus redes. Para apoyarlas en esta tarea, las células gliales desempeñan una serie de funciones estructurales, energéticas e inmunitarias, además de estabilizar las constantes fisiológicas.
El nuevo descubrimiento, que han denominado ‘astrocitos glutamatérgicos’, es una célula híbrida, a medio camino entre las neuronas y las células gliales. Algunas de las células gliales, conocidas como astrocitos, rodean íntimamente las sinapsis, los puntos de contacto donde se liberan los neurotransmisores para transmitir información entre neuronas.
Esta es la razón por la que los neurocientíficos han sugerido durante mucho tiempo que los astrocitos pueden tener un papel activo en la transmisión sináptica y participar en el procesamiento de la información, pero los estudios realizados daban resultados contradictorios.
Al identificar un nuevo tipo de célula con las características de un astrocito y que expresa la maquinaria molecular necesaria para la transmisión sináptica, el equipo ha puesto fin a años de controversia, considera la Universidad de Lausana (UNIL) en un comunicado.
Las implicaciones de este descubrimiento se extienden a los trastornos cerebrales. Al alterar específicamente los astrocitos glutamatérgicos, el equipo demostró efectos sobre la consolidación de la memoria, pero también observó vínculos con patologías como la epilepsia, cuyos ataques se exacerbaban.
El estudio muestra que este nuevo tipo de célula también tiene un papel en la regulación de los circuitos cerebrales implicados en el control del movimiento y podría ofrecer dianas terapéuticas para la enfermedad de Parkinson.
Este descubrimiento ‘abre inmensas perspectivas de investigación’, aseguró Andrea Volterra, de la UNIL y autor principal del estudio. Los próximos estudios ‘explorarán el posible papel protector de este tipo de célula frente al deterioro de la memoria en la enfermedad de Alzheimer, así como su función en otras regiones y patologías distintas de las exploradas aquí’, agregó.
En su estudio, el equipo trató de averiguar si estas células híbridas eran funcionales, es decir, capaces de liberar realmente glutamato con una velocidad comparable a la de la transmisión sináptica, para lo que usó una técnica de imagen que permite ver el glutamato liberado por las vesículas en tejidos cerebrales y en ratones vivos. ‘Hemos identificado un subgrupo de astrocitos que responden a estímulos selectivos con una rápida liberación de glutamato, que se produce en zonas espacialmente delimitadas de estas células que recuerdan a las sinapsis’, dijo Volterra.
Además, demostraron que ‘son células que modulan la actividad neuronal, controlan el nivel de comunicación y excitación de las neuronas’, afirmó Roberta de Ceglia, primera autora del estudio e investigadora principal del UNIL. Y sin esta maquinaria funcional, el estudio demuestra que la potenciación a largo plazo, un proceso neuronal implicado en los mecanismos de memorización, se ve alterada y que la memoria de los ratones se ve afectada.
Referencia
Ceglia R de, Ledonne A, Litvin DG, Lykke Lind B, Carriero G, Latagliata EC, et al. Specialized astrocytes mediate glutamatergic gliotransmission in the CNS. Nature, 2023. https://doi.org/10.1038/s41586-023-06502-w
https://www.nature.com/articles/s41586-023-06502-w
Fuente: Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
ago
31
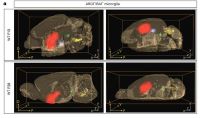 La investigación, liderada en conjunto por la Universidad de Sevilla- IBiS y el Karolinska Institutet, ayuda a entender como maduran los sistemas neuronales con funciones decisivas para el comportamiento humano. En profundidad, el estudio resalta el papel de la microglía, un conjunto celular del cual estamos experimentando una eclosión de información muy importante durante los últimos años por su implicación en diversas patologías cerebrales como la enfermedad de Alzheimer. Read more
La investigación, liderada en conjunto por la Universidad de Sevilla- IBiS y el Karolinska Institutet, ayuda a entender como maduran los sistemas neuronales con funciones decisivas para el comportamiento humano. En profundidad, el estudio resalta el papel de la microglía, un conjunto celular del cual estamos experimentando una eclosión de información muy importante durante los últimos años por su implicación en diversas patologías cerebrales como la enfermedad de Alzheimer. Read more
abr
12
El desarrollo de embriones humanos y la formación temprana de órganos siguen sin explorarse en gran medida debido a los problemas éticos relacionados con el uso de embriones para investigación, así como a la disponibilidad limitada de materiales para estudiar. Ahora, un equipo de investigadores de China ha logrado por primera vez crear estructuras similares a embriones a partir de células madre embrionarias de mono. Los investigadores también transfirieron estas estructuras similares a embriones en los úteros de monos hembra y determinaron que las estructuras podían implantarse y provocar una respuesta hormonal similar al embarazo. Los resultados del trabajo se publican en la revista Cell Stem Cell.
«Los mecanismos moleculares de la embriogénesis y la organogénesis humana no están muy claros», dice el coautor Zhen Liu, de la Academia de Ciencias de China (CAS, por sus siglas en inglés) en Shanghái. «Debido a que los monos están estrechamente relacionados con los humanos desde el punto de vista evolutivo, esperamos que el estudio de estos modelos contribuya a profundizar en nuestra comprensión del desarrollo embrionario humano, lo que incluye arrojar luz sobre algunas de las causas de los abortos espontáneos tempranos«, añade Zhen Liu.
«Esta investigación ha creado un sistema similar a un embrión que puede inducirse y cultivarse indefinidamente», dice el coautor correspondiente Quian Sun, también de la CAS. Apunta, además, que el trabajo desarrollado «proporciona nuevas herramientas y perspectivas para la exploración posterior de embriones de primates y la salud médica reproductiva«.
Los investigadores comenzaron con células madre embrionarias de macacos a las que expusieron a una serie de factores de crecimiento en cultivo celular. Estos factores indujeron a las células madre a formar estructuras similares a embriones, por primera vez, utilizando células de primates no humanos.
Cuando se estudiaron bajo un microscopio, se encontró que las estructuras similares a embriones, también llamadas blastoides, tenían una morfología similar a los blastocistos naturales. A medida que se desarrollaron más in vitro , formaron estructuras que se parecían al amnios (saco membranoso más interno que rodea y protege al embrión en desarrollo) y al saco vitelino (anexo embrionario que produce y transporta nutrientes y oxígeno hacia el embrión). Los blastoides también comenzaron a formar los tipos de células que eventualmente forman las tres capas germinales del cuerpo. La secuenciación de ARN de una sola célula reveló que los diferentes tipos de células que se encuentran dentro de las estructuras tenían patrones de expresión génica similares a las células que se encuentran en blastocistos naturales o embriones posteriores a la implantación.
A continuación, los blastoides se transfirieron a los úteros de ocho monas hembras; en tres de ellas se implantaron las estructuras y esta implantación dio lugar a la liberación de progesterona y gonadotropina coriónica, hormonas normalmente asociadas al embarazo. Los blastoides también formaron sacos de gestación temprana, estructuras llenas de líquido que se desarrollan al principio del embarazo para albergar un embrión, y líquido amniótico. Sin embargo, no formaron fetos y las estructuras desaparecieron aproximadamente al cabo de una semana.
En trabajos futuros, los investigadores planean centrarse en desarrollar aún más el sistema de cultivo de estructuras similares a embriones a partir de células de mono. «Esto nos proporcionará un modelo útil para estudios futuros», dice el coautor correspondiente Fan Zhou de la Universidad de Tsinghua. «Una mayor aplicación de blastoides de mono puede ayudar a diseccionar los mecanismos moleculares del desarrollo embrionario de los primates».
Los investigadores reconocen los problemas éticos que rodean a este tipo de investigación, pero subrayan que sigue habiendo muchas diferencias entre estas estructuras similares a embriones y los blastocistos naturales. Y lo que es más importante, las estructuras embrionarias no tienen pleno potencial de desarrollo. Señalan que para que este campo avance es importante que haya debates entre la comunidad científica y el público.
Alfonso Martínez Arias, profesor de investigación ICREA e investigador en Sistemas de Bioingeniería-MELIS de la Universidad Pompeu Fabra, explica, en declaraciones a Science Media Centre España (SMC), que el estudio «es un paso en la caracterización de modelos del desarrollo embrionario basados en células madre embrionarias. Este trabajo está basado en los estudios pioneros de Nicolas Rivron, que fue el primero en construir blastocistos con células madre. El blastocisto es el primer hito en el desarrollo de un mamífero y, por supuesto, de un ser humano. Rivron fue capaz de construir estructuras similares a blastocistos de ratón y humano que llamó blastoides».
Martínez Arias añade que, «desde el punto de vista estructural (genes que expresan sus células), los blastoides son casi idénticos a sus homólogos naturales, los blastocistos. Sin embargo, la prueba de lo que son es funcional. Lo que hace el blastocisto es implantarse en el útero y, una vez bien asentado, comenzar la construcción del organismo con el proceso de gastrulación: la generación de las semillas de cada tejido y órgano a la vez que se ordenan en el espacio». En cualquier caso, este investigador reconoce que «hasta ahora no había evidencia de que los blastoides pudieran implantarse correctamente e iniciar el desarrollo del embrión. En el caso de los humanos, por razones éticas obvias».
En opinión de Martínez Arias, los datos del trabajo de los investigadores chinos «parecen de buena calidad, y aunque la frecuencia de éxito es baja, la demostración de que estos blastoides implantan parece segura. Menos claro es si gastrulan (el proceso por el que el embrión adquiere tres capas germinales» y añade: «Mi impresión es que el proceso de gastrulación es defectuoso. Los pocos embriones que inician esta fase crucial del desarrollo colapsan al poco de iniciar el proceso.
Modelo para estudiar fases del desarrollo
Según dice, el trabajo es un paso más en la caracterización de estos modelos de desarrollo basados en células madre embrionarias y habrá otros, pero «su valor dependerá de dos cosas: la reproducibilidad y la demostración de su valor científico en aportar conocimiento nuevo. Lo último está, por el momento, lejos. Los macacos y los humanos son diferentes, incluso en la manera en la que los blastocistos implantan». Para él este trabajo «es una prueba de concepto que será un reto reproducir por el coste de la investigación -trabajar con primates no es fácil ni asequible-, pero claramente es una evidencia de que los blastoides serán, son, una herramienta útil para estudiar los primeros pasos de la implantación uterina, que afectan a muchos aspectos de la infertilidad«.
Antonio Urries, director de la Unidad de Reproducción Asistida del Hospital Quirónsalud de Zaragoza y presidente de la Asociación para el Estudio de la Biología de la Reproducción (Asebir), aclara en SMC que lo que han desarrollado estos investigadores «no son embriones propiamente dichos, sino estructuras embrioides capaces de comportarse como un embrión en sus primeros días de desarrollo». Recuerda además, que «ya se han conseguido generar con éxito este tipo de estructuras embrioides en humanos con morfología y estructuras similares a los embriones naturales, pero no está permitido su cultivo más allá del día 14 ni su implantación en el útero de una mujer debido a cuestiones éticas«. Por ello, cree que «poder hacer este tipo de investigaciones en una especie tan estrechamente relacionada con la nuestra supone un modelo ideal para el estudio en detalle de las primeras fases de desarrollo de órganos tan vitales de los mamíferos como son el corazón, cerebro o tubo neural. El comienzo de la organogénesis».
Urries también defiende que este trabajo «puede ayudar a profundizar en determinados mecanismos de implantación y comprender por qué fallan los embarazos, detectando aquellas anomalías que pueden generar abortos. Igualmente, nos puede guiar en el desarrollo de órganos y tejidos sintéticos para trasplantes y conocer el origen de algunas enfermedades». El presidente de Asebir reconoce que lo logrado «tiene las limitaciones propias de ser una técnica en fase muy preliminar, fruto de un proceso muy complicado e ineficiente (alrededor del 25%), pero con un gran potencial a futuro y una aplicabilidad en humanos muy esperanzadora».
Por último, Lluís Montoliu, investigador en el Centro Nacional de Biotecnología (CNB-CSIC) y en el CIBERER-ISCIII, en declaraciones recogidas por SMC, señala que el estudio «no reporta el nacimiento de ningún bebé macaco por el momento. Este es un experimento que no puede realizarse en humanos, por las limitaciones técnicas, legales y éticas asociadas, pero estudios como este, realizado en macacos, nos acercan paulatinamente a dicha posibilidad. Cada vez está más cerca el nacimiento de primates no humanos derivados íntegramente de células troncales pluripotentes embrionarias cultivadas en el laboratorio (el siguiente trabajo que intentarán sin duda llevar a cabo los autores de este estudio), sin necesidad de pasar por la fecundación de un óvulo por un espermatozoide, como ya es posible, desde hace años, en ratones».
Montoliu añade: «Queda por ver cuántos de estos avances llegarán a ser testados en células troncales pluripotentes embrionarias humanas. Y quizás sería lícito también preguntarnos si deberíamos acometer estos experimentos, cómo deberíamos regularlos y con qué fines deberíamos permitir abordarlos«.
Abril 06/2023 (Diario Médico) – Tomado de la Selección Ginecología y Obstetricia – Publicado en ‘Cell Stem Cell’. Copyright 2018 Unidad Editorial Revistas, S.L.U.
may
16
Dos nuevos trabajos del consorcio Atlas Celular Humano dan nueva información sobre los tipos y características de las células inmunitarias que pueden encontrarse en nuestros órganos, desde las etapas de desarrollo hasta la edad adulta. Estas contribuciones ayudarán a comprender y diagnosticar enfermedades. Read more

