ene
27
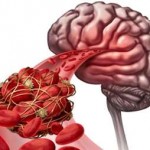 Una investigación de la Universidad de Extremadura (UEx) y el Hospital San Pedro de Alcántara en Cáceres propone un nuevo biomarcador para la prevención y tratamiento del ictus, la proteína STC2, tras revelar que niveles bajos de la misma se asocian a un mayor riesgo de accidente cerebrovascular.
Una investigación de la Universidad de Extremadura (UEx) y el Hospital San Pedro de Alcántara en Cáceres propone un nuevo biomarcador para la prevención y tratamiento del ictus, la proteína STC2, tras revelar que niveles bajos de la misma se asocian a un mayor riesgo de accidente cerebrovascular.
El estudio es fruto de la colaboración entre el departamento de Fisiología de la Facultad de Veterinaria de la UEx y el servicio de Hematología del citado hospital del Servicio Extremeño de Salud (SES).
Plantea que la proteína STC2 desempeña un papel esencial en la regulación de la actividad plaquetaria y, por tanto, en la formación de trombos arteriales.
El hallazgo ha sido publicado recientemente en la revista Journal of Molecular Sciences.
Este abre la puerta a nuevas estrategias para prevenir el ictus, una de las principales causas de muerte y discapacidad en el mundo.
Regulación de la actividad plaquetaria
STC2 es una proteína que participa en la regulación de la entrada del ion calcio en varios tipos de células.
Entre ellas las plaquetas humanas y de ratón, impidiendo el exceso de calcio en la célula.
Cuando la STC2 disminuye, aumenta la entrada de calcio en las plaquetas favoreciendo su agregación y la consiguiente formación de trombos, especialmente en las arterias.
Esto es lo que ocurre en los pacientes diagnosticados de ictus, un tipo de trombosis arterial que afecta a la circulación cerebral.
La investigación sobre el papel de la STC2 aporta un enfoque diferente en el estudio de los mecanismos que contribuyen a la trombosis, centrado en la hiperagregabilidad plaquetaria relacionada con la entrada de calcio en las plaquetas.
La hematóloga Nuria Bermejo, primera autora del estudio, recuerda que la trombosis es una patología multifactorial.
En cada paciente puede pesar más un tipo u otro de causas que la favorezcan. Por ello, añade, «cuanto más amplio sea el panel de factores que caractericemos e identifiquemos, más oportunidades tendremos de prevenir y tratar esta patología».
Trombosis arterial
En la primera de las dos fases de investigación, se realizó un estudio prospectivo no aleatorizado de una cohorte de pacientes de dicho hospital. En concreto, se llevó a cabo el correspondiente estudio de trombofilia, que es una tendencia anormal a desarrollar trombos, tras un episodio de trombosis, venosa o arterial.
Por su parte, el equipo de Pedro Cosme en el Departamento de Fisiología de la UEx, analizó las muestras de sangre de los pacientes.
Los primeros resultados confirmaron la causalidad entre la alteración de expresión de la proteína STC2 y el aumento de la entrada de calcio, tal y como, se había previamente descrito en plaquetas de ratón.
Los investigadores hallaron, por tanto, una relación entre los niveles de STC2 y el riesgo de presentar trombosis arterial.
En una segunda fase posterior, el equipo realizó un seguimiento de los pacientes participantes en el estudio durante más de 10 años.
Se revisaron las historias de los pacientes diagnosticados de ictus y trombosis arterial, y se midieron los parámetros bioquímicos en la UEx.
«Los resultados indicaron valores de STC2 en su mayoría normalizados con respecto a los pacientes sanos gracias al tratamiento con aspirina que regula los niveles de STC2», explica la doctora Bermejo.
Tratamiento preventivo
Tras este primer hallazgo relevante sobre el papel de STC2 en trombosis, se prevé realizar estudios multicéntricos aleatorizados con mayor número de pacientes.
Se incluirán además otras patologías trombóticas como los síndromes coronarios agudos (infarto de miocardio) o crónicos que avalen la proteína STC2 como biomarcador de ictus.
Los investigadores subrayan que el seguimiento regular de la proteína STC2 es un buen candidato de biomarcador de ictus en colectivos ya en riesgo y en la población general, que por edad tiene un mayor riesgo de sufrir trombosis, favoreciendo así el tratamiento preventivo con aspirina.
Además, la detección periódica de STC2 podría ayudar a valorar en qué pacientes el tratamiento con aspirina es efectivo para prevenir el desarrollo de nuevos ictus, concluye el comunicado.
22 enero 2026 | Fuente: EFE | Tomado de | Noticia
ene
26
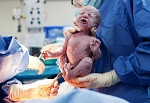 Un estudio liderado por el Hospital Clínic y el Banco de Sangre de Cataluña ha comprobado los beneficios de transfundir sangre de cordón umbilical, donada por una parturienta, a prematuros extremos que sufren anemia, que es una complicación frecuente en estos casos.
Un estudio liderado por el Hospital Clínic y el Banco de Sangre de Cataluña ha comprobado los beneficios de transfundir sangre de cordón umbilical, donada por una parturienta, a prematuros extremos que sufren anemia, que es una complicación frecuente en estos casos.
Son las conclusiones de un ensayo clínico, pionero en España y el segundo en el mundo, en el que se ha estudiado este tipo de transfusión en bebés extremadamente prematuros, nacidos por debajo de las 28 semanas de gestación.
En este tipo de prematuros, que no superan los 1,5 kilos de peso, necesitan a menudo transfusiones de sangre -alrededor de dos tercios de ellos- porque son especialmente vulnerables a sufrir anemia.
Un recurso es administrar sangre de adulto convencional, pero el problema es que es un tipo de hemoglobina distinta a la del prematuro y aporta demasiado oxígeno a los tejidos.
«Algunos órganos como pulmón o la retina pueden tener afectación», ha explicado en rueda de prensa el impulsor del estudio, Miquel Alsina, adjunto del Servicio de Neonatologa del Hospital Clínic.
Siguiendo una experiencia previa en Italia, el Clínic y el Banco de Sangre y Tejidos (BST) impulsaron este ensayo clínico con 41 recién nacidos prematuros extremos con anemia entre los años 2023 y 2025.
Los resultados han demostrado que «es factible y seguro» hacer este tipo de transfusiones en Cataluña, por lo que la voluntad es poder escalarlo a seis centros más de esta comunidad, ha explicado Alsina.
Con la transfusión de sangre de cordón no ocurre lo mismo que con la sangre de adulto convencional, pues se «conserva el perfil sanguíneo de los bebés prematuros», ha señalado Alsina.
En el estudio se comprobó que hubo una disponibilidad del 78,4 % de sangre de cordón umbilical, que debe proceder de una donación de una mujer que acaba de dar a luz.
Recientemente se cumplieron los 30 años de la primera donación de cordón umbilical, cuya función inicialmente era para el tratamiento de leucemias, pero con los años se han ido ampliando las aplicaciones de este tipo de sangre tan especial, en el ámbito de la dermatología, oftalmología, traumatología o ginecología, entre otras.
Las donaciones flaquean
El director del Banco de Sangre y Tejidos, Jesús Fernández, ha explicado que el año pasado no lograron el objetivo de obtener 1 500 donaciones, pues se quedaron en 1 200.
Es una cifra que ha ido descendiendo en los últimos años, pues en 2017 se recibieron más de 4.000 donaciones.
Todo ello a pesar de que se puede hacer en los principales hospitales de Cataluña y no supone ninguna intervención para la parturienta: basta con que lo comunique en el plan de parto.
El caso de Eira
Hace 17 meses, Eira fue una de las beneficiarias de una transfusión de cordón umbilical tras haber nacido a las 23 semanas de gestación, según han explicado este jueves sus madres, Elisabet Rotela y Silvia Buenestado.
«Cuando nos dijeron que había que hacer una cesárea de urgencias se nos paró el mundo; se fueron todas aquellas imágenes idílicas del nacimiento de una hija y pasamos a tener miedo e incertidumbre», ha rememorado Rotela.
Tras 79 días ingresada en la UCI neaonatal del Clínic y transfusiones de cordón umbilical para tratar la anemia, Eira fue dada de alta.
«A día de hoy Eira está grande, tiene 17 meses ya, está muy bien y es imparable; estamos muy agradecidas a esa madre que hizo la donación», ha dicho por su parte Buenestado.
22 enero 2026 | Fuente: EFE | Tomado de | Noticia
ene
5
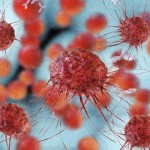 Un método de purificación de sangre afronta su primera prueba como vacuna contra el cáncer, mediante un ensayo clínico que pretende utilizar células tumorales completas inactivadas por luz ultravioleta (UV) como inmunoterapia.
Un método de purificación de sangre afronta su primera prueba como vacuna contra el cáncer, mediante un ensayo clínico que pretende utilizar células tumorales completas inactivadas por luz ultravioleta (UV) como inmunoterapia.
El estudio que comenzará este mes en California modificará células de cáncer de ovario y las devolverá a las pacientes para estimular una respuesta inmunitaria contra los tumores, reflejó la revista Science. En algunas partes del mundo, la sangre donada o sus componentes, como las plaquetas, se desinfectan con UV y riboflavina (vitamina B2) antes de transfundirlas a los pacientes.
Los investigadores buscan utilizar esta técnica, conocida como proceso Mirasol, que puede neutralizar diversos virus, bacterias y parásitos, para combatir el cáncer, inactivar las células tumorales y reintroducirlas en el organismo en busca de desencadenar una respuesta inmunitaria beneficiosa.
El método fue probado en ratones y perros y este mes comenzará un ensayo de fase 1 en pacientes con cáncer de ovario, con la esperanza de que desacelere o prevenga las recaídas en combinación con otras terapias, dijo el químico Ray Goodrich de la Universidad Estatal de Colorado.
Algunos estudiosos están escépticos, pues los intentos de crear vacunas con células cancerosas completas tienen un largo historial de fracasos, alegó Lawrence Fong, inmunólogo y oncólogo del Centro Oncológico Fred Hutchinson.
Ray Goodrich comenzó a trabajar en un método para desinfectar la sangre como estudiante de posgrado a fines de la década de 1980, cuando la contaminación del suministro de sangre por VIH era de gran preocupación.
Tras casi una década, él y sus colegas hallaron como solución mezclar sangre con riboflavina, que se adhiere a las moléculas de ADN y ARN, y luego exponer el líquido a luz ultravioleta, lo cual provoca que la riboflavina reaccione con el material genético de los microbios y lo dañe.
Este método impide que los patógenos se reproduzcan, aunque también daña las plaquetas, los glóbulos rojos y las proteínas del plasma, por lo cual los pacientes pueden requerir transfusiones adicionales.
La idea de una vacuna surgió cuando Goodrich observó que, tras el proceso Mirasol, los glóbulos blancos se inactivaban, pero permanecían intactos.
Los investigadores llevan más de 50 años intentando desarrollar vacunas que contengan células cancerosas completas, pero las formulaciones que llegaron a ensayos clínicos produjeron una respuesta inmunitaria deficiente, y ninguna vacuna fue aprobada para humanos, aunque hay una disponible para mascotas.
El próximo ensayo clínico busca reclutar ocho pacientes con cáncer de ovario en recaída, que serán sometidas a cirugía para extirpar los tumores y luego los científicos expondrán las células tumorales a riboflavina y luz ultravioleta, y las combinarán con un aditivo inmunoestimulante para producir una vacuna personalizada.
Las participantes recibirán tres dosis de vacuna y los expertos evaluarán los efectos secundarios y la respuesta inmunitaria.
02 enero 2026 | Fuente: Prensa Latina | Tomado de | Noticia
jun
19
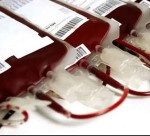 Un reciente informe de la Organización Panamericana de la Salud (OPS) mostró hoy avances en la donación voluntaria de sangre en América Latina y el Caribe, aunque persisten desigualdades y desafíos.
Un reciente informe de la Organización Panamericana de la Salud (OPS) mostró hoy avances en la donación voluntaria de sangre en América Latina y el Caribe, aunque persisten desigualdades y desafíos.
Datos recabados en 2023 indican que 23 países —17 latinoamericanos y seis del Caribe de no habla hispana— recolectaron 9 212 861 unidades de sangre, un aumento de 15,5% respecto a las 7 776 198 de 2020.
Cerca del 80% de las naciones notificaron incrementos significativos gracias a la transición postpandemia y nuevas estrategias de sensibilización.
Según el documento, la región promedia 16 donaciones de sangre por cada 1000 habitantes, pero existen grandes diferencias: 13 países están por debajo de este promedio y 10 lo superan, en tanto Brasil, México, Colombia y Argentina aportan el 75% de las donaciones totales.
Detalla que en 2023 el 56,8% de las unidades recolectadas provino de donantes voluntarios, un aumento de 6,7 puntos porcentuales respecto a 2019, retomando el ritmo de crecimiento previo a la pandemia.
Tal avance es resultado de la realización de campañas digitales, colectas móviles y alianzas con instituciones, aunque los especialistas remarcan que aún está lejos de la meta del 100%.
Mientras, el resto de las donaciones provino de familiares y personas cercanas a los pacientes que respondieron a un llamado.
Ningún país reportó donaciones remuneradas, lo cual refleja un compromiso con la donación altruista. El informe de la OPS destaca también avances en la seguridad y calidad: países reportan que la totalidad de las unidades de sangre donadas fueron sometidas a tamizaje, y el 90% fueron fraccionadas en componentes como glóbulos rojos, plasma y plaquetas, optimizando su uso clínico.
Sin embargo, la gobernanza y organización de los sistemas nacionales y regionales de sangre presentan debilidades, con más de 1 900 centros de colecta y 1 400 de procesamiento que operan de manera dispersa, limitando la eficiencia.
Solo cuatro naciones procesaron un promedio superior a 10 00 unidades anuales, con Paraguay como el más destacado con 20 706.
Las transfusiones de sangre son esenciales para tratar hemorragias en el parto, anemia infantil por desnutrición o malaria, emergencias por desastres, y procedimientos quirúrgicos complejos.
En este contexto, el organismo sanitario insta a los gobiernos a invertir en sistemas nacionales de sangre eficientes, promover la donación voluntaria y fortalecer la vigilancia para garantizar un acceso equitativo y seguro.
12 junio 2025 | Fuente: Prensa Latina | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2025. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
dic
2
 Al celebrarse este domingo el Día Mundial del Sida, la Organización Mundial de la Salud (OMS) exhortó a mandatarios y ciudadanos a defender el derecho a la salud subsanando las desigualdades que entorpecen los progresos hacia el fin de esta enfermedad.
Al celebrarse este domingo el Día Mundial del Sida, la Organización Mundial de la Salud (OMS) exhortó a mandatarios y ciudadanos a defender el derecho a la salud subsanando las desigualdades que entorpecen los progresos hacia el fin de esta enfermedad.
Este año la jornada se desarrolla bajo el lema «Emprendamos la senda de los derechos: Mi salud, mi derecho», con el objetivo de poner fin al sida como amenaza sanitaria para el 2030, informó la OMS.
«A pesar de los enormes progresos realizados en la respuesta al VIH, las violaciones de los derechos humanos siguen impidiendo que el mundo acabe con el sida», afirmó la directora ejecutiva del Programa Conjunto de Naciones Unidas sobre el VIH/sida (Onusida), Winnie Byanyima.
Entre los aspectos que impiden a las personas acceder a los servicios relacionados con el VIH, esenciales para salvar sus vidas y acabar con la pandemia, mencionó la falta de acceso de las niñas a la educación, la impunidad para la violencia de género, y el hecho de que pueden ser detenidas por lo que son o por lo que aman.
Según un nuevo informe de Onusida, de los 39,9 millones de personas que viven con el VIH, 9,3 millones aún no tienen acceso a un tratamiento que podría salvarles la vida.
El año pasado, 630 000 individuos murieron de enfermedades relacionadas con el sida, y 1,3 millones en todo el mundo contrajeron el VIH.
Mostró que en al menos 28 países, el número de nuevas infecciones por VIH va en aumento.
Cada día de 2023, 570 mujeres jóvenes y niñas de entre 15 y 24 años contrajeron el VIH, mientras en unos 22 países de África oriental y meridional, las comprendidas en este grupo de edad tienen tres veces más probabilidades de vivir con esta enfermedad que sus compañeros varones.
El documento resaltó que la criminalización y estigmatización de las comunidades marginadas continúa obstruyendo el acceso a servicios adecuados, y evidenció que en el pasado año 63 países siguen penalizando las relaciones entre personas del mismo sexo.
Onusida subrayó que, aún cuando la ciencia ha avanzado, no llega a todas partes.
Los medicamentos de acción prolongada que sólo necesitan inyectarse un par de veces al año podrían inclinar la balanza, pero sólo si se comparte la tecnología que permita bajar los precios y posibilitar la producción en todas las partes del mundo, precisaron los expertos.
En este contexto, la Organización Panamericana de la Salud (OPS) lanzó la campaña «Mejor con PrEP», dirigida a ampliar el acceso a la Profilaxis Preexposición (PrEP) en América Latina y el Caribe para prevenir el VIH.
También busca aumentar la conciencia sobre este medicamento altamente eficaz para prevenir el VIH cuando se toma de forma consistente.
Aunque esta intervención preventiva está demostrando ser crucial para el control del VIH en la región, su adopción sigue siendo limitada.
A finales del año en curso, 24 de 33 países en América Latina y el Caribe habían adoptado la PrEP como política de salud pública, y aunque más de 160 000 personas ya se benefician de su uso, continúan los esfuerzos para acercarse a la meta de 2,3 millones en la región.
«Hacemos un llamado a todos los países de la región a transformar la realidad del VIH con políticas inclusivas y ampliadas de PrEP. La eliminación del VIH es posible, pero solo si actuamos con valentía y compromiso», afirmó el doctor Jarbas Barbosa, director de la OPS.
El VIH/Sida es una de las más de 30 enfermedades transmisibles y condiciones relacionadas que la OPS busca eliminar para 2030.
01 diciembre 2024|Fuente: Prensa Latina |Tomado de |Noticia
oct
28
 Un estudio dirigido por científicos de la Agencia Internacional para la Investigación sobre el Cáncer (IARC), en colaboración con 17 instituciones asociadas en todo el mundo, ha descubierto marcadores moleculares en la sangre al nacer que están relacionados con el desarrollo posterior de la leucemia linfoblástica aguda (LLA), el tipo de cáncer más común que afecta a los niños.
Un estudio dirigido por científicos de la Agencia Internacional para la Investigación sobre el Cáncer (IARC), en colaboración con 17 instituciones asociadas en todo el mundo, ha descubierto marcadores moleculares en la sangre al nacer que están relacionados con el desarrollo posterior de la leucemia linfoblástica aguda (LLA), el tipo de cáncer más común que afecta a los niños.
Estos marcadores también estaban presentes en los tejidos cancerosos de los niños con leucemia y sirvieron como indicadores de la supervivencia del paciente. Esta investigación ofrece nuevas esperanzas para el diagnóstico temprano y las posibles intervenciones terapéuticas en el cáncer infantil, que es la principal causa de muerte entre las enfermedades en los niños.
El nuevo estudio, publicado en la revista Molecular Cancer, utilizó un enfoque innovador para rastrear los orígenes moleculares del cáncer desde el nacimiento.
Los investigadores perfilaron mapas moleculares en pacientes en varias etapas: nacimiento, diagnóstico, remisión y recurrencia. En el centro de estos mapas se encuentra el epigenoma, que entrelaza intrincadamente las cadenas de ADN en una impronta molecular de la naturaleza y la crianza: lo que nuestros genes proporcionan y cómo el entorno los influye.
Esto permite que el epigenoma capture una instantánea molecular, una especie de diario, de los factores de la vida temprana a los que el bebé estuvo expuesto durante el embarazo. «Este estudio es el resultado de un esfuerzo multidisciplinario a gran escala, una inversión sustancial y una amplia colaboración internacional», señala el doctor Zdenko Herceg, Jefe de la División de Epigenómica y Mecanismos del IARC y coautor principal del estudio.
«Al combinar la epidemiología, la oncología clínica y la ciencia de laboratorio avanzada, hemos obtenido conocimientos únicos sobre las causas del cáncer e identificado biomarcadores que podrían conducir a una detección temprana y una estratificación y terapia de riesgo personalizadas».
Para generar huellas epigenéticas, se requieren muestras biológicas. Sin embargo, la mayor parte de la investigación sobre el cáncer pediátrico se ha basado en muestras clínicas recolectadas después de la aparición de la enfermedad. Esto plantea inquietudes sobre la causalidad inversa, donde los procesos biológicos identificados de esta manera pueden ser resultado del cáncer en lugar de ser su causa.
Para abordar esto, los científicos buscaron marcadores epigenéticos (metilación del ADN) tanto en tejidos sustitutos (sangre) como cancerosos a lo largo del desarrollo de la leucemia, comenzando en el momento del nacimiento mediante el uso de tarjetas de Guthrie archivadas (o sangre del cordón umbilical, cuando esté disponible) de los niños. Las tarjetas de Guthrie albergan manchas de sangre, a menudo se originan a partir de punciones en el talón de los bebés y se recolectan comúnmente como parte de los exámenes de detección neonatal de rutina. Esto descubrió posibles precursores epigenéticos de la leucemia detectables al nacer, antes de que se manifieste la enfermedad.
Después de que se realizó un seguimiento de los pacientes durante más de 10 años, los hallazgos revelaron que las alteraciones específicas de la metilación del ADN al nacer pueden servir como biomarcadores significativos para el desarrollo, el pronóstico y la supervivencia de la LLA. En ausencia de cambios en el código del ADN, los niveles de metilación son potencialmente reversibles, y esto es lo que se observó en los pacientes que respondieron positivamente a la terapia.
Los hallazgos de esta investigación fueron reproducibles con diferentes tecnologías, en tres continentes y en dos etnias, incluida la etnia hispana, a menudo subrepresentada; los niños hispanos tienen las tasas más altas de leucemia infantil en todo el mundo.
«Dado que el cáncer infantil puede tener su origen en el útero, hemos viajado en el tiempo para recolectar muestras de sangre al nacer de niños que luego desarrollaron cáncer», afirma el Dr. Akram Ghantous, científico del IARC y autor principal del estudio. «Estamos trazando un mapa de los ‘diarios’ moleculares de la naturaleza y la crianza en pacientes con cáncer, al tiempo que rastreamos estos diarios hasta el nacimiento; de alguna manera, invertimos la flecha del tiempo para descubrir los orígenes tempranos de la enfermedad», afirma.
Con una mayor validación, estos hallazgos podrían revolucionar la detección temprana y el tratamiento de la leucemia infantil. Las futuras investigaciones se ampliarán a poblaciones más grandes y diversas para descubrir precursores moleculares adicionales de la LLA pediátrica y mejorar las aplicaciones clínicas.
24 octubre 2024|Fuente: Europa Press |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia

