jun
29
 Un reciente estudio sobre longevidad humana, publicado en GeroScience, demostró que aquellas personas con bajos niveles de glucosa, creatinina y ácido úrico llegaron a vivir hasta 100 años.
Un reciente estudio sobre longevidad humana, publicado en GeroScience, demostró que aquellas personas con bajos niveles de glucosa, creatinina y ácido úrico llegaron a vivir hasta 100 años.
Esta investigación tuvo como muestra a 44 000 suecos con edades que oscilaban de 64 a 99 años, sometidos a diferentes estudios médicos.
Durante la investigación, que duró 35 años, se compararon los perfiles de esas personas en la búsqueda de patrones y de las cuales 2,7 % vivió hasta los 100 años y entre ellas 85 % eran mujeres.
Al comparar los perfiles se incluyeron 12 biomarcadores sanguíneos relacionados con la inflamación, el metabolismo, la función hepática y renal, así como con la posible desnutrición y anemia.
Los resultados de los exámenes en la sangre revelaron los individuos con bajos niveles de glucosa, creatinina y ácido úrico llegaron a vivir hasta 100 años.
Cabe destacar que la glucosa es la principal fuente de energía para las células, por lo que su regulación adecuada es crucial para mantener la salud y prevenir enfermedades metabólicas como la diabetes.
Por otro lado, la creatinina y el ácido úrico son desechos que el cuerpo genera, los niveles de la primera son un indicador sobre el funcionamiento de los riñones, mientras el segundo es muestra de la función renal, por lo que el estado normal de ambas sustancias significan un buen proceso metabólico y un estándar saludable.
Cuando se compararon los resultados de las personas investigadas de 90 y 100 años, resultaban equivalentes al promedio de la población joven y saludable.
Aunque no fue posible sacar conclusiones sobre qué factores determinan la esperanza de vida de una persona, es razonable pensar que una dieta balanceada y la actividad física necesaria son variables que regulan el metabolismo y funcionamiento del cuerpo humano.
Si bien, hoy parece común encontrar personas de 70 u 80 años, lo cierto es que es una tendencia reciente, ya que a inicios del siglo XX la esperanza de vida no superaba los 40 años debido a la hambruna, epidemias y guerras.
Ello se debe a que desde mediados del siglo pasado la esperanza de vida ha aumentado 2,5 años por cada década.
27 junio 2024|Fuente: Prensa Latina |Tomado de |Noticia
jun
15
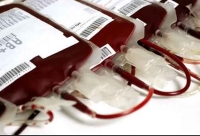 Al celebrarse hoy el Día Mundial del Donante de Sangre, la OPS instó a elevar las cifras de donaciones voluntarias y aumentar la disponibilidad de reservas esenciales de este tejido líquido vital para la salud.
Al celebrarse hoy el Día Mundial del Donante de Sangre, la OPS instó a elevar las cifras de donaciones voluntarias y aumentar la disponibilidad de reservas esenciales de este tejido líquido vital para la salud.
Según los últimos datos disponibles para 34 países de la Región de las Américas, en el año 2020 se alcanzaron los 8,2 millones de unidades de sangre, de las cuales el 48 % provenían de donantes voluntarios, informó el doctor Jarbas Barbosa, director de la Organización Panamericana de la Salud (OPS).
Sin embargo, en numerosos países del área la demanda es mayor que la oferta, y los servicios de sangre enfrentan el reto de que haya suficiente disponibilidad y, al mismo tiempo, de garantizar su calidad y seguridad.
Barbosa indicó que aun cuando las cifras generales de la Región muestran un aumento importante en las donaciones y en la disponibilidad y seguridad de la sangre, la tasa de donación por cada 1 000 personas en los países de ingresos medios y bajos sigue estando entre 50 y 70 % por debajo de las naciones de ingresos más altos.
Tal situación muestra la necesidad de que los países pongan en marcha programas sostenibles, con sistemas y servicios regulados que les permitan disponer de sangre segura en cantidad suficiente para satisfacer las necesidades de los pacientes.
Las donaciones de sangre voluntarias y no remuneradas constituyen la base de un suministro de sangre seguro y suficiente.
Además, desempeñan un papel crucial en el apoyo a pacientes con una amplia gama de problemas crónicos de salud, como la hemofilia y las deficiencias inmunitarias.
Los expertos destacan que las transfusiones de sangre y hemoderivados ayudan a los pacientes a vivir más tiempo y a tener una mejor calidad de vida.
También significan un apoyo en procedimientos médicos y quirúrgicos complejos, por lo que son indispensables en los servicios de atención maternoinfantil y en casos de desastres de origen natural o causados por los seres humanos.
14 junio 2024|Fuente: Prensa Latina |Tomado de |Noticia
jun
8
 Un estudio en el que ha participado el Instituto de Investigación del Hospital del Mar de Barcelona ha descubierto, mediante la manipulación de una proteína, una posible vía para generar células madre de la sangre desde el laboratorio para combatir la leucemia.
Un estudio en el que ha participado el Instituto de Investigación del Hospital del Mar de Barcelona ha descubierto, mediante la manipulación de una proteína, una posible vía para generar células madre de la sangre desde el laboratorio para combatir la leucemia.
En el estudio, publicado en Nature Communications, un grupo de investigadores ha descrito el papel de la proteína IkBa en el proceso de diferenciación de las células madre hematopoyéticas, claves en la producción de sangre.
La diferenciación celular es un proceso por el cual las células madre son capaces de cambiar y transformarse en otros tipos de células, habitualmente más especializadas, que se encuentran en el cuerpo.
Según ha informado este miércoles el Hospital del Mar, la nueva investigación ha determinado que, al faltar IkBa, estas células madre entran en un estado de quiescencia, es decir, se duermen y mantienen su potencialidad para producir otras células con características distintas a las de la original.
El estado de quiescencia puede permitir el trasplante de estas células madre para usos terapéuticos o en enfermedades de la sangre de origen genético.
Así, la investigación abre la puerta a poder generar este tipo de células en el laboratorio, por la vía de inducirles a que no se diferencien ni que se conviertan en otras células antes de tiempo.
El estudio, en el que también ha colaborado el Instituto de Investigación contra la Leucemia Josep Carreras y el Centro de Investigación Biomédica en Red de Cáncer (Ciberonc), se ha llevado a cabo a partir de embriones de ratón que se habían modificado para eliminar esta proteína.
Esto permitió a los investigadores demostrar que el número de células madre hematopoyéticas que se generan en los embriones carentes de IkBa es escaso, aunque mantienen su potencial de célula madre y de convertirse en cualquier célula sanguínea.
Los resultados también han revelado que IkBa reduce los niveles de ácido retinoico, básico a la hora de inducir a las células un estado de quiescencia, es decir, que se mantengan inactivas, sin alterar sus características y sin diferenciarse.
«Al eliminar esta proteína, los niveles de ácido retinoico aumentan y esto permite que las células se duerman. Esto enriquece una población de células que hace la función de célula madre más primitiva, la más conservada, y perdura durante toda su vida», ha explicado la doctora Anna Bigas, de Instituto de Investigación del Hospital del Mar y del Instituto Josep Carreras.
Pese a presentar un número reducido, las células madre hematopoyéticas de los embriones modificados no dejaban de tener su potencial de convertirse en otras células.
Según Bigas, en un futuro se podría evitar que se diferencien las células madre hematopoyéticas «y disponer de ellas para trasplantarlas a un paciente».
En estos momentos, la única fuente viable de este tipo de tratamiento es una donación de células madre de una persona sana y que sea compatible con el enfermo.
En este sentido, este proyecto abre la puerta a avanzar hacia el objetivo de generar células madre hematopoyéticas en el laboratorio, teniendo en cuenta los beneficios de una mayor presencia de ácido retinoico, para que se puedan utilizar en múltiples aplicaciones.
«Estas irían desde trasplante directo de células madre a pacientes de leucemia, hasta al tratamiento con terapia génica de otros trastornos», ha detallado la doctora Bigas, quien ha concluido que el siguiente paso debe ser «que los resultados sean trasladables también a células humanas».
05 junio 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
may
22
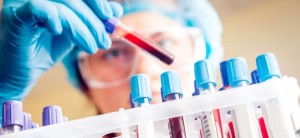 Las autoridades de Reino Unido encubrieron un escándalo asociado a las transfusiones de sangre de 1970 a 1991, causantes del contagio de más de 30 000 personas con VIH y hepatitis, reveló hoy un estudio.
Las autoridades de Reino Unido encubrieron un escándalo asociado a las transfusiones de sangre de 1970 a 1991, causantes del contagio de más de 30 000 personas con VIH y hepatitis, reveló hoy un estudio.
Según el grupo de trabajo de la denominada «Investigación de Sangre Infectada», pesquisa prolongada durante los últimos cinco años, personal médico y Gobierno conocían de esta situación, desde los orígenes del Servicio Nacional de Salud (NHS) en 1948.
No obstante, significó el documento, fallaron a las víctimas en repetidas ocasiones y las expusieron a riesgos inaceptables.
Para el responsable de la investigación, Brian Langstaff, la magnitud de esas conclusiones resulta «horripilante» y subrayó la deliberada intención de «ocultar la verdad».
El texto mencionó entre los riesgos a los que expusieron a miles de personas —3 000 de las cuales ya fallecieron— la repetida importación de productos sanguíneos del extranjero, incluida sangre de donantes estadounidenses de alto riesgo como presos o drogadictos.
Langstaff denunció que ese desastre no fue un accidente, pues médicos, centros de transfusión y gobiernos no dieron prioridad a la seguridad de los pacientes, de ahí la ocurrencia de infecciones y la destrucción de vidas por la negligencia.
Los grupos más afectados, de acuerdo con el estudio, fueron las personas con hemofilia y trastornos en la coagulación, a quienes se les suministró sangre con hepatitis C, y aquellos que recibieron transfusiones tras el parto, accidentes o durante tratamientos médicos.
20 mayo 2024|Fuente: Prensa Latina |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
may
8
 Belice, Jamaica y San Vicente y las Granadinas recibieron hoy, en acto celebrado aquí, la certificación de la Organización Mundial de la Salud (OMS) por haber eliminado la transmisión maternoinfantil del VIH y la sífilis.
Belice, Jamaica y San Vicente y las Granadinas recibieron hoy, en acto celebrado aquí, la certificación de la Organización Mundial de la Salud (OMS) por haber eliminado la transmisión maternoinfantil del VIH y la sífilis.
A nivel mundial, 19 países y territorios han sido certificados por eliminar la transmisión maternoinfantil del VIH y de la sífilis, 11 de ellos ubicados en las Américas.
En 2015, Cuba hizo historia al convertirse en el primer país del mundo en lograr la doble eliminación del VIH y la sífilis congénita, seguido de Anguila, Antigua y Barbuda, Bermudas, Islas Caimán y Montserrat y San Cristóbal y Nevis en 2017, y Dominica en 2020.
En 2010, los países de las Américas se comprometieron a eliminar la transmisión de estas enfermedades y respaldaron la estrategia regional, que fue actualizada en 2016 en el marco del Plan de acción de la Organización Panamericana de la Salud (OPS) para la prevención y el control del VIH y las infecciones de transmisión sexual.
Para cumplir con los objetivos de eliminación, las naciones se centraron en fortalecer los servicios de prevención y tratamiento dentro de la atención primaria de salud y en la salud maternoinfantil, actualizar las guías, garantizar la detección efectiva en las mujeres embarazadas, monitorear los casos y dar seguimiento a los bebés expuestos a esas enfermedades.
En opinión del doctor Jarbas Barbosa, director de la OPS, este logro es un testimonio de años de dedicación, trabajo arduo y colaboración entre gobiernos, profesionales de la salud y comunidades.
Reconoció la resiliencia notable demostrada por los tres países, asegurando la adaptación y continuidad de los servicios esenciales a pesar de los desafíos planteados por la pandemia de covid-19.
Confío en que la celebración de hoy inspirará a otros países a revitalizar sus compromisos hacia una generación libre de VIH y sífilis congénita, destacó.
Por su parte, el director general de la OMS, Tedros Adhanom Ghebreyesus, destacó que si bien la validación es un logro tremendo, mantenerla requiere esfuerzos sostenidos para prevenir nuevas infecciones.
Aseveró que la OMS y sus socios seguirán apoyando a todos los países de las Américas para que fortalezcan los sistemas de salud, presten servicios integrales y garanticen la participación de las mujeres en la planificación y la prestación de servicios.
07 mayo 2024|Fuente: Prensa Latina |Tomado de |Noticia
abr
30
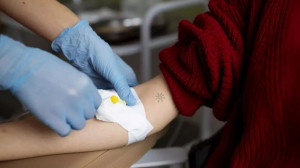 Aunque la terapia celular con CAR-T lleva décadas investigándose, los medicamentos se administran en España desde hace apenas cuatro años, abriendo horizontes para atacar enfermedades como el cáncer, ganar en supervivencia y mejorar la vida del paciente, en un campo todavía incipiente, muy prometedor y en el que aún se afronta una «curva de aprendizaje».
Aunque la terapia celular con CAR-T lleva décadas investigándose, los medicamentos se administran en España desde hace apenas cuatro años, abriendo horizontes para atacar enfermedades como el cáncer, ganar en supervivencia y mejorar la vida del paciente, en un campo todavía incipiente, muy prometedor y en el que aún se afronta una «curva de aprendizaje».
Las terapias avanzadas suponen un gran paso en el sistema sanitario y una «ventana de oportunidad» en patologías y situaciones donde otros tratamientos no llegan. Ese nuevo camino está en la terapia génica, regenerativa o celular, como las CAR-T, explica a EFE la hematóloga del Hospital Universitario Marqués de Valdecilla de Santander, Lucrecia Yáñez.
Estas terapias tienen un gran potencial para desarrollar tratamientos personalizados y representan una perspectiva de revolución en la medicina.
En el otro lado de la balanza está su elevado coste: el tratamiento de cada paciente con CAR-T puede superar los 300 000 euros.
Una de las funciones de nuestro sistema inmunológico es eliminar las células tumorales. Pero esta función se puede perder y desarrollar una formación anormal en alguna parte del cuerpo de tejido en forma de tumor. Ahí entrarían en juego las CAR-T, «un linfocito, modificado genéticamente, que reconoce específicamente a las células que tiene que matar», detalla la doctora Yáñez.
Esta terapia consiste, básicamente, en extraer linfocitos T de la propia persona, modificarlos genéticamente, e introducirlos posteriormente como un medicamento. «Pero primero hay que evaluar al paciente, porque no todos los pacientes van a poder recibir esta terapia», advierte la hematóloga de Valdecilla.
Viaje a Ámsterdam e infusión
El primer paso es la extracción de linfocitos de esa persona, que posteriormente se envían a Ámsterdam, donde se realiza la modificación genética. Esos linfocitos son «la materia prima» con la que se van a desarrollar las células CAR-T para que después vuelvan a infundirse en ese paciente.
El proceso para crear esas células se prolonga dos o tres semanas y, una vez concluido, son necesarios controles. Cuando hay una validación, se devuelven las células criopreservadas y cuando retornan al lugar de origen, donde está el paciente, se le ingresa y se le administra una linfodepleción, que es un tipo de quimioterapia que se aplica para preparar al organismo.
Ya por fin, el CAR-T se descongela y se infunde. »
Durante los primeros días pueden aparecer complicaciones, que son variables dependiendo en parte del paciente y de cómo esté controlada la enfermedad», señala la doctora Yáñez.
Tras los primeros días, y si no aparecen más complicaciones, el paciente es dado de alta y tiene un seguimiento de consulta externa, para monitorizar la enfermedad.
Éste es un procedimiento complejo y que justifica que el Ministerio de Sanidad haya seleccionado para la administración de la terapia CAR-T a centros con gran experiencia en el uso de terapias antitumorales complejas, incluyendo el trasplante de progenitores hematopoyéticos, como es el Hospital Universitario Marqués de Valdecilla de Santander.
Veinte pacientes en dos años
Valdecilla fue designado en junio de 2022 centro infusor de CAR-T, junto a otros trece más dentro de la geografía nacional, en un movimiento del Ministerio que supuso duplicar la red de terapias avanzadas en España.
Yáñez explica que realmente había una necesidad de ampliar esa red, ya que cuando se decidieron los primeros centros en todo el país no se designó ninguno en el norte, «desde Galicia hasta el País Vasco», de forma que los pacientes tenían que trasladarse a Madrid o Barcelona.
El primer paciente al que se infundió terapia CAR-T en Valdecilla fue en agosto de 2022. Hasta hoy ha habido 20 beneficiados de esta terapia y hay dos en espera de que se les administre en las próximas semanas.
De los veinte, además, tres han llegado de otras comunidades autónomas, el País Vasco y La Rioja.
La puesta en marcha y la administración de esta terapia ha requerido el trabajo de un equipo multidisciplinar de profesionales, e involucra al Hospital Marqués de Valdecilla y al Banco de Sangre y Tejidos de Cantabria. «El proceso es muy complejo y se necesita a muchas personas para llevarlo a cabo», destaca la doctora Yáñez.
28 abril 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia

