may
10
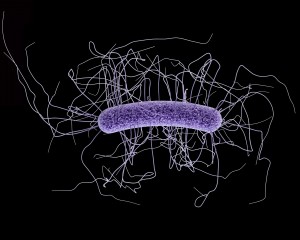
Un equipo de bioquímicos de la Universidad de Notre Dame ha hallado una posible nueva forma de tratar a los pacientes infectados por Clostridium difficile, un tipo de bacteria que causa graves problemas gastrointestinales. En su estudio, publicado en Proceedings of the National Academy of Sciences, el grupo buscó en bases de datos médicas moléculas antibacterianas que pudieran funcionar mejor en pacientes con infecciones por C. difficile.
Las infecciones por C. difficile pueden provocar desde pequeñas molestias hasta episodios potencialmente mortales: cada año mueren unas 13.000 personas. Una vez infectados (muy a menudo mientras están hospitalizados por otra causa), los pacientes suelen recibir un antibiótico para tratar la infección. Desgraciadamente, los antibióticos son cada vez menos eficaces a medida que C. difficile desarrolla resistencias.
Actualmente sólo se utiliza uno: la vancomicina. Otro problema es que C. difficile produce esporas que no son eliminadas por el antibiótico, lo que significa que muchas personas sufren reinfecciones. La vancomicina no funciona bien en estos pacientes, y menos aún en infecciones posteriores. Por estas razones, el equipo de Indiana se propuso encontrar un tratamiento más eficaz para estas infecciones.
El trabajo consistió en buscar en bases de datos antibacterianas moléculas que se sabe que se unen a una proteína específica asociada a C. difficile. Así se llegó a dos compuestos: los oxadiazoles 1 y 2. Las pruebas in vitro demostraron que ambos eran eficaces para eliminar la C. difficile cuando se administraban a la misma dosis que la vancomicina.
A continuación, el equipo comprobó la rapidez con la que se absorbían en el torrente sanguíneo si se administraban por vía oral. El oxadiazol 1 se absorbía con rapidez, lo que lo hacía inadecuado para combatir las bacterias intestinales. En cambio, el oxadiazol 2 se absorbía lentamente, lo que lo convertía en el candidato ideal para una nueva terapia contra las infecciones por C. difficile. En ratones, previno la muerte un 30% mejor que la vancomicina.
El estudio también descubrió que el oxadiazol 2 ayudaba a prevenir la pérdida de peso mejor que la vancomicina. Y lo mejor de todo es que las pruebas fecales no mostraron indicios de esporas: tras tres semanas de pruebas, ninguno de los ratones presentaba reinfecciones.
Mayo 10/2023 (MedicalXpress) – Tomado de Medications – Gastroenterology Copyright Medical Xpress 2011 – 2023 powered by Science X Network.
Traducción realizada con la versión gratuita del traductor www.DeepL.com/Translator
abr
25
La bacteria Clostridioides difficile es un patógeno oportunista que, sobre todo en individuos vulnerables, aprovecha cualquier alteración en la microbiota intestinal para hacerse fuerte y proliferar. La infección por este microbio puede provocar inflamación y un tipo grave de diarrea difícil de combatir que es capaz de ocasionar la muerte del paciente.
Existen diferentes estrategias para combatir esta infección, aunque la más efectiva podría ser el trasplante de heces, a juzgar por una revisión de estudios que publica esta semana Cochrane Review.
Según este análisis, que repasó los datos de seis ensayos clínicos en los que participaron 320 adultos, este abordaje que ya es una realidad en los hospitales españoles es más efectivo que el tratamiento con antibióticos para el control de C.difficile.
En concreto, el trabajo puso de manifiesto que el 77% de los pacientes que recibieron un trasplante de microbiota intestinal no experimentó ninguna reinfección en un periodo de ocho semanas, un porcentaje que se redujo al 40% en el grupo que solo recibió antibióticos.
Una de las principales causas de infección por C.difficile es la disbiosis intestinal, un trastorno que se produce cuando las bacterias ‘buenas’ que habitualmente colonizan nuestro intestino pierden presencia y poder. Esta pérdida puede producirse, por ejemplo, por el consumo de antibióticos.
La bacteria aprovecha esa circunstancia para colonizar el intestino y empezar a destruirlo, lo que provoca una diarrea que puede ir acompañada de dolor tipo cólico, fiebre, vómitos, deshidratación y puede llegar a provocar la muerte. Las personas más afectadas por este problema son aquellas de edad avanzada, que se encuentran ingresadas en un hospital y con varios problemas de salud, aunque puede darse también en colectivos no vulnerables.
El tratamiento estándar de la infección incluye la prescripción de antibióticos, si bien esta indicación en ocasiones puede exacerbar la disbiosis, contribuyendo a crear un círculo vicioso.
¿Qué es el trasplante fecal?
El trasplante fecal ha ido ganando terreno como alternativa para reestablecer una microbiota saludable y combatir la acción de la bacteria patógena. El objetivo del trasplante es utilizar la microbiota saludable de un donante para recolonizar el intestino del paciente afectado y restablecer el balance entre los microorganismos que viven habitualmente en el intestino. El procedimiento puede realizarse por diferentes vías: mediante cápsulas preparadas que se toman por vía oral, a través de un enema o con infusión de preparaciones líquidas también por vía rectal, entre otras.
Además de una mayor efectividad para controlar la infección, la revisión de estudios también mostró la existencia de menos efectos secundarios en el trasplante fecal en comparación con la terapia estándar con antibióticos.
Una segunda revisión publicada en Cochrane esta semana también ha analizado la utilidad del trasplante de heces frente a otros trastornos: las enfermedades inflamatorias intestinales, entre las que figuran problemas como la colitis ulcerosa o la enfermedad de Crohn. Los datos de este trabajo también mostraron resultados prometedores frente a la colitis, si bien el trabajo señala que las conclusiones no son lo suficientemente robustas. En el caso de la enfermedad de Crohn es necesario tener más datos antes de saber si la estrategia puede ser efectiva.
Abril 25/2023 (Diario Médico) - Tomado de Aparato Digestivo – Publicación Copyright Junio 2018 Unidad Editorial Revistas, S.L.U.
abr
18
Eli Lilly and Company ha anunciado que el Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea del Medicamentos (EMA) ha emitido una opinión positiva para el uso de mirikizumab en pacientes adultos con colitis ulcerosa (CU) activa de moderada a grave que hayan tenido respuesta inadecuada, pérdida de respuesta o fueran intolerantes a la terapia convencional o a un tratamiento biológico.
Este dictamen marca el primer paso hacia la aprobación reglamentaria europea de mirikizumab, cuya información se remite ahora a la Comisión Europea para la decisión definitiva. Una vez aprobado, este fármaco será el primer antagonista de la interleucina-23p19 (IL-23p19) autorizado para el tratamiento de la CU activa de moderada a grave en la Unión Europea. Se espera que la decisión de la Comisión Europea llegue en los próximos dos meses.
«Los objetivos terapéuticos en la colitis ulcerosa están avanzando en los últimos años y en muchos casos no consiguen alcanzarse con los fármacos actuales o se pierde su eficacia con el tiempo», afirma la Dra. María Dolores Martín Arranz, jefa de Servicio de Digestivo del Hospital Universitario La Paz. En este contexto, «la aparición de moléculas con nuevos mecanismos de acción, más selectivas y seguras, añade oportunidades para mejorar la calidad de vida de nuestros pacientes, incluso en pacientes con otras enfermedades inmunomedidadas concomitantes», añade esta experta.
La opinión positiva se basó en los resultados del programa LUCENT, que incluía dos ensayos clínicos de fase 3 aleatorizados, doble ciego y controlados con placebo: el LUCENT-1, un estudio de inducción de 12 semanas de duración, y LUCENT-2, un estudio de mantenimiento de 40 semanas, constando en total un seguimiento de 52 semanas.
En el estudio de inducción LUCENT-1 se incluyeron 1.162 pacientes en la población de eficacia primaria. Los pacientes fueron aleatorizados para recibir mirikizumab 3:1 (300 mg) por vía intravenosa (IV) o placebo IV cada 4 semanas durante 12 semanas. Tras 12 semanas de tratamiento con mirikizumab, el 24.2% (n=210/868) de los pacientes alcanzaron el objetivo primario de remisión clínica, frente al 13.3% (n=39/294) que recibió placebo.
Los pacientes que lograron una respuesta clínica (63.5%, n=551/868) con mirikizumab en el estudio LUCENT-1 fueron re-aleatorizados 2:1 para recibir inyección subcutánea de mirikizumab (200 mg) o inyección subcutánea de placebo cada 4 semanas durante otras 40 semanas en el estudio LUCENT-2. De los pacientes de LUCENT-1 que lograron una respuesta clínica a las 12 semanas, el 49,9% (n=182/365) alcanzaron la remisión clínica, y el 43,3% (n=158/365) la remisión histológica-endoscópica mucosa al año, en comparación con placebo (25,1%, n=45/179 y 21,8%, n=39/179 para la remisión clínica y la remisión histológica-endoscópica mucosa, respectivamente).
Así mismo, los pacientes tratados con mirikizumab lograron una mayor reducción del sangrado rectal y de la frecuencia de deposiciones ya a las dos semanas del tratamiento. En los estudios LUCENT también se tuvieron en cuenta nuevos criterios de valoración, como la remisión y la gravedad de la urgencia intestinal, medida con la Escala de Calificación Numérica de la Urgencia (NRS) de 0-10 centrada en el paciente, siendo cero la ausencia de urgencia y 10 la peor urgencia posible. Así, en los pacientes tratados con mirikizumab se observó una reducción en la gravedad de la urgencia intestinal ya a las dos semanas de estudio. Tras el tratamiento con mirikizumab, el 42,9% (n=144/336) de los pacientes lograron la remisión de la urgencia intestinal al año, frente al 25% (n=43/172) de los tratados con placebo.
El programa de ensayos clínicos de fase 3 LUCENT también evaluó el perfil de seguridad de mirikizumab. Pocos pacientes interrumpieron el tratamiento debido a acontecimientos adversos, y la mayoría de los acontecimientos adversos emergentes fueron de leves a moderados. Las reacciones adversas notificadas con mayor frecuencia fueron infecciones de las vías respiratorias superiores, cefalea, artralgia, erupción cutánea y reacciones en el lugar de inyección.
«Mirikizumab puede convertirse en el primer y único antagonista de la IL-23p19 autorizado a nivel europeo para la colitis ulcerosa. El desarrollo clínico de este nuevo fármaco pone de manifiesto el continuo foco de Lilly para generar innovación relevante que contribuya a mejorar la salud de los pacientes, incidiendo en el tratamiento de los síntomas que más afectan a su calidad de vida», afirmó José Antonio Sacristán, director médico de Lilly España. «La opinión positiva del CHMP representa un hito importante en el tratamiento de la colitis ulcerosa en la Unión Europea, y pone de manifiesto el compromiso de Lilly de seguir aportando opciones terapéuticas innovadoras en el área de las enfermedades autoinmunes», concluye.
Abril 17/2023 (IMmedico) – Tomado de Farmacia Hospitalaria y Gastroenterología Digestivo. Copyright 2023: Publimas Digital.
abr
12
Un equipo internacional de investigadores ubicados en el Centro RIKEN de Ciencias Médicas Integrativas (IMS) en Japón descubrió que las personas que portan ciertos factores de riesgo genéticos para el cáncer gástrico tienen un riesgo más elevado de desarrollar esta enfermedad si también han sido infectadas por la bacteria Helicobacter pylori. El hallazgo, publicado en The New England Journal of Medicine, podría contribuir al desarrollo de una medicina genómica adaptada para tratar específicamente este tumor, según los autores.
El cáncer de estómago es la cuarta causa principal de muerte por cáncer en todo el mundo y en su potencial desarrollo influyen factores de riesgo tanto ambientales como genéticos. Ambientalmente, la infección por H. pylori aumenta el riesgo de cáncer de estómago. Debido a que la presencia de H. pylori en el este de Asia es alta, la incidencia de cáncer de estómago es mayor en países como Japón, por ejemplo.
Estudio en población japonesa
Desde el punto de vista genético, se conoce que ciertas variantes están asociadas con el riesgo de enfermedad. Así, por ejemplo, las personas que portan una determinada variante patógena hereditaria del gen CDH1 tienen un mayor riesgo de cáncer gástrico.
La prueba de la presencia de variantes patogénicas es ahora otra de las distintas medidas que se están tomando para la prevención, vigilancia y selección del tratamiento del cáncer. Sin embargo, todavía faltan estudios de casos y controles a gran escala. Además, los datos de los que se han realizado no han evaluado todavía cómo cambia el riesgo de cáncer de estómago cuando las variantes patogénicas interactúan con factores ambientales como H. pylori. Por tanto, tampoco está claro qué medidas clínicas reales podrían llevarse a cabo.
Para abordar este problema, el equipo de investigación analizó el riesgo de cáncer gástrico en un estudio a gran escala de casos y controles en población japonesa, considerando si eran portadores de variantes patogénicas y si habían sido infectados por H. pylori.
Usando un método para el análisis genómico desarrollado originalmente en RIKEN, el equipo conjunto dirigido por Yukihide Momozawa, del Laboratorio de Desarrollo de Genotipado de RIKEN IMS y Keitaro Matsuo, de la División de Epidemiología y Prevención del Cáncer del Centro del Cáncer Aichi, en Japón, analizó muestras de ADN de más de 11.000 pacientes con cáncer de estómago y 44. 000 personas sin cáncer para 27 genes asociados con herencia tumores Su análisis identificó nueve genes que estaban altamente asociados con el riesgo de cáncer de estómago. Después, se estudió la interacción entre las variantes patogénicas en los nueve genes y el historial de infección por H. pylori de cada paciente.
El primer hallazgo fue que el riesgo de cáncer gástrico era significativamente mayor cuando una variante patogénica se combinaba con una infección por H. pylori que cuando cualquiera de los factores estaba presente solo. De los nueve genes en los que se centraron el estudio, cuatro fueron de particular interés porque codifican proteínas que normalmente ayudan a reparar el ADN dañado.
Yoshiaki Usui, coordinador de la investigación, considera que estas variantes patogénicas exacerban el daño causado por la infección por H. pylori. «La infección por esta bacteria conduce al desarrollo tumoral porque promueve la ruptura de la doble cadena del ADN y desestabiliza el ADN de las células del estómago. La combinación de este fenómeno con la presencia de variantes genéticas que impiden la reparación normal del daño parece aumentar sustancialmente el riesgo de cáncer gástrico».
Dado que la prevalencia de la infección por H. pylori es elevada y su erradicación ha resultado difícil, la detección de variantes patogénicas puede ayudar a determinar a quién se debe dar prioridad para las intervenciones. En general, reducir el riesgo de cáncer de estómago mediante la prueba de infección por H. pylori y erradicarla sigue siendo una alta prioridad para el colectivo médico, independientemente de si son portadores de las variantes patogénicas.
Prevención y erradicación
«Para la práctica clínica, tendremos que determinar hasta qué punto la erradicación de H. pylori tiene realmente un efecto preventivo o cuándo se debe considerar la erradicación», señala Matsuo.
Para este profesional, la información obtenida contribuirá a la renovación de las pautas de la práctica médica sobre el cáncer gástrico y las variantes patogénicas. «Se espera que contribuya a establecer un sistema de medicina genómica a la medida, que incluya una mejor precisión diagnóstica, el desarrollo de terapias dirigidas a los genes causantes y los métodos y medidas preventivas más apropiadas para reducir los casos de cáncer gástrico», dice Momozawa.
Abril 12/2023 (Diario Médico) – Tomado de la Selección de Oncología. Copyright 2018 Unidad Editorial Revistas, S.L.U.
mar
3
Aunque bajo control, el cólera, sin embargo, puede retornar a África en condiciones muy precarias para enfrentarla, advirtió la Organización Mundial de la Salud (OMS) en un comunicado circulado aquí. Read more
feb
27
Uno de los tipos de quimioterapia que sirve para tratar el cáncer de colon y recto avanzado, la quimioterapia basada en el platino, se acumula en las células sanas que rodean las células cancerosas, y, como consecuencia, puede hacer disminuir la sensibilidad del cáncer en el tratamiento. Read more