nov
14
Los tratamientos, especialmente la radioterapia, provocan deficiencias cognitivas a largo plazo en supervivientes de oligodendrogliomas, lo que señala la necesidad de revisar las terapias.
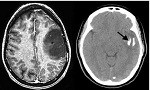 El oligodendroglioma es uno de los pocos tumores cerebrales en los que los tratamientos actuales consiguen prolongadas y significativas tasas de supervivencia. El tratamiento actual consiste en cirugía y radioterapia sobre el cerebro, junto con esquemas de quimioterapia. Sin embargo, se desconocen con exactitud sus posibles efectos tóxicos a medio y largo plazo, especialmente en la esfera de la cognición. Sin embargo, un nuevo estudio publicado en Neuro-Oncology, coordinado por Jordi Bruna y Marta Simó, del Instituto de Investigación Biomédica de Bellvitge y profesionales de la Unidad de Neuro-oncología del Hospital Universitario de Bellvitge
El oligodendroglioma es uno de los pocos tumores cerebrales en los que los tratamientos actuales consiguen prolongadas y significativas tasas de supervivencia. El tratamiento actual consiste en cirugía y radioterapia sobre el cerebro, junto con esquemas de quimioterapia. Sin embargo, se desconocen con exactitud sus posibles efectos tóxicos a medio y largo plazo, especialmente en la esfera de la cognición. Sin embargo, un nuevo estudio publicado en Neuro-Oncology, coordinado por Jordi Bruna y Marta Simó, del Instituto de Investigación Biomédica de Bellvitge y profesionales de la Unidad de Neuro-oncología del Hospital Universitario de Bellvitge
Instituto Catalán de Oncología, ha supuesto un gran avance en el conocimiento de estos efectos del tratamiento oncológico en los pacientes.
Para Bruna, este estudio es pionero en varios aspectos. En primer lugar, no se trata de un análisis de factores pronóstico, sino que establece una relación causal directa, sospechada pero no clara y directamente demostrada hasta este momento. Supera además las debilidades que presentaban los estudios previos relacionados. Según explica, se centra en una población concreta y bien delimitada de pacientes con un tumor cerebral específico, que reciben tratamientos relativamente homogéneos, incluyendo a un número suficiente de ellos para obtener conclusiones sólidas. Estos factores permiten controlar las variables confusoras que presentaban anteriores publicaciones. Por último, y más novedoso, combina por un lado las exploraciones más clásicas de las funciones neuropsicológicas con técnicas avanzadas de análisis de neuroimagen cerebral, permitiéndonos obtener datos tanto funcionales como estructurales de forma detallada y precisa.
Toxicidad cognitiva tardía
Las conclusiones muestran que los pacientes con tumores oligodendrogliales de grado II y III, según la clasificación de la Organización Mundial de la Salud (OMS), presentan, después de más de 5 años de la finalización del tratamiento, un deterioro cognitivo que se considera grave en hasta el 38 % de los afectados. Esta toxicidad cognitiva tardía se asocia principalmente con atrofia cerebral y daño en la sustancia blanca cerebral.
Actualmente, el tratamiento estándar de los pacientes de tumor oligodendroglial incluye la quimioterapia (procarbazina, lomustina y vincristina) y la radioterapia craneal, una combinación que mejora significativamente la supervivencia general y la supervivencia libre de progresión de oligodendrogliomas de grado II y III. Específicamente, la tasa de supervivencia general a 10 años con el tratamiento estándar es de casi el 80 % para los oligodendrogliomas de grado II y del 60 % para los de grado III, una cifra nunca antes observada en los gliomas malignos.
Impacto de la terapia oncológica
Por lo tanto, el impacto de los efectos a largo plazo del tratamiento oncológico en pacientes con tumor oligodendroglial se ha vuelto un aspecto cada vez más relevante, especialmente por lo que hace referencia al funcionamiento cognitivo. Bruna matiza que en el caso de un paciente con un tumor activo, su deterioro puede ser debido a dos causas: la progresión del tumor o a los tratamientos administrados, por lo que, y para evitar este factor de confusión, se eligió a pacientes sin evidencia de enfermedad activa. Por tanto, y claramente, las conclusiones se dirigen a los tratamientos administrados.
Los principales déficits cognitivos y cambios estructurales del cerebro en una serie de sobrevivientes a largo plazo de tumores oligodendrogliales de grado II y III se observaron especialmente en funciones de memoria y ejecutivas, asociado con un daño tardío de la sustancia gris y la sustancia blanca.
¿Hay que revisar los tratamientos?
Los datos del grupo del Idibell evidencian, por primera vez, la necesidad de desarrollar nuevas estrategias de tratamiento para los pacientes con tumores oligodendrogliales de los cuales se espera una larga supervivencia, aunque cualquier modificación de un esquema terapéutico, requiere comprobación mediante el perceptivo ensayo clínico prospectivo, randomizado, sobre su eficacia respecto a la rama estándar aceptada hasta el momento. Al menos utilizando un diseño de no inferioridad, señala Bruna.
El investigador especifica que sobre la pauta de citostáticos existe actualmente controversia, ya que podría potencialmente plantearse un cambio. De hecho, en la mayoría de centros de Estados Unidos y Latinoamérica, en vez de administrarse procarbazina, lomustina y vincristina (PCV) se utiliza la temozolamida. Pero su justificación está basada en una aproximación teórica sobre sus mecanismos de acción, la experiencia y comodidad de su administración, y en estudios que aportan unos niveles de evidencia muy limitada en comparación a la clase 1 del ensayo que demostró la eficacia del PCV.
Sin embargo, y según los investigadores, este no sería el principal problema o el punto donde realizar modificaciones que puedan revertir en mejores resultados cognitivos para los pacientes. Aunque por el diseño de nuestro estudio no se pueden excluir potenciales efectos de chemobrain añadidos, el principal responsable del deterioro progresivo en el tiempo es la radioterapia sobre el cerebro. Por lo que si se hubiese de testar una modificación del esquema terapéutico actual para minimizar efectos adversos, se tendría que comprobar es si este tumor es suficientemente quimio sensible para evitar la administración de radioterapia. Es decir, si PCV sin radioterapia, presenta supervivencias similares al régimen actual, radioterapia seguida de PCV. Otra posibilidad sería permitir la radioterapia de rescate si se progresase en la rama de PCV en monoterapia, y de este modo al menos retardar la aparición del deterioro cognitivo, aproximación aceptable siempre que las supervivencias fueran similares.
Por otro lado, el abordaje mediante rehabilitación cognitiva, al igual que el ejercicio físico, ha demostrado ser positivo para mejorar las funciones cognitivas de los pacientes con tumores cerebrales una vez producido el daño, pero aún no ha demostrado ningún efecto neuroprotector, es decir de prevención de este. Y a pesar de tener efectos positivos, y por tanto recomendables en toda clase de pacientes con tumores cerebrales tratados, su impacto es limitado y no devuelve al paciente a su estado basal. Por tanto, lo más recomendable sería testar modificaciones del tratamiento actual, como la comentada de limitar la administración de radioterapia o bien, utilizar nuevas técnicas de radioterapia que limitasen la exposición del tejido sano cerebral a la radiación.
noviembre 13/2019 (Diario Médico)

