oct
8
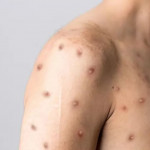 La Organización Mundial de la Salud (OMS) ha incluido el ensayo ‘Alinity m MPXV’, de Abbott Molecular, como primer diagnóstico in vitro (IVD) de mpox en su procedimiento de Listado de Uso de Emergencia (EUL, por sus siglas en inglés), un paso importante para mejorar el acceso global a las pruebas de viruela símica (mpox).
La Organización Mundial de la Salud (OMS) ha incluido el ensayo ‘Alinity m MPXV’, de Abbott Molecular, como primer diagnóstico in vitro (IVD) de mpox en su procedimiento de Listado de Uso de Emergencia (EUL, por sus siglas en inglés), un paso importante para mejorar el acceso global a las pruebas de viruela símica (mpox).
La aprobación para el uso de emergencia de esta prueba permitirá ampliar la capacidad de diagnóstico en países que enfrentan brotes de mpox, donde la necesidad de pruebas rápidas y precisas ha aumentado drásticamente. El diagnóstico temprano de mpox permite el tratamiento y la atención oportunos, así como el control del virus.
De ello podrán beneficiarse los países africanos donde, según la OMS, persisten la capacidad limitada para realizar pruebas y las demoras en confirmar los casos de mpox, lo que contribuye a la propagación continua del virus. En 2024, se han notificado más de 30 000 casos sospechosos en toda la región, con las cifras más altas en la República Democrática del Congo, Burundi y Nigeria. Además, la OMS ha señalado que en la República Democrática del Congo solo se han realizado pruebas al 37 % de los casos sospechosos este año.
La presencia del virus de la viruela del simio se confirma mediante pruebas de amplificación de ácidos nucleicos (NAAT), como la reacción en cadena de la polimerasa (PCR) convencional o en tiempo real, como se indica en la Guía provisional de la OMS sobre pruebas diagnósticas para el virus de la viruela del simio (MPXV, por sus siglas en inglés). El tipo de muestra recomendado para la confirmación diagnóstica de la infección por MPXV en casos sospechosos es el material de la lesión.
El ensayo ‘Alinity m MPXV’ es una prueba de PCR en tiempo real que permite la detección del ADN del virus de mpox (clado I/II) en muestras de lesiones cutáneas humanas. Está diseñado específicamente para que lo utilice personal de laboratorio clínico capacitado que sea competente en técnicas de PCR y procedimientos de diagnóstico in vitro. Al detectar el ADN de muestras de erupciones pustulosas o vesiculares, los trabajadores de laboratorio y de la salud pueden confirmar casos sospechosos de mpox de manera eficiente y eficaz.
«Esta primera prueba diagnóstica mpox incluida en el procedimiento de Listado de Uso en Emergencias representa un hito importante en la ampliación de la disponibilidad de pruebas en los países afectados», ha resaltado la subdirectora general de la OMS para el Acceso a Medicamentos y Productos Sanitarios, Yukiko Nakatani.
Hasta el momento, la OMS ha recibido tres solicitudes adicionales para su evaluación en el marco de la autorización de uso de sustancias y se están llevando a cabo conversaciones con otros fabricantes de dispositivos de diagnóstico ‘in vitro’ de mpox para garantizar una gama más amplia de opciones de diagnóstico de calidad garantizada. Esto ayudará a los países que no han aprobado los productos médicos a través de sus propios procesos de aprobación a adquirir las pruebas que se necesitan de manera crítica a través de organismos de las Naciones Unidas y otros socios.
04 octubre 2024|Fuente: Europa Press |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia