dic
9
 El nuevo premio nobel de Medicina Drew Weissman, cuyas investigaciones están en la base de la tecnología que hizo posibles las vacunas contra la covid-19, cree que aún hay margen de mejora y está trabajando para conseguir una inmunización universal frente a los coronavirus.
El nuevo premio nobel de Medicina Drew Weissman, cuyas investigaciones están en la base de la tecnología que hizo posibles las vacunas contra la covid-19, cree que aún hay margen de mejora y está trabajando para conseguir una inmunización universal frente a los coronavirus.
El inmunólogo estadounidense ha merecido este año el galardón junto a la bioquímica húngara Katalin Karikó por crear la tecnología que permite usar ARN mensajero como agente terapéutico, premio que recogerán junto al resto de galardonados el próximo domingo. Esa investigación fue crucial para desarrollar las primeras vacunas de la pandemia, salvando millones de vidas y previniendo enfermedades graves en muchas más, según dijo, al dar a conocer el premio, el Instituto Karolinska, encargado de otorgar este nobel.
Weissman (1959) señaló a EFE que aún hay margen para mejorar las vacunas basadas en ARN mensajero para la covid-19, un virus que muta de forma similar a la gripe, lo que supone que cada año haya que hacer nuevas vacunas pues el virus ya no es bloqueado por la del año anterior. Sin embargo, el nuevo nobel ya está trabajando, tanto en su laboratorio de la Facultad de Medicina de la Universidad de Pensilvania (EE.UU), como con un grupo internacional, en una vacuna ‘pancoronavirus’ o universal, ‘que protegerá contra todos’.
Dicha inmunización, que ‘tal vez sirva para cinco años, pero eso no lo sabemos aún’, evitará cualquier nuevo coronavirus, incluso los que puedan pasar a personas, procedentes por ejemplo de murciélagos, y cualquiera de las variantes del actual covid-19. El candidato vacunal se dirige a la fase de ensayos clínicos (con personas), pues hay uno que empezará en Tailandia, ‘probablemente dentro de seis u ocho meses’ y también trabaja en otro, de inicio ‘probablemente dentro de un año’, en colaboración con la Universidad de Duke (EE.UU).
El centro de las investigaciones de Weissman y Karikó es el ARN mensajero (ARNm) o ácido ribonucleico mensajero, un tipo de molécula que transporta la información genética necesaria de una parte de la célula a otra para fabricar las proteínas que nos permiten vivir. Ambos científicos, en aquella época en la Universidad de Pensilvania, descubrieron cómo modificar las moléculas de ARN para usarlas como agente terapéutico sin que el sistema inmune humano las destruyera e idearon un sistema para ponerlo en nanopartículas, lo que evita su rápida degradación.
Aunque durante la pandemia, esta tecnología se convirtió en base para el rápido desarrollo de vacunas, su potencial es muy grande en las más distintas áreas de la medicina, y Weissman estimó que ‘los principales cambios se producirán en los próximos 10 o 20 años’. En la actualidad -dijo- su equipo tiene siete vacunas en fase uno de ensayos clínicos para prevenir, entre otros, los norovirus (que causan vómitos y diarreas) o bacterias como ‘Clostridioides difficile’, que provoca infección en el intestino grueso, sin olvidar una universal para la gripe.
Además, ha creado un programa de terapia génica contra la malaria, que espera poder empezar a administrar en los próximos dos años, entre otras ‘muchas terapias en desarrollo’. Weissman lleva años investigando una vacuna para el VIH, de hecho ese era su objetivo principal cuando en 1997 conoció de forma casual, en una fotocopiadora de la Universidad, a Karikó. Ella ya investigaba en ARN-mensajero y allí comenzaría una estrecha colaboración de más de dos décadas.
Entre los proyectos de vacunas que está investigando el laboratorio de Weissman hay ‘un par’ dirigidas al VIH, que ‘probablemente tardarán entre cinco y siete años’ en llegar a fase tres (la última) de los ensayos clínicos. Además, destacó un programa de curación de la enfermedad, que ya prueba en modelos de macacos y ‘en seis meses sabremos si funciona’ si ese fuera el caso el próximo paso sería la prueba con pacientes.
El futuro del ARN-mensajero es muy prometedor, pero en el inicio de las investigaciones su potencial contó con poca atención de otros científicos. Sin embargo lo hoy nuevos nobeles siempre lo tuvieron claro. ‘Hace 25 años, Katie y yo enumerábamos todo lo que podía hacer el ARN-mensajero, pero bromeábamos diciendo que probablemente moriríamos antes de que este dejara huella en el mundo. Sin embargo, hemos sobrevivido hasta ahora’, dijo.
9 diciembre 2023|Fuente: EFE| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
dic
8
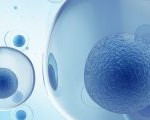 Un equipo internacional de científicos ha descubierto por primera vez cómo se organizan las células de un embrión para formar las extremidades humanas, lo que ayudará en el futuro a diagnosticar y a tratar las enfermedades congénitas asociadas a las mismas.
Un equipo internacional de científicos ha descubierto por primera vez cómo se organizan las células de un embrión para formar las extremidades humanas, lo que ayudará en el futuro a diagnosticar y a tratar las enfermedades congénitas asociadas a las mismas.
El hallazgo, que publica este miércoles la revista Nature, ha sido posible gracias a la aplicación de tecnologías celulares de vanguardia para crear un atlas que caracteriza el mapa celular de las extremidades humanas desde que empiezan a formarse. De este modo, los investigadores han visto cómo las extremidades se crean en una fase inicial como una especie de bolsas celulares indiferenciadas a los lados del cuerpo, sin una forma o función específicas.
Es a las ocho semanas de desarrollo cuando empiezan a estar bien diferenciadas, son anatómicamente complejas e inmediatamente reconocibles como extremidades, con dedos en las manos y en los pies. Este proceso requiere ‘una orquestación muy rápida y precisa de las células’, subraya el estudio, ya que cualquier pequeña alteración durante este proceso puede tener un efecto secundario, razón por la cual las variaciones en las extremidades se encuentran entre los síndromes más frecuentes al nacer, afectando aproximadamente a uno de cada 500 bebés en todo el mundo.
Para llegar a esta conclusión, los investigadores analizaron tejidos humanos de entre 5 y 9 semanas de desarrollo, lo que les permitió rastrear programas específicos de expresión génica, activados en determinados momentos y zonas, que dan forma a las extremidades en formación. Como parte del estudio, los investigadores demostraron que hay patrones genéticos con implicaciones en la formación de las manos y los pies, identificando ciertos genes que, cuando se alteran, se asocian a síndromes específicos de las extremidades como la braquidactilia -dedos cortos- y la polisindactilia -dedos de más o de menos-.
El equipo también pudo confirmar que muchos aspectos del desarrollo de las extremidades son comunes a humanos y ratones. En conjunto, estos hallazgos no solo proporcionan una caracterización en profundidad del desarrollo de las extremidades en humanos, sino que también aportan datos fundamentales que podrían influir en el diagnóstico y tratamiento de los síndromes congénitos de las extremidades. ‘Lo que revelamos es un proceso muy complejo y regulado con precisión. Es como ver trabajar a un escultor que va cincelando un bloque de mármol hasta revelar una obra maestra. En este caso, la naturaleza es la escultora, y el resultado es la increíble complejidad de nuestros dedos’, ha señalado uno de los autores, Hongbo Zhang, investigador de la Universidad Sun Yat-sen de Guangzhou en un comunicado.
Este estudio forma parte de la iniciativa internacional Atlas Celular Humano, cuyo objetivo es cartografiar todos los tipos celulares del cuerpo humano para transformar la comprensión de la salud y la enfermedad, y ha sido llevado a cabo por investigadores del Instituto Wellcome Sanger, el Instituto Europeo de Bioinformática (ambos en el Reino Unido), la Universidad Sun Yat-sen (China), además de colaboradores de otros centros. ‘Nuestro trabajo en el Atlas Celular Humano está profundizando nuestra comprensión de cómo se forman estructuras anatómicamente complejas, ayudándonos a descubrir los procesos genéticos y celulares que subyacen al desarrollo humano sano, con muchas implicaciones para la investigación y el tratamiento de las enfermedades’, ha señalado la autora Sarah Teichmann, doctora en el Instituto Wellcome Sanger y cofundadora del Atlas de Células Humanas.
Ver más información: Zhang B, He P, Lawrence JEG, Wang S, Tuck E, Williams BA, et al. A human embryonic limb cell atlas resolved in space and time. Nature [Internet]. 2023[citado 7 dic 2023];. https://doi.org/10.1038/s41586-023-06806-x
8 diciembre 2023|Fuente: EFE| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
dic
7
 Líderes y expertos del sector salud se reunirán el 6 de diciembre en Ciudad de Panamá en la «Cumbre de Innovación en Salud de América Central y el Caribe», donde debatirán sobre los avances, los desafíos y la innovación en el área sanitaria.
Líderes y expertos del sector salud se reunirán el 6 de diciembre en Ciudad de Panamá en la «Cumbre de Innovación en Salud de América Central y el Caribe», donde debatirán sobre los avances, los desafíos y la innovación en el área sanitaria.
«Este encuentro se enfoca en fomentar la colaboración y el intercambio de conocimientos entre profesionales de la salud, reguladores, funcionarios gubernamentales, innovadores y médicos, centrados en las problemáticas y oportunidades actuales en la industria sanitaria de la región CamCar», detalla en un comunicado Bamberg Health, organizador del encuentro.
La cumbre abordará temas como las estrategias innovadoras en la gestión de sistemas de salud, la transformación digital en el sector salud y su impacto en la región de CamCar, o las innovaciones en infraestructura y atención médica para mejorar la atención al paciente y optimizar costos.
Daniel Para Mata, CEO de Bamberg Health, comentó que la meta de estos eventos es «brindar visibilidad global» a iniciativas locales que puedan inspirar a otros más allá de sus fronteras.
«Constantemente buscamos aprender de los actores claves del sector para ofrecer un contenido diverso y relevante que aborde los desafíos y tendencias actuales», sostuvo Para Mata.
Otros aspectos clave que se debatirán durante el foro es la implementación de tecnologías avanzadas y equipos inteligentes en hospitales y su influencia en la eficacia organizacional y la atención al paciente, los avances en terapias innovadoras incluyendo medicina de precisión y regenerativa, o la aplicación de herramientas de inteligencia artificial y análisis de datos para mejorar la calidad del sistema de salud regional.
Y es que, como indica la directora del Laboratorio Clínico del Hospital Santo Tomás de Panamá, Jovanna Itzel Borace de Cereijo, las «instalaciones de salud se hacen eficientes innovando, tanto tecnológica como digitalmente» y todo ese esfuerzo va dirigido en beneficio del paciente.
El objetivo principal de la iniciativa de Bamberg Health es transformar radicalmente el cuidado de la salud, promoviendo un enfoque centrado en la generación de conocimientos regionales.
“La sostenibilidad de los sistemas de salud dependerá en gran medida de la innovación y la articulación de todos los actores del ecosistema sanitario”, remarcó por su parte Manuel Rodríguez Arce, director del Proyecto de Expediente Digital Único en Salud, de la Caja Costarricense de Seguro Social.
7 diciembre 2023|Fuente: Proceso Digital| Noticia| Salud
dic
4
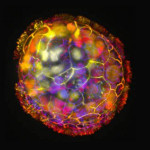 Las células de la tráquea de adultos sanos han servido para crear un diminuto robot biológico, bautizados como ‘anthrobots’, que en una placa de laboratorio pueden moverse y estimular el crecimiento de neuronas en cultivo que están dañadas.
Las células de la tráquea de adultos sanos han servido para crear un diminuto robot biológico, bautizados como ‘anthrobots’, que en una placa de laboratorio pueden moverse y estimular el crecimiento de neuronas en cultivo que están dañadas.
La creación de estos robots, que varían en tamaño desde el ancho de un cabello hasta la punta de un lápiz afilado y fueron hechos para autoensamblarse, es el resultado de una investigación de las universidades de Tufts y Harvard (EE.UU.) que dan los detalles en un estudio que publica Advances in Science.
El descubrimiento es un punto de partida para la visión de los investigadores de utilizar biobots derivados de pacientes como nuevas herramientas terapéuticas para la regeneración, la curación y el tratamiento de enfermedades, destacó la Universidad de Tufts.
Esta investigación sucede a otra publicada en 2020, en la que un equipo logró construir milimétricos robots ensamblados a partir de células embrionarias de ranas, llamados ‘xenobots’ y capaces de recolectar material, registrar información, curarse a sí mismos e incluso replicarse durante algunos ciclos por sí solos.
Los investigadores no sabían si esas capacidades dependían de que derivaran de un embrión de anfibio o si los biobots podrían construirse a partir de células de otras especies. Ahora, el equipo ha descubierto que este tipo de robots biológicos pueden crearse a partir de células adultas humanas sin ninguna modificación genética y que muestran capacidades más allá de lo observado con los ‘xenobots’.
Para su estudio, emplearon células humanas de la tráquea a las que dieron la oportunidad de reiniciarse y encontrar formas de crear nuevas estructuras y tareas. De hecho, crearon nuevas formas multicelulares y podían moverse de diferentes maneras sobre una superficie de neuronas humanas cultivadas en una placa de laboratorio, así como estimular un nuevo crecimiento para llenar los huecos causados al raspar la capa de células.
Los ‘anthrobots’ fomentan el crecimiento de las neuronas, pues estas crecían bajo la zona cubierta por un conjunto agrupado de estos robots biológicos, al que llamaron ‘superbot’, y no lo hicieron en las zonas donde no estaban. Al menos en el simplificado mundo 2D de la placa de laboratorio, los conjuntos de ‘anthrobots’ fomentaron la cicatrización eficaz del tejido neuronal vivo, agrega la universidad en un comunicado.
Aunque los investigadores aún no saben exactamente cómo lo logran, ahora están analizando cómo funciona ese mecanismo de curación y se preguntán qué más pueden hacer estas construcciones, señaló Michael Levin, firmante del artículo y de la Universidad de Tufts. Para Levin es ‘fascinante y completamente inesperado que las células traqueales de pacientes normales, sin modificar su ADN, puedan moverse por sí solas y estimular el crecimiento neuronal a través de una región dañada’. Una ventaja de utilizar células humanas incluye la capacidad de construir robots a partir de las propias del paciente para realizar trabajos terapéuticos sin el riesgo de desencadenar una respuesta inmune o requerir inmunosupresores.
Estos robots biológicos solo duran de 45 a 60 días antes de descomponerse de forma natural, por lo que el cuerpo puede reabsorberlos fácilmente una vez acabado su trabajo. Fuera del cuerpo solo pueden sobrevivir en condiciones de laboratorio muy específicas, por lo que no hay riesgo de exposición o propagación involuntaria fuera de esas instalaciones. Además, no se reproducen y no tienen ediciones, adiciones o eliminaciones genéticas, por lo que no hay riesgo de que evolucionen más allá de las salvaguardas existentes, asegura la universidad.
Para crear uno de estos ‘anthrobots’ se comienza con una célula derivada de un donante adulto procedente de la superficie de la tráquea. Estás células están cubiertas por proyecciones parecidas a pelos llamadas cilios que se mueven hacia adelante y hacia atrás. Los investigadores desarrollaron condiciones de crecimiento que animaban a los cilios a mirar hacia fuera en los organoides y a los pocos días empezaron a moverse, impulsados por los cilios que actuaban como remos. Los ‘anthrobots’ se autoensamblan en la placa de laboratorio y, a diferencia de los ‘xenobots’, no necesitan pinzas ni bisturís para darles forma, explicó Gizem Gumuskaya, también firmante de la investigación.
El equipo considera que un mayor desarrollo de los robots podría dar lugar a otras aplicaciones, como la eliminación de la placa acumulada en las arterias de pacientes con aterosclerosis, la reparación de daños en la médula espinal o los nervios de la retina, el reconocimiento de bacterias o células cancerosas, o el suministro de fármacos a tejidos específicos.
Ver más información: Gumuskaya G, Srivastava P, Cooper BG, Lesser H, Semegran B, Garnier S. Motile Living Biobots Self-Construct from Adult Human Somatic Progenitor Seed Cells. Adv Sci [Internet]. 2023[citado 2 dic 2023]; 2303575. https://doi.org/10.1002/advs.202303575
4 diciembre 2023 |Fuente: EFE| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
dic
4
 RENACER (Red Nacional de Metástasis Cerebral) es un proyecto creado por investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO), con el objetivo de almacenar muestras vivas de metástasis cerebral para favorecer la investigación oncológica.
RENACER (Red Nacional de Metástasis Cerebral) es un proyecto creado por investigadores del Centro Nacional de Investigaciones Oncológicas (CNIO), con el objetivo de almacenar muestras vivas de metástasis cerebral para favorecer la investigación oncológica.
¿Por qué es importante este estudio?
Las investigaciones oncológicas comienzan en modelos experimentales, y solo cuando se produce un descubrimiento significativo comienza la búsqueda de muestras de pacientes. Este proceso suele llevar mucho tiempo y conlleva dificultades asociadas (como el acceso a muestras). Con el proyecto RENACER se ha creado un biobanco «vivo» que ofrece la posibilidad de realizar experimentos directamente con muestras de pacientes.
Metodología
En el proyecto participan 18 hospitales españoles. Cuando un paciente con metástasis cerebral se somete a una intervención quirúrgica tiene la opción de donar una parte de su cerebro a este repositorio. Tras la cirugía, las muestras salen de quirófano en contenedores especiales, en su medio de cultivo con una temperatura de entre 4 y 8ºC y deben llegar al Biobanco del CNIO en menos de 24 horas. Se realizan cultivos organotípicos y se dividen en partes alícuotas que se almacenan como muestras para futuras investigaciones. Además, se analizan con diversas técnicas y secuencia, para extraer de ellas la mayor cantidad posible de información. Todos los datos se introducen en una base de datos abierta a la comunidad científica internacional.
Resultados principales
El proyecto se inició hace tres años y en 2 años se ha perfilado, con RNAseq y secuenciación de exosomas completos, más de 150 metástasis cerebrales. Gracias a esta red ya hay dos ensayos clínicos en marcha, que determinarán la capacidad de dos biomarcadores para discriminar los casos en que será efectiva la radioterapia.
Conclusión
La información y recursos en RENACER se contribuya al Sistema Nacional de Salud para facilitar la sostenibilidad a largo plazo y explotar plenamente los beneficios de esta estrategia emergente para la sociedad. Este proyecto se ha desarrollado para el realizar estudios básicos y clínicos que contribuyan al avance de terapias contra las metástasis cerebrales.
Ver más información: Equipo editorial Univadis. Red Nacional de Metástasis Cerebral (RENACER): primer repositorio mundial de muestras vivas de metástasis cerebral – Medscape – 1 de dic de 2023
4 diciembre 2023 | Fuente: Medscape | Tomado de Noticias y Perspectivas| Noticias de Univadis
nov
24
 El Instituto de bioingeniería de Cataluña (IBEC) coordinará el proyecto PHOTOTHERAPORT que se desarrollará con la financiación del programa Pathfinder Open del Consejo de Innovación Europeo.
El Instituto de bioingeniería de Cataluña (IBEC) coordinará el proyecto PHOTOTHERAPORT que se desarrollará con la financiación del programa Pathfinder Open del Consejo de Innovación Europeo.
Pau Gorostiza, profesor de investigación ICREA e investigador principal del grupo de Nanosondas y Nanoconmutadores del Instituto de bioingeniería de Cataluña (IBEC) y del CIBER-BBN, coordinará el proyecto PHOTOTHERAPORT financiado por el prestigioso programa Pathfinder Open del Consejo de Innovación Europeo (EIC, por sus siglas en inglés). Con esta iniciativa el EIC impulsa la exploración de ideas atrevidas para tecnologías radicalmente nuevas, apoyando colaboraciones científicas de vanguardia, interdisciplinarias y de alto riesgo/alta recompensa que sustentan avances tecnológicos.
PHOTOTHERAPORT se centra en el desarrollo de implantes luminiscentes como puertos para terapias de luz, en analogía a los que se emplean en quimioterapia para administrar fármacos. Un consorcio de 8 instituciones de 4 países, coordinado por el IBEC, llevará a cabo el proyecto con una financiación de 3 millones de euros durante los próximos 3 años.
Las terapias basadas en la luz están cobrando importancia en medicina debido a su capacidad para dirigirse a regiones específicas del cuerpo. A pesar de su demostrado potencial terapéutico, estas terapias se enfrentan a un desafío común: la atenuación de la luz visible a través de tejidos blandos y huesos antes de que llegue de manera efectiva al lugar de interés. Esta atenuación es mayor cuanto más profundos son los tejidos y órganos que se pretende alcanzar.
La plataforma PhotoTheraPort ofrece una solución a este desafío. Se trata de unos implantes diseñados para que emitan luz localmente al iluminarlos con una fuente de luz externa. Estos dispositivos incorporan nanopartículas de upconversion (conversión ascendente, en inglés), que al iluminarlas con luz infrarroja emiten fotones de mayor energía (luz visible o ultravioleta). De este modo, la emisión de luz por parte de las nanopartículas se puede controlar de forma remota y no invasiva, aplicando externamente luz infrarroja, que sí penetra a través del tejido y el hueso. La forma y el color de emisión de los PhotoTheraPorts podrán ajustarse a diversos propósitos terapéuticos. El consorcio de investigación empleará inicialmente esta plataforma para producir efectos analgésicos únicamente mediante luz, lo que se conoce cómo fotobiomodulación contra el dolor, y lo compararán con lámparas que ya se utilizan clínicamente. El propósito es tratar el dolor inflamatorio de manera más efectiva en regiones ocultas de la columna vertebral.
A continuación, los PhotoTheraPort se aplicarán a terapias de neuromodulación fotofarmacológica. Para ello se desarrollarán fotofármacos diseñados para trabajar juntamente con la plataforma de emisores de luz. Estos fármacos se activan únicamente cuando se exponen a un color de luz específico. Esta segunda tecnología se probará para reducir el dolor neuropático iluminando en ciertas regiones de la columna vertebral. También se intentará inhibir la hiperactividad neuronal característica de la epilepsia focal, que afecta a una zona limitada del cerebro y es intratable en el 30% de pacientes epilépticos.
“Nuestra meta es demostrar, dentro de cinco años, la seguridad y no toxicidad de la plataforma y acercar esta nueva terapia de fotobiomodulación al uso clínico. Los plazos de desarrollo de los fotofármacos son impredecibles, pero se prevén más largos. Si obtenemos buenos resultados preclínicos para la neuromodulación, sería la primera molécula de este tipo que cumpla con los requisitos regulatorios.” explica Gorostiza.
Una vez probada la eficacia de los PhotoTheraPort para estas patologías, la plataforma tiene el potencial de poder aplicarse a otras condiciones que requieren de tratamientos con acción localizada, como son la artritis, las enfermedades autoinmunes, las infecciones o los trasplantes. La simplicidad y versatilidad de esta innovadora plataforma pretende mejorar el tratamiento del dolor y la calidad de vida de los pacientes, además de ofrecer al sistema sanitario formas de optimizar costes médicos y ampliar sus beneficios.
El consorcio PHOTOTHERAPORT está formado por el Instituto Letón de Síntesis Orgánica, la Universidad de Tampere (Finlandia), el instituto de Tecnología Technion (Israel), la Universidad Stradins de Riga (Letonia), la Universidad de Cádiz, el Instituto de Investigaciones Biomédicas de Barcelona (IIBB-CSIC) y el Instituto Teamit, y está coordinado por el IBEC.
Ver más información:
Institute for Bioengineering of Catalonia (IBEC) . Luminescent Nanoparticle-based Implants for Pain and Epilepsy Treatment.
24 noviembre 2023 Fuente: EurekAlert Tomado de Prensa

