mar
25
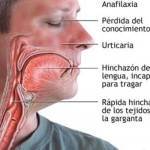 Investigadores del Hospital Universitario Vall d’Hebron de Barcelona y del Hospital Universitario de Santa María de Lleida han identificado el primer caso documentado en el mundo de transmisión de una enfermedad minoritaria -angioedema hereditario- a través de un donante de esperma anónimo en una clínica de reproducción asistida.
Investigadores del Hospital Universitario Vall d’Hebron de Barcelona y del Hospital Universitario de Santa María de Lleida han identificado el primer caso documentado en el mundo de transmisión de una enfermedad minoritaria -angioedema hereditario- a través de un donante de esperma anónimo en una clínica de reproducción asistida.
El trabajo, publicado en la revista científica Frontiers in Immunology, destaca la identificación de varios casos portadores de la misma variante genética (T328K gen F12), todos ellos concebidos mediante reproducción asistida a través de un único donante.
Angioedema hereditario
El angioedema hereditario es una enfermedad genética muy poco frecuente que provoca hinchazón en la piel, aparato digestivo o vías respiratorias; unos síntomas que afectan al 60-80 % de las mujeres portadoras, frente a una probabilidad muy baja en los hombres.
La investigación arrancó con una paciente que presentaba episodios recurrentes de hinchazón en la cara, sin responder a los tratamientos antialérgicos habituales, y cuyo análisis genético identificó la variante T328K.
Esta fue también detectada posteriormente en otras personas concebidas con el esperma del mismo donante, mientras que no estaba presente en la línea materna analizada.
Ante la sospecha de que la mutación genética podía proceder del padre, los investigadores contactaron con la clínica de fertilidad y, tras coordinar un estudio con el banco de esperma, pudieron confirmar que este era portador heterocigoto de la variante.
Notificación de la clínica
La clínica notificó entonces a las mujeres que habían utilizado el esperma de dicho donante, un procedimiento que permitió identificar a más portadores, algunos de ellos sin manifestaciones sintomáticas.
«Desde el punto de vista genético, este caso es especialmente relevante porque demuestra cómo una variante patogénica puede pasar desapercibida en un donante asintomático y transmitirse a varios descendientes», explica el jefe del grupo de Inmunología Traslacional del Vall d’Hebron Institut de Recerca (VHIR), Roger Colobran.
Los investigadores subrayan que este caso pone de relieve los retos que plantean las enfermedades genéticas hereditarias asintomáticas en los programas de donación de gametos, ya que el cribado genético de los donantes se centra principalmente en enfermedades infecciosas.
En este sentido, señalan que, en regiones donde esta variante es más prevalente, podría valorarse el cribado dirigido al gen F12.
20 marzo 2026 | Fuente: EFE | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2026. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
ago
5
 La presidenta de la Sociedad Española de Inmunología, Silvia Sánchez-Ramón, y la catedrática de Inmunología de la Universidad de Vigo, África González, han asegurado que habrá nuevas pandemias porque con la movilidad y el aumento de la población es «mucho más fácil» distribuir este tipo de infecciones.
La presidenta de la Sociedad Española de Inmunología, Silvia Sánchez-Ramón, y la catedrática de Inmunología de la Universidad de Vigo, África González, han asegurado que habrá nuevas pandemias porque con la movilidad y el aumento de la población es «mucho más fácil» distribuir este tipo de infecciones.
En una rueda de prensa para hacer balance de la séptima edición de la Escuela de Inmunología e Inmunoterapia que se está desarrollando en la Universidad Internacional Menéndez Pelayo, ambas han explicado que la capacidad infecciosa y de contagio de los virus que se distribuyen por el aire, como es el caso del coronavirus, «es tremenda».
«Antes las enfermedades se quedaban confinadas en pequeños poblados y eran patógenos muy mortales, como el virus del Nilo, porque no había movilidad de ese patógeno con otras personas», ha recordado África González.
Además de que cada vez hay más personas y más movilidad, el cambio climático también afecta a la propagación de los virus o de patógenos, porque insectos que casi habían desaparecido en determinadas zonas pueden volver o llegar y traer determinadas infecciones de otros sitios.
González ha puntualizado que la población siempre ha estado sometida a distintos microorganismos en su entorno y «es habitual tener pandemias cada cierto tiempo».
Sobre la pandemia del coronavirus, las inmunólogas han destacado que «hay que quitarse de la cabeza» que es un virus estacional como la gripe, porque «claramente no es así».
Según han apuntado, este virus ha tenido picos altos de infecciones en verano pero también en Semana Santa, cuando «claramente había más movimiento de la gente».
«El covid va a estar y va a seguir estando, seguramente cada vez más leve pero también más contagioso. Ahora mismo lo que hay son variantes, no cepas, que están circulando varias y lo van a seguir haciendo», ha añadido González.
En su opinión, cada vez que haya este tipo de infecciones respiratorias serán más leves porque ya se ha estado expuesto al virus y, por tanto, el sistema inmunitario ya lo ha visto, además de que la mayor parte de la población está vacunada y cuenta con una inmunidad reforzada.
«Incluso con las variantes que van cambiando, aunque se pierdan los anticuerpos, no se pierde la inmunidad celular y eso es muy importante», ha subrayado la catedrática de la Universidad de Vigo.
Y ha asegurado que el sistema sanitario público de España «es un ejemplo y absolutamente de lujo», que lo ha demostrado siendo capaces de vacunar a la mayor parte de la población.
01 agosto 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
abr
30
 Profesionales de la salud celebran hoy el Día Internacional de la Inmunología, a fin de divulgar la importancia de esta ciencia en la erradicación de infecciones, el cáncer y enfermedades autoinmunes.
Profesionales de la salud celebran hoy el Día Internacional de la Inmunología, a fin de divulgar la importancia de esta ciencia en la erradicación de infecciones, el cáncer y enfermedades autoinmunes.
La fecha, creada en 2005 por iniciativa de la Unión Internacional de Sociedades de Inmunología, busca sensibilizar y concienciar al mundo sobre la importancia de la investigación en inmunología y dar a conocer el funcionamiento del sistema inmunológico en la prevención de enfermedades.
Esta disciplina de las ciencias biomédicas se dedica al estudio del sistema inmunitario en la defensa del organismo ante diversos agentes internos y externos.
Cuando el sistema inmunitario no funciona adecuadamente genera ciertos tipos de alteraciones, como las enfermedades autoinmunes, inmunodeficiencias e hipersensibilidades.
Algunas recomendaciones básicas para mantener el sistema inmunitario son realizar ejercicios o alguna actividad física de manera regular, seguir una dieta equilibrada y mantener actualizado el esquema de inmunizaciones.
Asimismo, evitar situaciones de estrés prolongadas, dormir entre siete y ocho horas diarias y evitar el consumo de bebidas alcohólicas y tabaco.
En los últimos 50 años, los esfuerzos mundiales de inmunización salvaron unas 154 millones de vidas, o el equivalente a seis personas por minuto durante ese lapso.
La gran mayoría de las vidas salvadas (101 millones) fueron de niños menores de un año de edad, de acuerdo con un estudio de la Organización Mundial de la Salud.
29 abril 2024|Fuente: Prensa Latina |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
mar
22
 Los virus son las entidades biológicas más abundantes de la Tierra y se encuentran en casi todos los ecosistemas. Se trata de pequeños agentes infecciosos que se multiplican dentro de las células de todo tipo de seres vivos, desde plantas y hongos hasta bacterias, e incluso otros virus. Hasta nosotros, los seres humanos, ofrecemos un ecosistema ideal para su multiplicación.
Los virus son las entidades biológicas más abundantes de la Tierra y se encuentran en casi todos los ecosistemas. Se trata de pequeños agentes infecciosos que se multiplican dentro de las células de todo tipo de seres vivos, desde plantas y hongos hasta bacterias, e incluso otros virus. Hasta nosotros, los seres humanos, ofrecemos un ecosistema ideal para su multiplicación.
No todos los virus provocan enfermedades. Algunos forman parte de nuestra flora microbiológica natural y nos ayudan a realizar distintas funciones, al igual que lo hacen las bacterias que forman parte de nuestro sistema digestivo.
En cuanto a los que nos hacen enfermar, suelen tener un gran impacto, tanto en términos de salud como económicos. Prevenir y controlar las enfermedades que causan es una prioridad para muchos países, sobre todo tras la pandemia de covid-19 ocasionada por el SARS-CoV-2.
Lo que ocurre durante las infecciones virales
Nuestro sistema inmune trata de protegernos de los virus que nos rodean. Cuando enfermamos (infecciones agudas), se dedica a producir anticuerpos y células para combatir la infección. En la mayoría de las ocasiones, nuestro cuerpo logra vencer al virus y nos recuperamos. Este es el caso de las infecciones causadas por el virus de la gripe, el virus SARS-CoV-2 (covid-19) o el rotavirus (causante de gastroenteritis), entre otros.
¿Quiénes somos?
Sin embargo, en algunas ocasiones nuestro sistema inmune no es capaz de eliminar estos virus, que permanecen en nuestro organismo durante largos periodos de tiempo, a menudo años, o incluso durante toda la vida. Hablamos entonces de infecciones crónicas, entre las que podemos destacar a las infecciones por el virus de la hepatitis C o el virus del sida.
En otros casos, los virus pueden esconderse de nuestro sistema inmune y permanecer en un estado inactivo denominado “latencia” dentro de las células o en localizaciones de difícil acceso al sistema inmune como el sistema nervioso central (médula espinal o cerebro). En algunas ocasiones, pueden activarse y causar recidivas, como ocurre en el caso del virus de Epstein-Barr, o enfermedades crónicas, como el virus de la hepatitis B.
Afortunadamente, hoy en día existen tratamientos para combatir algunas de estas infecciones graves, ya sea para eliminar el virus causante de la infección o para controlar su replicación en caso de que no sea posible eliminarlo.
Qué ocurre después de eliminar la infección: huella viral
Hablamos de memoria inmunológica para referirnos a la capacidad que tienen algunas de las células producidas por nuestro sistema inmune de permanecer tras la infección para, en futuras infecciones, responder de manera más rápida. Coloquialmente se conoce como “hacerse inmune”, y es la base de la inmunidad adquirida.
Sin embargo existe un concepto que va aún más lejos: la huella viral. Se trata de una serie de respuestas inmunológicas a largo plazo, incluso años después de que la infección se haya resuelto o el virus haya entrado en estado de latencia, que pueden desequilibrar nuestro sistema inmune, haciéndolo más débil (inmunosupresión) o más reactivo de lo normal.
También se ha observado que los virus pueden acelerar los procesos de envejecimiento del sistema inmune (inmunosenescencia), donde hay una acumulación progresiva de células envejecidas que no son capaces de cumplir correctamente su función inmune.
Estos procesos relacionados con el envejecimiento forman parte de un círculo vicioso que deteriora el funcionamiento del sistema inmunitario. Por un lado, las células senescentes acumuladas liberan moléculas que provocan inflamación, entre otros efectos. Por otro, la inflamación que se produce altera al sistema inmune, contribuyendo a la inmunosenescencia.
La huella viral puede condicionar el riesgo de futuras enfermedades
Todo este impacto en el sistema inmune deja a las personas en situación de vulnerabilidad frente a otras infecciones. Además, y más allá del conocido síndrome de fatiga posviral, aumenta el riesgo de desarrollar distintas enfermedades como las cardiovasculares, diabetes, trastornos neurológicos y desarrollo de tumores, entre otras.
Estas enfermedades se han relacionado con una gran variedad de virus. Por ejemplo, el virus Epstein-Barr, el virus de la hepatitis C o el VIH/SIDA pueden aumentar el riesgo de enfermedades cardiovasculares y diabetes tipo 2. Otros, como el virus de la gripe o el virus Epstein-Barr, se han visto asociados a trastornos neurológicos como la depresión, la esquizofrenia, el alzhéimer y la esclerosis múltiple.
Algunos virus también aumentan el riesgo de desarrollar ciertos tipos de cáncer. Es el caso del virus del sida (asociado a cáncer de hígado, pulmón o linfoma de Hodgkin), los virus de la hepatitis B y C (asociado a carcinoma hepatocelular, linfoma no-Hodgkin o cáncer de cabeza y cuello), el papilomavirus (asociado a carcinoma cervical, esofágico o anal), el virus Epstein-Barr (asociado a carcinoma nasofaríngeo, cáncer de colon y linfoma de Burkitt) o el virus linfotrópico de células T humanas (asociado a varios tipos de leucemias y linfomas).
Para colmo, las infecciones virales pueden dejar huellas de formas más sutiles. Por ejemplo, se ha observado que algunas infecciones virales pueden alterar la microbiota intestinal. Esta microbiota está muy relacionada con el sistema inmunitario, y cambios en ella pueden aumentar el riesgo de enfermedades autoinmunes y alergias a largo plazo.
Actualmente, muchos investigadores estudian cómo los virus dejan huellas duraderas en nuestro cuerpo y su relación con la salud a largo plazo. Invertir en esta línea de investigación resulta crucial para saber cómo las infecciones virales afectan a nuestro sistema inmunitario a corto, medio y largo plazo. Pero también para encontrar nuevos biomarcadores para identificar a las personas que tienen más riesgo de sufrir complicaciones después de una infección. Solo así podremos desarrollar estrategias de prevención y tratamiento eficaces.
19 marzo 2024| Fuente: The conversation| Tomado de| Medicina| Salud
dic
9
 El nuevo premio nobel de Medicina Drew Weissman, cuyas investigaciones están en la base de la tecnología que hizo posibles las vacunas contra la covid-19, cree que aún hay margen de mejora y está trabajando para conseguir una inmunización universal frente a los coronavirus.
El nuevo premio nobel de Medicina Drew Weissman, cuyas investigaciones están en la base de la tecnología que hizo posibles las vacunas contra la covid-19, cree que aún hay margen de mejora y está trabajando para conseguir una inmunización universal frente a los coronavirus.
El inmunólogo estadounidense ha merecido este año el galardón junto a la bioquímica húngara Katalin Karikó por crear la tecnología que permite usar ARN mensajero como agente terapéutico, premio que recogerán junto al resto de galardonados el próximo domingo. Esa investigación fue crucial para desarrollar las primeras vacunas de la pandemia, salvando millones de vidas y previniendo enfermedades graves en muchas más, según dijo, al dar a conocer el premio, el Instituto Karolinska, encargado de otorgar este nobel.
Weissman (1959) señaló a EFE que aún hay margen para mejorar las vacunas basadas en ARN mensajero para la covid-19, un virus que muta de forma similar a la gripe, lo que supone que cada año haya que hacer nuevas vacunas pues el virus ya no es bloqueado por la del año anterior. Sin embargo, el nuevo nobel ya está trabajando, tanto en su laboratorio de la Facultad de Medicina de la Universidad de Pensilvania (EE.UU), como con un grupo internacional, en una vacuna ‘pancoronavirus’ o universal, ‘que protegerá contra todos’.
Dicha inmunización, que ‘tal vez sirva para cinco años, pero eso no lo sabemos aún’, evitará cualquier nuevo coronavirus, incluso los que puedan pasar a personas, procedentes por ejemplo de murciélagos, y cualquiera de las variantes del actual covid-19. El candidato vacunal se dirige a la fase de ensayos clínicos (con personas), pues hay uno que empezará en Tailandia, ‘probablemente dentro de seis u ocho meses’ y también trabaja en otro, de inicio ‘probablemente dentro de un año’, en colaboración con la Universidad de Duke (EE.UU).
El centro de las investigaciones de Weissman y Karikó es el ARN mensajero (ARNm) o ácido ribonucleico mensajero, un tipo de molécula que transporta la información genética necesaria de una parte de la célula a otra para fabricar las proteínas que nos permiten vivir. Ambos científicos, en aquella época en la Universidad de Pensilvania, descubrieron cómo modificar las moléculas de ARN para usarlas como agente terapéutico sin que el sistema inmune humano las destruyera e idearon un sistema para ponerlo en nanopartículas, lo que evita su rápida degradación.
Aunque durante la pandemia, esta tecnología se convirtió en base para el rápido desarrollo de vacunas, su potencial es muy grande en las más distintas áreas de la medicina, y Weissman estimó que ‘los principales cambios se producirán en los próximos 10 o 20 años’. En la actualidad -dijo- su equipo tiene siete vacunas en fase uno de ensayos clínicos para prevenir, entre otros, los norovirus (que causan vómitos y diarreas) o bacterias como ‘Clostridioides difficile’, que provoca infección en el intestino grueso, sin olvidar una universal para la gripe.
Además, ha creado un programa de terapia génica contra la malaria, que espera poder empezar a administrar en los próximos dos años, entre otras ‘muchas terapias en desarrollo’. Weissman lleva años investigando una vacuna para el VIH, de hecho ese era su objetivo principal cuando en 1997 conoció de forma casual, en una fotocopiadora de la Universidad, a Karikó. Ella ya investigaba en ARN-mensajero y allí comenzaría una estrecha colaboración de más de dos décadas.
Entre los proyectos de vacunas que está investigando el laboratorio de Weissman hay ‘un par’ dirigidas al VIH, que ‘probablemente tardarán entre cinco y siete años’ en llegar a fase tres (la última) de los ensayos clínicos. Además, destacó un programa de curación de la enfermedad, que ya prueba en modelos de macacos y ‘en seis meses sabremos si funciona’ si ese fuera el caso el próximo paso sería la prueba con pacientes.
El futuro del ARN-mensajero es muy prometedor, pero en el inicio de las investigaciones su potencial contó con poca atención de otros científicos. Sin embargo lo hoy nuevos nobeles siempre lo tuvieron claro. ‘Hace 25 años, Katie y yo enumerábamos todo lo que podía hacer el ARN-mensajero, pero bromeábamos diciendo que probablemente moriríamos antes de que este dejara huella en el mundo. Sin embargo, hemos sobrevivido hasta ahora’, dijo.
9 diciembre 2023|Fuente: EFE| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
oct
25
 Para defendernos adecuadamente de cualquier patógeno que pueda entrar en nuestro organismo, las células del sistema inmunitario deben estar en continuo movimiento, de manera que ejerzan una labor de vigilancia hasta en los más recónditos lugares de nuestro cuerpo. Las células de la inmunidad inespecífica (granulocitos, macrófagos, células dendríticas, células NK y mastocitos, entre otras) tienen una distribución muy dispersa, pero las células de la inmunidad específica se encuentran sobre todo en los órganos inmunitarios secundarios, en los que se va a producir la presentación del antígeno y la estimulación de los linfocitos capaces de reconocerlo.
Para defendernos adecuadamente de cualquier patógeno que pueda entrar en nuestro organismo, las células del sistema inmunitario deben estar en continuo movimiento, de manera que ejerzan una labor de vigilancia hasta en los más recónditos lugares de nuestro cuerpo. Las células de la inmunidad inespecífica (granulocitos, macrófagos, células dendríticas, células NK y mastocitos, entre otras) tienen una distribución muy dispersa, pero las células de la inmunidad específica se encuentran sobre todo en los órganos inmunitarios secundarios, en los que se va a producir la presentación del antígeno y la estimulación de los linfocitos capaces de reconocerlo.
El carácter disperso del sistema inmunitario plantea tres interesantes incógnitas muy difíciles de resolver: cuántas células inmunitarias tenemos, cuántas tenemos exactamente en cada órgano y cuánto es su peso total.
Un interesante estudio recién publicado trata de responder a estas preguntas. Como contar una a una las células es completamente imposible, los autores han usado una triple estrategia.
En primer lugar, han realizado una extensa revisión bibliográfica, recabando todos los datos disponibles referidos a la presencia de células inmunitarias en los tejidos. En concreto, trataron de recopilar las distintas densidades celulares, es decir, el número de células por gramo de tejido, además de datos histológicos.
Nuestra misión es compartir el conocimiento y enriquecer el debate.
En segundo lugar, emplearon imágenes de células en canales múltiples, una nueva tecnología que permite identificar muchos biomarcadores de manera simultánea. Eso permite reconocer tejidos y fenotipos celulares complejos.
Y, en tercer lugar, echaron mano de la de convolución basada en patrones de metilación. Aunque el nombre puede parecer rocambolesco, la de convolución celular consiste en estimar, mediante técnicas computacionales, la proporción de células que existe en un tejido concreto. Como cada célula tiene un patrón de metilación característico, la combinación de ambas técnicas permite identificar las diferentes subpoblaciones celulares presentes en una muestra.
Nuestro sistema inmune tiene 1,8 billones de células
El uso y la validación cruzada de estas tres técnicas ha permitido a los autores llegar a la conclusión de que una persona prototípica –eso sí, varón de 20-30 años, 176 cm de estatura y 73 kg de peso– tiene un total de 1,8×10¹² células. Es decir, casi dos billones (según la nomenclatura española) de células. Son muchas, especialmente si tenemos en cuenta que los tejidos muscular y adiposo constituyen el 75 % del total de la masa corporal pero que, al tratarse de células muy grandes, solo representan el 0,2 % de todas las células de nuestro organismo.
La mayoría de las células inmunitarias se ubican en dos lugares: la médula ósea y el tejido linfático. La médula ósea contiene un 40 % de esa astronómica cantidad total de células –en un 80 %, neutrófilos–. En el tejido linfático se ubica el 39 % de las células inmunes, con un importante predominio de linfocitos. La piel, los pulmones y el tracto gastrointestinal albergan, cada uno de ellos, un modesto 3 % del total.
Distribución de las células inmunitarias en el cuerpo humano. Estimaciones de las poblaciones de células inmunitarias por tipo de célula y tejido agrupadas por tejidos y sistemas primarios. GI significa tracto gastrointestinal. PNAS, CC BY-NC-ND.
Los macrófagos, que tienen una escasa representación en muchos tejidos, se acumulan en el hígado, donde representan el 70 % de las células inmunitarias de este órgano. También residen aquí un 30% de todas las células NK. De ahí se deduce que el hígado juega un importante papel en la respuesta inmunitaria, en especial en lo que se refiere a la eliminación de antígenos que han entrado por vía digestiva.
Si el sistema inmunitario fuese un órgano sólido pesaría más de un kilo
El estudio ofrece algunos descubrimientos sorprendentes. Por ejemplo, que si el sistema inmunitario fuese un órgano sólido pesaría 1.2 kg. O, lo que es lo mismo, tendría casi el mismo peso del hígado, considerado el órgano más grande y pesado.
De esos 1.2 kilos, los macrófagos, que representan apenas el 15 % del total de células inmunitarias, pesarían 600 gramos. Y las aún más escasas células dendríticas pesarían otros 100 gramos más. ¿Por qué? Pues debido al gran tamaño de estos dos tipos de células, que se contrapone al de los pequeños linfocitos, que a pesar de su elevado número solo representarían menos de 200 gramos en su conjunto. La masa de células inmunitarias contenidas en la médula ósea y el tejido linfático es la más relevante de todas (30 % y 27 % del total, respectivamente).
No obstante, la mayor sorpresa está relacionada con el tracto gastrointestinal. A diferencia de lo que se pensaba, aquí solo se ubica un 3 % del total de células inmunitarias, muchas menos de las esperadas. Y resulta también sorprendente que en el digestivo se acumulen alrededor de un 70 % de las células plasmáticas totales, que son las productoras de anticuerpos.
Mirando al futuro
Este estudio es relevante porque combina múltiples aproximaciones para resolver problemas que no permiten un abordaje directo, y que podría ser de interés para determinar el número de células pertenecientes a otros linajes.
Lo que es más importante aún, al ofrecernos una distribución global de las células del sistema inmunitario puede ayudarnos a entender mejor su organización global y, por tanto, cómo modularlo para diseñar terapias innovadoras.
Sender R, Weiss Y, Navon Y, Milo I, Azulay N, Keren L, et al. The total mass, number, and distribution of immune cells in the human body. PNAS[Internet]2023[citado 23 oct 2023];120 (44): e2308511120. https://doi.org/10.1073/pnas.2308511120.
25 octubre 2023 | Fuente: Conversación

