sep
21
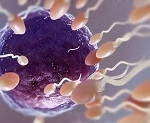 Un trabajo, en el que participa el IIBB-CSIC, revela los mecanismos moleculares que impiden que el ADN mitocondrial se herede de los padres
Un trabajo, en el que participa el IIBB-CSIC, revela los mecanismos moleculares que impiden que el ADN mitocondrial se herede de los padres
CSIC/DICYT Un rasgo evolutivo de los humanos y de la mayoría de animales es que heredan el ADN mitocondrial exclusivamente de la madre, a pesar de que los espermatozoides del padre tienen mitocondrias. Si los espermatozoides tienen mitocondrias, ¿por qué no trasmiten ADN mitocondrial?
Responder a esta pregunta es lo que ha hecho un equipo internacional en un trabajo publicado en Nature Genetics y que cuenta con la participación de investigadores del Instituto de Investigaciones Biomédicas de Barcelona del CSIC (IIBB). Tras varios años de investigación, han podido demostrar que los espermatozoides no tienen ADN mitocondrial y que, además, sus mitocondrias carecen de un factor de transcripción A (o TFAM, del inglés Transcription Factor A mitocondrial) que es imprescindible para que el ADN mitocondrial humano se replique.
“En muchas especies, incluida la humana, las mitocondrias del espermatozoide se introducen en el óvulo durante la fecundación, así que una de las hipótesis existentes era que el ADN mitocondrial sí que llegaba al ovocito pero se eliminaba en el proceso de fecundación”, detalla el investigador Ramón Trullás, investigador del CSIC en el IIBB y del Centro de Investigación Biomédica en Red de Enfermedades Neurodegenerativas (CIBERNED). Ramón Trullás ha desarrollado esta investigación con su equipo, formado por Anna Calderon, Margalida Puigròs y Petar Podlesniy. Han colaborado junto con los equipos de Shoukhrat Mitalipov (Oregon Health & Science University, EUA) y Dmitry Temiakov, coordinador del estudio, y su equipo William Lee, Angélica Zamudio-Ochoa y Gina Buchel (Thomas Jefferson University, EUA).
PCR digital
Para averiguar si los espermatozoides tienen ADN mitocondrial, los investigadores del IIBB-CSIC han desarrollado una técnica de PCR digital, más precisa que el PCR convencional y que permite cuantificar en una misma muestra el número absoluto de ADN en diferentes tipos de células. Los análisis se han realizado con muestras procedentes de clínicas de Oregón (EEUU).
Los resultados muestran que los espermatozoides no tienen ni una sola molécula completa de ADN mitocondrial, y que el ADN mitocondrial residual encontrado probablemente ni siquiera es de los espermatozoides. “Cada espermatozoide contiene entre 50 y 70 mitocondrias, que corresponden a menos de 0,01 moléculas de ADN mitocondrial. Aunque extremadamente bajo, esta cifra probablemente se explicaría por unas pocas células que contaminaban las muestras (concretamente leucocitos)”, explican los autores en el trabajo.
Los investigadores han descubierto que lo que explica la ausencia de ADN en las mitocondrias del espermatozoide es un proceso de relocalización del factor de transcripción TFAM, una molécula que penetra en las mitocondrias para la replicación del ADN mitocondrial. Durante la espermatogénesis, el espermatozoide modifica la señal de localización de TFAM y no permite que penetre en las mitocondrias sino que la dirige al núcleo del espermatozoide, lo que evita la replicación del ADN mitocondrial.
“Nuestro trabajo demuestra que la modificación de TFAM durante la espermatogénesis resulta en la eliminación del ADN mitocondrial y explica su herencia materna. Un proceso fascinante, producto de la evolución, que impide la herencia del ADN paterno”, añade Trullás.
Este descubrimiento de la relocalización de TFAm tiene importantes implicaciones para los campos de la fertilidad humana y la terapia de células germinales, ya que podría explicar algunos casos de oligospermia y de oligoastenospermia, una alteración en la que se da un bajo recuento y una baja movilidad de espermatozoides. De hecho, se han encontrado niveles elevados de ADN mitocondrial en el esperma de hombres infértiles con oligoastenospermia grave, dicen los investigadores.
Referencia
Lee W, Zamudio-Ochoa A, Buchel G, Podlesniy P, Marti Gutierrez N, Puigros M, et al. Molecular basis for maternal inheritance of human mitochondrial DNA. Nat Genet. 2023. https://doi.org/10.1038/s41588-023-01505-9
https://www.nature.com/articles/s41588-023-01505-9
20/09/2023
Fuente: (Dicyt) Noticias – Salud España
sep
11
 Un reciente estudio internacional ha identificado nuevos genes y variantes genéticas que aumentan el riesgo a desarrollar cáncer de mama.
Un reciente estudio internacional ha identificado nuevos genes y variantes genéticas que aumentan el riesgo a desarrollar cáncer de mama.
Pese a los relevantes avances en diagnóstico y tratamiento, el cáncer de mama sigue siendo la principal causa de muerte en mujeres. Según datos de la Organización Mundial de la Salud, solo en 2020, fallecieron alrededor de 685 000 mujeres por esta enfermedad.
Los factores genéticos juegan un papel importante en el cáncer de mama. Estudios realizados en los últimos años han identificado tanto variantes genéticas concretas, poco frecuentes, que confieren un riesgo elevado a la enfermedad, como variantes más comunes que tienen un menor peso. Sin embargo, todavía no está disponible el mapa completo de susceptibilidad genética a la enfermedad, información con la que podría estimarse mejor la probabilidad de cada persona a tener la enfermedad.
A partir del análisis del exoma completo de 26 368 mujeres con cáncer de mama y 217 673 mujeres control, un reciente estudio, publicado en Nature Genetics, amplia el mapa genético de la enfermedad al aportar evidencias de nuevos genes de susceptibilidad.
“Que sepamos, éste es el mayor estudio de este tipo. Ha sido posible gracias al uso de datos de múltiples colaboradores de muchos países, así como de datos de acceso público del Biobanco del Reino Unido”, ha señalado Douglas Easton, director del Centro de Epidemiología Genética del Cáncer de la Universidad de Cambridge, y codirector del estudio.
Análisis de exomas para identificar contribuyentes genéticos al cáncer de mama
Para identificar nuevas variantes poco frecuentes, los investigadores analizaron los datos genómicos de tres grandes proyectos internacionales y compararon los exomas (regiones codificantes del genoma) de las pacientes con cáncer de mama respecto al de mujeres no diagnosticadas. Especialmente analizaron la variación genética que lleva a proteínas truncadas y la variación genética que da lugar a cambios de aminoácidos en las proteínas que derivaran en un efecto deletéreo.
Además de detectar variantes genéticas relacionadas con el cáncer de mama en genes de susceptibilidad ya conocidos como ATM, BRCA1, BRCA2, CHEK2 y PALB2, los investigadores encontraron evidencias de nuevos genes relacionados con la enfermedad: LZTR1, ATR, BARD1, CDKN2A y MAP3K1.
Aplicaciones en predicción de riesgo y desarrollo de tratamientos
La información obtenida en el estudio, podría mejorar las predicciones de riesgo del cáncer de mama. En la actualidad, la mayor parte de pruebas genéticas para el cáncer de mama en el ámbito clínico están dirigidas a detectar variantes en los genes más conocidos, pero disponer de mayor información a nivel genético podría aportar más precisión.
“Aunque la mayoría de las variantes identificadas en estos nuevos genes son poco frecuentes, los riesgos pueden ser importantes para las mujeres portadoras”, ha destacado Jacques Simard de la Universidad Laval, codirector del trabajo. “Por ejemplo, las alteraciones en uno de los nuevos genes, MAP3K1, parecen dar lugar a un riesgo especialmente elevado de cáncer de mama.”
“Necesitamos datos adicionales para determinar con mayor precisión los riesgos de cáncer asociados a las variantes de estos genes, estudiar las características de los tumores y comprender cómo se combinan estos efectos genéticos con otros factores del estilo de vida que afectan a los riesgos de cáncer de mama”, ha señalado también Douglas Easton.
En paralelo a su utilidad predictiva, la identificación de nuevos genes con potencial implicación en el cáncer de mama, amplía el conocimiento de los mecanismos que participan en la enfermedad. Esta información podría contribuir a detectar nuevas dianas de tratamiento.
Por último, los resultados del trabajo también apuntan a que una parte importante de los genes relacionados con la enfermedad deben encontrarse en regiones no codificantes. Estudios futuros deberán evaluar esta cuestión.
Referencia
Wilcox N, Dumont M, González-Neira A, Carvalho S, Beauparlant CH , Crotti M, et al. Exome sequencing identifies breast cancer susceptibility genes and defines the contribution of coding variants to breast cancer risk. Nat Genet (2023). https://doi.org/10.1038/s41588-023-01466-z
https://www.nature.com/articles/s41588-023-01466-z
07/09/2023 (Genotipia.com) Genética Médica Copyright 2023 © Genotipia
sep
6
 Las mutaciones del gen NEK1 se han relacionado con hasta el 2% de todos los casos de ELA, lo que lo convierte en una de las causas más conocidas de la enfermedad, pero se desconocía cómo el gen mutado altera la función de la motoneurona y provoca su degeneración y muerte. Ahora, científicos de Northwestern Medicine, de la Universidad de Northwestern (EE.UU.), han descubierto por primera vez cómo este gen mutado conduce a la ELA, según publican en Science Advances.
Las mutaciones del gen NEK1 se han relacionado con hasta el 2% de todos los casos de ELA, lo que lo convierte en una de las causas más conocidas de la enfermedad, pero se desconocía cómo el gen mutado altera la función de la motoneurona y provoca su degeneración y muerte. Ahora, científicos de Northwestern Medicine, de la Universidad de Northwestern (EE.UU.), han descubierto por primera vez cómo este gen mutado conduce a la ELA, según publican en Science Advances.
Los investigadores descubrieron que la mutación causa dos problemas en la neurona. El primero es que hace que las estructuras que sostienen el axón en la neurona se vuelvan menos estables y susceptibles de colapsarse. El segundo problema es que la mutación altera la capacidad de la neurona para importar carga en forma de ARN o proteínas a su núcleo (importación nuclear). Sin la importación de ARN y proteínas críticas, se interrumpe el papel operativo del núcleo para la función de la célula. Al esclarecer estas dos vías, sugieren que son grandes dianas terapéuticas para la enfermedad.
Los autores consideran que este descubrimiento es importante porque un gran avance en la investigación de la ELA en los últimos años fue descubrir que la importación nuclear está alterada en otras formas de ELA genética, de modo que sus resultados relacionan esta nueva causa de ELA con otras causas genéticas en las que se interrumpe el mismo proceso. De hecho, una de las principales cuestiones sin resolver en este campo es si la ELA es una sola enfermedad o un conjunto de versiones genéticamente distintas de menor tamaño bajo el «paraguas» de los mismos problemas clínicos, y este descubrimiento, referido a los mismos mecanismos destructivos en otras formas genéticas de ELA, lleva a creer que se trata de la misma enfermedad, algo fundamental para desarrollar tratamientos y para diseñar ensayos clínicos óptimos dirigidos a poblaciones específicas de pacientes con ELA.
Referencia
Jacob R. Mann et al. Loss of function of the ALS-associated NEK1 kinase disrupts microtubule homeostasis and nuclear import. Sci. adv. 9,eadi5548(2023). DOI:10.1126/sciadv.adi5548
https://www.science.org/doi/10.1126/sciadv.adi5548#tab-citations
28/08/2023(Neurología.com) Tomado- Noticia © Viguera Editores, S.L.U. 2023
sep
2
Investigadores del Instituto Weizmann identifican un biomarcador que podría permitir a un subgrupo de pacientes con cáncer de pulmón beneficiarse de un tratamiento sin recaídas.
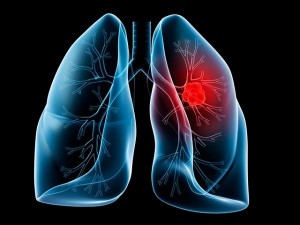 Las personas no fumadoras que desarrollan cáncer de pulmón pueden ser tratadas eficazmente con nuevos fármacos, pero sus tumores se niegan a rendirse sin luchar. Los fármacos dejan de funcionar a largo plazo porque los tumores adquieren mutaciones secundarias que les permiten eludir el efecto terapéutico de los medicamentos.
Las personas no fumadoras que desarrollan cáncer de pulmón pueden ser tratadas eficazmente con nuevos fármacos, pero sus tumores se niegan a rendirse sin luchar. Los fármacos dejan de funcionar a largo plazo porque los tumores adquieren mutaciones secundarias que les permiten eludir el efecto terapéutico de los medicamentos.
Una investigación publicada en la revista Cell Reports Medicine y realizada por investigadores del Instituto Weizmann de Ciencias proporciona resultados que podrían llevar a un tratamiento sin recaídas para un subgrupo considerable de pacientes con cáncer de pulmón. En un estudio realizado en ratones, los científicos han identificado un biomarcador que podría ayudar a los médicos a seleccionar a los pacientes con cáncer de pulmón que pueden ser tratados con un único fármaco basado en anticuerpos, el cual posiblemente derive en una remisión completa, sin recaída del cáncer.
“Hemos hallado un biomarcador potencial que podría cambiar la forma en que se trata a los pacientes con cáncer de pulmón en todo el mundo”, afirma el profesor Yosef Yarden, del Departamento de Inmunología y Biología Regenerativa de Weizmann, director del estudio. “De forma similar a cómo la presencia de mutaciones en genes BRCA predice cómo responderán los pacientes con cáncer de mama y ovario a los fármacos, el nuevo biomarcador podría hacer posible emparejar a algunos pacientes con cáncer de pulmón con la medicación específica con más probabilidades de ayudarles.”
Centrarse en las mutaciones que importan
La mayoría de los cánceres de pulmón se deben al tabaquismo, pero la segunda mayor fracción de casos afecta a no fumadores y se caracteriza por mutaciones en un gen llamado EGFR. El estudio comenzó cuando la Dra. Ilaria Marrocco, entonces investigadora postdoctoral en el laboratorio de Yarden, revisó la bibliografía de ensayos clínicos y se dio cuenta de que todos los pacientes con cáncer de pulmón EGFR-positivo recibían el mismo tratamiento multimedicamentoso, independientemente de cuál de las 30 mutaciones conocidas del EGFR se encontrara en sus tumores. Eventualmente, estos pacientes acababan desarrollando una resistencia a los fármacos que provocaba la recaída del cáncer. Marrocco se preguntó si, clasificando los tumores de pulmón en función de las mutaciones específicas del gen EGFR, sería posible crear un protocolo farmacológico más personalizado y lograr mejores resultados.
“La observación del Dr. Marrocco nos inspiró para buscar un biomarcador que predijera qué pacientes responderían bien a la terapia, según las mutaciones específicas que portaran”, señala Yarden. Los científicos decidieron centrarse en una de las dos variantes genéticas más comunes asociadas al gen EGFR en el cáncer de pulmón: la mutación L858R, en la que un solo aminoácido, de entre varios cientos, se sustituye por otro, en la posición 858 de la proteína EGFR. Esta mutación se produce en aproximadamente el 40 por ciento de los pacientes con cáncer de pulmón cuyos tumores se caracterizan por mutaciones en el gen EGFR.
Los científicos eligieron estudiar el cambio L858R porque, a diferencia de otras mutaciones que afectan a EGFR, tiene un impacto único en su función. “A diferencia de las demás mutaciones, esta mutación requiere que los receptores se emparejen en la membrana de la célula cancerosa, tras lo cual se envían al núcleo señales que ordenan a la célula iniciar la replicación”, explica Yarden. “Utilizando un modelo de ratón de cáncer de pulmón con la mutación L858R, descubrimos que, si no se produce este emparejamiento, es como un cortocircuito: la señal para iniciar la replicación celular no puede enviarse al núcleo y el tumor no crece”.
A continuación, los investigadores bloquearon la unión tratando a los ratones con un fármaco anticuerpo llamado cetuximab, conocido por su nombre comercial Erbitux, desarrollado a partir de las investigaciones de Yarden y el difunto profesor Michael Sela. Erbitux ha sido aprobado por la FDA para el tratamiento del cáncer de colon y de cabeza y cuello.
“Tras el tratamiento con Erbitux, los tumores de pulmón de los ratones se redujeron y no volvieron a aparecer, ni siquiera después de mucho tiempo”, afirma Yarden. “Estos resultados indican que, para el gran número de pacientes humanos con cáncer de pulmón que presentan la mutación L858R, un único fármaco podría ofrecer una vía hacia la recuperación total, sin el devastador fenómeno de la recaída del cáncer”.
El nuevo estudio también explica por qué los intentos anteriores de tratar con Erbitux el cáncer de pulmón con mutaciones en EGFR habían fracasado o, en el mejor de los casos, habían producido resultados contradictorios. “Desde que se aprobaron los nuevos inhibidores del EGFR como fármacos contra el cáncer de pulmón hace casi 10 años, todos los pacientes reciben estos medicamentos anti-EGFR, independientemente de la identidad y el número de sus mutaciones en EGFR. Son muy eficaces durante un tiempo, pero permiten la aparición de mutaciones secundarias que aceleran la recaída del cáncer”, explica Yarden. “En el momento en que se administra Erbitux, suele ser ineficaz porque sólo puede actuar contra determinadas mutaciones en EGFR. Nuestro estudio demuestra la importancia de preseleccionar desde el principio a los pacientes con cáncer de pulmón que pueden ser tratados eficazmente con Erbitux, en función de su perfil de mutaciones.”
Los científicos afirman que el siguiente paso sería poner en marcha un ensayo clínico para establecer la eficacia de este tratamiento en pacientes humanos con cáncer de pulmón, algo que se verá facilitado por el hecho de que Erbitux ya ha sido aprobado para tratar otros tipos de cáncer. Mientras tanto, Yarden y Marrocco están entusiasmados con la posibilidad de que su investigación acabe repercutiendo en la práctica clínica. “El biomarcador L858R podría ayudar a salvar vidas al ofrecer a los médicos una forma de proporcionar un tratamiento farmacológico personalizado a los pacientes con cáncer de pulmón portadores de la mutación pertinente”, señala Marrocco.
Artículo científico: Marrocco I, Giri S, SimonI et al. L858R emerges as a potential biomarker predicting response of lung cancer models to anti-EGFR antibodies: Comparison of osimertinib vs. cetuximab. Cell Rep Med. 2023 Aug 3:101142. doi: http://dx.doi.org/10.1016/j.xcrm.2023.101142
Referencia
Marrocco I, Giri S, Simoni-Nieves A, Gupta N, Rudnitsky A, Haga Y, et al. L858R emerges as a potential biomarker predicting response of lung cancer models to anti-EGFR antibodies: Comparison of osimertinib vs. cetuximab. Cell Reports Medicine. 2023, 4(8). https://doi.org/10.1016/j.xcrm.2023.101142.
https://www.sciencedirect.com/science/article/pii/S2666379123002951?via%3Dihub
28/08/2023(genotipia.com) Tomado- Noticias de investigación Copyright 2023 © Genotipia
sep
2
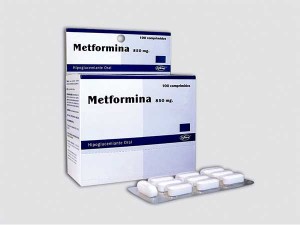 Un estudio que combina información genómica y epidemiológica ofrece nuevas evidencias de que la metformina, un fármaco utilizado en el tratamiento de la diabetes, puede promover un envejecimiento saludable y tener un efecto protector frente a enfermedades asociadas a la edad.
Un estudio que combina información genómica y epidemiológica ofrece nuevas evidencias de que la metformina, un fármaco utilizado en el tratamiento de la diabetes, puede promover un envejecimiento saludable y tener un efecto protector frente a enfermedades asociadas a la edad.
En la actualidad, la metformina es un fármaco de primera línea para el tratamiento de la diabetes tipo 2, a través de su función para controlar los niveles de azúcar en sangre. En paralelo a su utilización en el contexto de la diabetes, diferentes estudios empiezan a plantear si la metformina podría promover un envejecimiento más sano.
Con el objetivo de aportar nuevas evidencias sobre esta posibilidad un equipo de investigadores de la Universidad de Hong Kong ha estudiado a nivel genético el efecto de la metformina sobre diferentes características relacionadas con el envejecimiento. Esta aproximación, conocida como randomización mendeliana, aprovecha las combinaciones aleatorias de variantes genéticas presentes en cada persona y reduce los posibles sesgos que ocurren en estudios observacionales.
Conexión entre variación genética y características de envejecimiento
Para el estudio los investigadores utilizaron la información genética de 321 412 participantes del Biobanco de Reino Unido, de los que había disponible información genómica y fenotípica.
Dentro de la información genética, el equipo consideró la variación genética de los 10 genes relacionados con las cuatro dianas supuestas de la metformina: AMPK, ETFDH, GPD1 y PEN2 y estudió su variabilidad respecto a las variables de interés relacionadas con el envejecimiento: edad cronológica, nueve marcadores clínicos y la longitud de los telómeros de los leucocitos.
Tras analizar los datos, los investigadores detectaron asociación entre algunos de los genes estudiados y características de envejecimiento saludable. Por ejemplo, la reducción genética en los niveles de hemoglobina glicosilada inducida por la metformina a través de GPD1, estaba asociada a una edad biológica más joven y longitud mayor de los telómeros. En el caso de otra diana de la metformina, AMPKγ2, el equipo detectó una asociación con la edad biológica.
“Cada vez hay más pruebas que sugieren que la metformina también puede ejercer su efecto a través de vías independientes de la glucemia. La mejor comprensión de los mecanismos de acción de la metformina a través de aproximaciones de big data y diferentes ómicas está garantizada y mejora la evaluación de su potencial de reposicionamiento”, ha señalado Luo Shan Investigador en la Universidad de Hong Kong que ha participado en el estudio.
Evidencias para el reposicionamiento de la metformina
Los resultados del trabajo, publicados en The Lancet Healthy Longevity, proporcionan nuevas evidencias genéticas de que la metformina podría promover el envejecimiento saludable a través de dianas como GDP1 y AMPKγ2. Estas conclusiones apoyan la realización de nuevas investigaciones dirigidas a reposicionar el fármaco metformina, desde su utilización como tratamiento de la diabetes, a la regulación de la biología relacionada con el envejecimiento.
Entre los futuros estudios dirigidos a determinar los efectos y mecanismos exactos de la metformina en relación a la longevidad, destaca el ensayo clínico TAME (Metformina Dirigida al Envejecimiento en sus siglas en inglés), aprobado por la FDA y en la actualidad en sus primeras etapas.
Una ventaja para este reposicionamiento es que la metformina es un fármaco asequible a nivel económico y ya aprobado (por lo que se conoce su perfil de seguridad).
“Nuestro trabajo ha demostrado la utilidad de utilizar estudios epidemiológicos a gran escala y datos genómicos para evaluar las oportunidades de reposicionamiento de fármacos. Los estudios de validación genética, como el presente, contribuirán a mejorar la tasa de éxito de los ensayos clínicos posteriores”, ha señalado Ryan Au Yeung Shiu-lun, investigador en la Universidad de Hong Kong.
Referencia científica: Luo S, et al. Effects of putative metformin targets on phenotypic age and leukocyte telomere length: a mendelian randomisation study using data from the UK Biobank. Lancet Healthy Longev. 2023 Jul;4(7):e337-e344. doi: http://dx.doi.org/10.1016/S2666-7568(23)00085-5
Fuente: HKU MED. HKUMed finds metformin could promote healthy ageing based on genetics. https://sph.hku.hk/en/News-And-Events/Press-Releases/2023/HKUMed-finds-metformin-could-promote-healthy-ageing-based-on-genetics
24/08/2023 (Genotipia) tomado- Noticias de investigación- Envejecimiento y Longevidad Copyright 2023 © Genotipia
sep
2
La identificación, en población africana, de una variante genética humana asociada a una menor carga del VIH, abre nuevas vías de investigación de tratamientos para la infección por VIH.
 Con más de 37 millones de infectados en todo el mundo, el Virus de la Inmunodeficiencia Humana (VIH) sigue siendo un importante problema de salud. En los últimos años, el desarrollo de tratamientos, especialmente las terapias antirretrovirales, han mejorado notablemente el control de la enfermedad causada por el virus. No obstante, todavía no existe una cura definitiva, cada año siguen infectándose alrededor de millón y medio de personas y no todas ellas responden de forma igual al tratamiento, con aparición de resistencia en algunas de ellas.
Con más de 37 millones de infectados en todo el mundo, el Virus de la Inmunodeficiencia Humana (VIH) sigue siendo un importante problema de salud. En los últimos años, el desarrollo de tratamientos, especialmente las terapias antirretrovirales, han mejorado notablemente el control de la enfermedad causada por el virus. No obstante, todavía no existe una cura definitiva, cada año siguen infectándose alrededor de millón y medio de personas y no todas ellas responden de forma igual al tratamiento, con aparición de resistencia en algunas de ellas.
Para identificar nuevas estrategias con las que hacer frente al VIH, un equipo internacional de investigadores ha recurrido al análisis del genoma de 3879 personas de ascendencia africana con infección por VIH, con resultados muy prometedores, publicados en la revista Nature. El equipo ha identificado una variante genética que abre una vía de investigación sobre un nuevo mecanismo para controlar el virus y desarrollar tratamientos frente al mismo.
Nueva variante genética que influye en la replicación del VIH
Estudios genómicos previos habían revelado genes relacionados con el control del VIH. No obstante, en su mayoría se trataba de estudios en población europea y se tenía poca información del impacto de la variación genética en el control de la infección por parte del VIH en población africana.
Los investigadores analizaron el genoma de los 7879 participantes del estudio (de diferentes poblaciones africanas, y afectados por el VIH) en relación con la carga del virus presente en cada uno. Estudiar la carga viral, que representa la cantidad de virus presente en el cuerpo de un individuo infectado, es relevante porque correlaciona fuertemente con la progresión y la probabilidad de transmitir la infección. Es una medida de la forma en la que una persona controla el VIH de forma espontánea.
Además de una variante ya conocida, localizada en el gen HLA-B, el equipo identificó una variante genética en la región del gen CHD1L asociada a una menor carga viral.
CHD1L codifica para una proteína implicada en la reparación del ADN. De momento, los estudios experimentales con diversos tipos de células inmunitarias realizados por los investigadores apuntan a que pueda tener un papel en la replicación del VIH en algunas células. En estos estudios la inactivación de CHD1L derivaba en un aumento de la replicación del virus y la posterior expresión del gen disminuía los niveles del virus. No obstante, el papel exacto de CHD1L y de la variante identificada respecto a la infección por VIH se desconoce y serán necesarias nuevas investigaciones.
“Este gen parece ser importante para controlar la carga viral en personas de ascendencia africana”, ha destacado Harriet Groom, investigadora en la Universidad de Cambridge y una de las directoras del estudio. “Aunque aún no sabemos cómo lo hace, cada vez que descubrimos algo nuevo sobre el control del VIH, aprendemos algo nuevo sobre el virus y algo nuevo sobre la célula. La conexión entre la replicación del VIH en los macrófagos y la carga viral es particularmente interesante e inesperada”.
Una variante de origen africano con relevancia para todas las poblaciones
El trabajo muestra la utilidad de extender los estudios genómicos a otras poblaciones, especialmente la población Africana, que por su diversidad genética ofrece un buen potencial para el descubrimiento genético.
En el caso del virus VIH, este análisis es especialmente importante, ya que pese a representar una buena parte de la población humana afectada por el virus, se han realizado menos estudios genéticos en población africana. Esta situación, que refleja las desigualdades sanitarias a nivel global, también supone una pérdida de oportunidades para identificar nuevos mecanismos relacionados con la enfermedad.
“Nuestros resultados subrayan la importancia de realizar estudios genómicos en poblaciones ancestrales diversas para abordar mejor sus necesidades médicas específicas y las desigualdades en la salud global”, ha indicado Jacques Fellay, investigador de la Escuela Politécnica Federal de Lausanne que ha participado en el estudio.
Al identificar una posible vía de control del VIH, los resultados del trabajo tienen implicaciones para todas las poblaciones. Entender mejor el mecanismo mediado por CHD1L podría ser clave para el desarrollo de terapias para todas las personas infectadas con el VIH.
“Caracterizar al detalle todas las variables genéticas que permiten un mejor control de la infección por VIH permite disponer de nuevas dianas terapéuticas y tener diferentes flancos desde los que atacar el virus”, ha señalado Josep Maria Miró, Consultor Senior del Servicio de Enfermedades Infecciosas del Clínic Barcelona, jefe de grupo del IDIBAPS y del CIBERINFEC y catedrático de Medicina en la Universidad de Barcelona que haparticipado en el estudio.
Artículo científico: McLaren, P.J., Porreca, I., Iaconis, G. et al. Africa-specific human genetic variation near CHD1L associates with HIV-1 load. Nature. 2023. https://doi.org/10.1038/s41586-023-06370-4
Referencia
McLaren PJ, Porreca I, Iaconis G, Ping Mok H, MukhopadhyayS, et al. Africa-specific human genetic variation near CHD1L associates with HIV-1 load. Nature 620, 1025–1030 (2023). https://doi.org/10.1038/s41586-023-06370-4
31/08/2023(genotipia) Tomado- Noticias de investigación Microbiología Molecular Copyright 2023 © Genotipia

