feb
12
 El Ministerio de Salud de Rusia comunicó hoy que autorizó al Centro Nacional de Investigación Médica Oncológica Blojín el uso de Neovac-RONTs, una vacuna de ARNm personalizada de producción nacional para el tratamiento del melanoma.
El Ministerio de Salud de Rusia comunicó hoy que autorizó al Centro Nacional de Investigación Médica Oncológica Blojín el uso de Neovac-RONTs, una vacuna de ARNm personalizada de producción nacional para el tratamiento del melanoma.
El servicio de prensa de la cartera sanitaria emitió un comunicado donde explica que el fármaco se elaborará de forma individualizada para cada paciente, a partir de compuestos sintetizados sobre la base de los resultados de los estudios genéticos del material extraído, y se aplicará tras la extirpación quirúrgica de las metástasis.
«Se administrará como terapia adyuvante después de la cirugía en pacientes adultos de 18 años o más con melanoma cutáneo en estadio IIB-IV (una vez extirpadas todas las lesiones metastásicas), en combinación con un inhibidor de PD-1», precisó la entidad de Salud.
En ese contexto, detalló el organismo que, en los últimos años, Rusia ha intensificado el desarrollo de medicamentos de nueva generación, incluyendo vacunas contra el cáncer, basadas en la tecnología de ARNm (ARN mensajero), considerada una de las líneas terapéuticas más prometedoras.
El Ministerio añadió que el ARNm es un ácido ribonucleico que transfiere la información genética desde el ADN del núcleo celular a los ribosomas en el citoplasma.
La principal ventaja de este fármaco, desarrollado por el Centro Nacional de Investigación de Epidemiología y Microbiología Gamaleya y el de Investigación Radiológica Médica, reside en su carácter personalizado, enfatizó.
“A partir del análisis genético del tumor de cada paciente, se genera una vacuna única capaz de ‘enseñar’ al sistema inmunitario a reconocer las células cancerosas”, argumentó el ente sanitario.
Los primeros tres prototipos de vacunas experimentales de ARNm contra el cáncer fueron presentados en diciembre de 2025 por el Centro Gamaleya.
En medio de esta nueva innovación científica, el director general del Centro Nacional de Investigación Médica de Radiología del Ministerio de Salud, Andréi Kaprin, informó que el desarrollo de cada dosis personalizada tiene un costo de 300 mil rublos (unos 3.900 dólares) para el Estado, aunque los pacientes la recibirán de forma gratuita.
12 febrero 2026 | Fuente: Prensa Latina | Tomado del sitio web | Noticia
ene
30
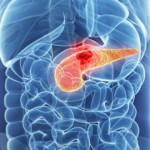 El equipo de Mariano Barbacid, del Centro Nacional de Investigaciones Oncológicas (CNIO), ha eliminado en ratones el cáncer de páncreas más común, el adenocarcinoma ductal, y lo ha hecho, con una terapia combinada de tres fármacos que evita la aparición de resistencias y que no tiene efectos secundarios importantes.
El equipo de Mariano Barbacid, del Centro Nacional de Investigaciones Oncológicas (CNIO), ha eliminado en ratones el cáncer de páncreas más común, el adenocarcinoma ductal, y lo ha hecho, con una terapia combinada de tres fármacos que evita la aparición de resistencias y que no tiene efectos secundarios importantes.
La terapia, la primera lograr la curación completa en modelos experimentales, ha sido diseñada por las científicas del CNIO Vasiliki Liaki y Sara Barrambana -primeras autoras del estudio- y por Carmen Guerra, coautora principal del estudio que se ha publicado en la revista PNAS.
Presentación de los resultados del estudio
El director del Grupo de Oncología Experimental del CNIO y presidente de honor científico de la Fundación CRIS Contra el Cáncer, ha presentado los resultados del estudio en una rueda de prensa junto la investigadora Carmen Guerra, a la presidenta de la Fundación, Lola Manterola, y a la soprano y paciente de cáncer de páncreas, Cristina Domínguez.
El adenocarcinoma ductal de páncreas -el tipo más habitual de cáncer de páncreas y el de peor pronóstico- suele diagnosticarse demasiado tarde, por lo que apenas un 5 % de los pacientes sobrevive más allá de los 5 años.
Cada año se diagnostican en España más de 10 300 nuevos casos de este cáncer que carece de terapias específicas.
«Desde 1981, cuando todavía no se conocían las bases moleculares del cáncer se ha avanzado mucho», ha explicado Barbacid.
«En el caso del páncreas, lo conocemos muy bien pero todavía no podemos hacer nada más allá de la quimioterapia actual, que desgraciadamente no sirve para muchos pacientes».
La mutación que inicia el cáncer de páncreas es el oncogén KRAS y aunque ya existen fármacos que bloquean la acción de KRAS, su eficacia es limitada porque al cabo de unos meses el tumor se vuelve resistente al tratamiento.
Atacar tres puntos claves de los mecanismos del tumor
Sin embargo, frente a las monoterapias que inhiben KRAS, la estrategia del grupo de Barbacid consiste en atacar tres puntos claves de los mecanismos del tumor: las proteínas KRAS, EGFR y STAT3, que actúan como motores de crecimiento del cáncer y que además causan las resistencia.
El equipo probó la triple terapia en 18 ratones a los que se les implantó las células cancerígenas de seis pacientes y 200 días después de finalizar el tratamiento, 16 continuaban vivos, libres de enfermedad y sin sufrir efectos secundarios adversos.
Un largo camino
Pero para llegar hasta ahí, el camino fue largo. En 2019, el equipo del CNIO logró suprimir el cáncer en ratones eliminando dos dianas EGFR y RAF1 pero «con varios peros», entre ellos, que «solo la mitad de los tumores respondieron, que eran relativamente pequeños para lo que puede aguantar un ratón y cuando los tumores superaban los 100 m3 ninguno respondió», ha recordado el investigador.
Durante seis años más, el equipo buscó dianas adicionales y descubrió STAT3, implicado en múltiples procesos celulares como la proliferación, la supervivencia o la inflamación. El equipo del CNIO probó entonces una terapia triple dirigida contra STAT3, EGFR y RAF1 y logró que durante el tiempo del estudio los ratones estuvieran 300 días libres de tumor «aproximadamente la mitad de lo que vive un ratón», ha apuntado Barbacid.
Para ello, el equipo combinó daraxonrasib -un inhibidor de KRAS diseñado por la empresa estadounidense Revolution Medicines que aún no ha sido aprobado por la FDA americana-, afatinib, un fármaco aprobado para ciertos tipos de cáncer de pulmón y el degradador de proteínas SD36.
La hoja de ruta
A partir de ahora, ha explicado Barbacid, «nuestra hoja de ruta» será seguir investigando para mejorar la terapia y ampliarla a otros modelos de ratón con otras alteraciones genéticas, estudiar las metástasis derivadas de estos tumores para identificar con precisión los pacientes que podrían beneficiarse de la nueva estrategia terapéutica, y analizar «con detalle» su efecto en el microambiente tumoral.
Para ello, Barbacid ha hecho un llamamiento a los cirujanos y patólogos de los hospitales para que envíen al CNIO muestras de pacientes con las que poder realizar todas estas investigaciones porque «nos queda mucho por hacer».
27 enero 2026 | Fuente: EFE | Tomado de | Noticia
ene
29
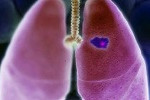 Partículas finas procedentes de la contaminación atmosférica aumentan el riesgo de todos los subtipos del cáncer, mientras que el dióxido de nitrógeno (NO2), el ozono (O3) y el dióxido de azufre (SO2) se relacionan con el de pulmón no microcítico, indica un estudio publicado hoy en Environmental Pollution.
Partículas finas procedentes de la contaminación atmosférica aumentan el riesgo de todos los subtipos del cáncer, mientras que el dióxido de nitrógeno (NO2), el ozono (O3) y el dióxido de azufre (SO2) se relacionan con el de pulmón no microcítico, indica un estudio publicado hoy en Environmental Pollution.
El cáncer de pulmón se clasifica principalmente en dos grandes tipos, el E más común es el cáncer de pulmón no microcítico, que incluye el adenocarcinoma, el carcinoma escamoso y el carcinoma de células grandes.
Estos subtipos se diferencian por el tipo de células afectadas y por su localización dentro del pulmón, y representan la mayoría de los diagnósticos.
El segundo gran tipo es el cáncer de pulmón microcítico, menos frecuente pero más agresivo, que tiene una fuerte relación con el tabaquismo.
Varios estudios señalan a la contaminación del aire exterior, especialmente la exposición a partículas finas en suspensión (PM2,5), como un carcinógeno para el cáncer de pulmón —es decir, un agente capaz de causar este cáncer.
Sin embargo, no se conoce del todo cómo influye en la incidencia de los distintos subtipos del cáncer, ni si afecta a cómo éste evoluciona después del diagnóstico. En concreto, se han realizado pocos estudios sobre el impacto de la contaminación atmosférica en la supervivencia al cáncer de pulmón, y este estudio aporta información valiosa en este ámbito, detallan los autores.
Para llegar a estos resultados, fueron incluidos en el estudio más de 122 000 personas de la cohorte estadounidense Cancer Prevention Study-II (CPS-II), de la American Cancer Society, a partir de 1992.
Los participantes actualizaron cada dos años sus datos personales y diagnósticos de cáncer hasta 2017. Para cada participante se estimó su exposición anual a distintos contaminantes: partículas finas PM2,5, PM10, ozono (O3), dióxido de azufre (SO2), dióxido de nitrógeno (NO2) y monóxido de carbono (CO).
El análisis tuvo en cuenta la variación de la exposición a lo largo del tiempo y ajustó los resultados por múltiples factores individuales, incluido un historial de tabaquismo. Entre 1992 y 2017, se detectaron 4 282 casos de cáncer de pulmón en esta cohorte.
El dióxido de nitrógeno mostró una relación más fuerte con el adenocarcinoma, el subtipo más frecuente de cáncer de pulmón, subraya el texto.
“Utilizamos datos nacionales de calidad del aire combinados con información satelital y del uso del suelo”, explica Ryan Diver, investigador en ISGlobal y primer autor del estudio. “Así, pudimos relacionar la exposición a la contaminación con el riesgo de desarrollar diferentes subtipos de cáncer de pulmón, además de la supervivencia tras el diagnóstico en subgrupos específicos de pacientes”.
El estudio confirmó que la exposición a partículas finas (PM2,5) aumenta el riesgo de desarrollar cáncer de pulmón, y que este efecto se observa de forma similar en todos los subtipos histológicos, incluidos el adenocarcinoma, el carcinoma de células escamosas y el carcinoma de células grandes, explicaron.
27 enero 2026 | Fuente: Prensa Latina | Tomado de | Noticia
ene
29
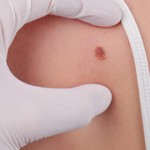 Los diagnósticos de cáncer de piel en Brasil aumentaron 17 veces en una década, al pasar de 4 237 casos en 2014 a 72 728 en 2024, según datos difundidos hoy. De acuerdo con la información difundida por la Sociedad Brasileña de Dermatología (SBD), ese incremento refleja mejoras en los registros sanitarios, pero también factores estructurales como mayor exposición solar, envejecimiento poblacional y desigualdades históricas en el acceso a la atención médica.
Los diagnósticos de cáncer de piel en Brasil aumentaron 17 veces en una década, al pasar de 4 237 casos en 2014 a 72 728 en 2024, según datos difundidos hoy. De acuerdo con la información difundida por la Sociedad Brasileña de Dermatología (SBD), ese incremento refleja mejoras en los registros sanitarios, pero también factores estructurales como mayor exposición solar, envejecimiento poblacional y desigualdades históricas en el acceso a la atención médica.
El mapa de la enfermedad muestra un patrón regional marcado: los estados del Sur y del Sudeste concentran las tasas más altas, con Espírito Santo a la cabeza con 139,37 casos por 100 000 habitantes, seguido por Santa Catarina (95,65).
Para la SBD, el crecimiento responde a una combinación de mayor radiación solar acumulada, predominio de población de piel clara en determinadas zonas y aumento de la expectativa de vida.
A ello se suma, desde 2018, la exigencia de completar el Cartón Nacional de Salud y la Clasificación Internacional de Enfermedades en las biopsias, lo que fortaleció la vigilancia epidemiológica y redujo subregistros históricos.
En el Norte y Nordeste del país, aunque las tasas siguen siendo más bajas, la entidad advierte que persisten subnotificaciones, especialmente en áreas rurales y de difícil acceso.
Según reporta la Agencia Brasil, en estados como Roraima, Acre y Amapá, el aumento reciente puede indicar avances en la detección, pero también revela fragilidades del sistema en territorios periféricos.
Las brechas de acceso al sistema de salud inciden de forma directa en el diagnóstico precoz, pues datos de la SBD indican que los usuarios del Sistema Único de Salud (SUS) enfrentan 2,6 veces más dificultades para conseguir consultas con dermatólogos que quienes cuentan con planes privados.
De igual forma, estados como Sao Paulo, Minas Gerais y Río Grande do Sul concentran la mayoría de los centros oncológicos especializados, mientras que Acre, Amazonas y Amapá cuentan con apenas una unidad cada uno y carecen de centros de referencia.
En consecuencia, los tiempos entre diagnóstico e inicio del tratamiento varían: en el Sur y Sudeste suelen ser menores a 30 días, mientras que en el Norte y Nordeste superan con frecuencia los 60 días.
26 enero 2026 | Fuente: Prensa Latina | Tomado de | Noticia
ene
20
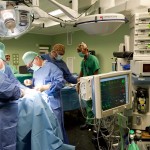 Cirujanos del dispensario oncológico regional de la provincia rusa de Sverdlovsk, en los Urales, extirparon un tumor de más de 60 kilogramos a un hombre de 50 años, informó hoy el Ministerio de Salud regional.
Cirujanos del dispensario oncológico regional de la provincia rusa de Sverdlovsk, en los Urales, extirparon un tumor de más de 60 kilogramos a un hombre de 50 años, informó hoy el Ministerio de Salud regional.
«Los médicos del dispensario oncológico regional de Sverdlovsk extirparon exitosamente un tumor gigante de más de 60 kilogramos a un paciente de 50 años, que lo había desarrollado durante casi dos décadas», precisó el comunicado oficial.
La cartera sanitaria explicó que «el abdomen del hombre creció durante unos 20 años» sin generar sospechas de peligro para la vida.
«La barriga comenzó a crecerme a los 33 años, hasta los 50 no me molestó, podía correr tranquilo, tenía fuerza, no interfería en el trabajo. Después de los 50 años se volvió pesado. Tras los exámenes se descubrió un tumor grande», relató el paciente, citado por la institución.
La masa, identificada como un liposarcoma, un tumor maligno del tejido adiposo, ocupaba prácticamente toda la cavidad abdominal, comprimiendo la vena cava inferior y desplazando completamente los intestinos, la vejiga y otros órganos, en un caso único para los oncólogos locales en sus 30 años de práctica.
Un equipo quirúrgico de ocho especialistas realizó la intervención durante casi ocho horas, logrando remover la gigantesca formación que, debido a su crecimiento inicial lento y asintomático, había pasado inadvertida como una amenaza vital durante años hasta volverse físicamente incapacitante.
16 enero 2026 | Fuente: Prensa Latina | Tomado de | Noticia
ene
7
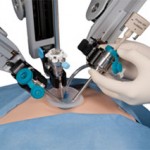 La primera cirugía robótica del mundo para la extracción de un tumor agresivo al final de la tráquea con un único orificio y con el paciente sin intubar se ha realizado esta semana en el hospital Ruber Internacional (Madrid) a un paciente venezolano que viajó a España gracias a la Fundación “González Rivas”, del cirujano torácico Diego González.
La primera cirugía robótica del mundo para la extracción de un tumor agresivo al final de la tráquea con un único orificio y con el paciente sin intubar se ha realizado esta semana en el hospital Ruber Internacional (Madrid) a un paciente venezolano que viajó a España gracias a la Fundación “González Rivas”, del cirujano torácico Diego González.
En una entrevista con EFE, González Rivas, que ha liderado la cirugía, explica que el tumor se encontraba «en la peor localización posible» en la carina (el final de la tráquea donde se bifurcan los bronquios), pero lo que convierte la operación en pionera en el mundo es que el robot Da Vinci ha utilizado una única incisión (en el tórax de 4 centímetros) y durante el proceso operatorio el paciente ha respirado por sí mismo, sin necesidad de una máquina.
González, que preside esta fundación que tiene por objetivo llevar la cirugía mínimamente invasiva a países en desarrollo, subraya que se trata de una intervención curativa con buenas expectativas.
La intervención en el Ruber tuvo lugar este lunes y se prolongó durante cinco horas y media, con resultado satisfactorio.
Cirugía de riesgo
No obstante, González Rivas admite que, aún saliendo bien, es una cirugía de riesgo ya que puede haber complicaciones posoperatorias.
Se trata de un cáncer escamoso situado en la parte final de la tráquea que, en este caso, invade el bronquio derecho y parte del izquierdo: «Lo que se hace en la intervención es cortar la tráquea y reconstruir la carina sin quitar nada de pulmón».
«Estamos yendo a un sitio donde una complicación da poco margen ya que es el tubo que da la respiración a los pulmones. Tratamos el tronco donde se conectan los pulmones, no quitamos el pulmón pero sí la conexión. Si falla, la complicación es severa».
González Rivas precisa que se trata de un tumor extremadamente raro. Un cirujano torácico puede ver uno o dos así en toda su vida, aunque en el Shanghái Pulmonary Hospital, donde opera habitualmente, llegan más casos al ser centro de referencia.
Lo que valora el equipo médico (tres cirujanos torácicos, dos anestesistas y tres enfermeros) es que sin esta operación, el paciente hubiera fallecido en unos meses por muerte súbita.
Y es que el tamaño del tumor es de dos centímetros, prácticamente iguala el ancho de la tráquea.
Otros dos cirujanos han participado: el venezolano Regulo Ávila, que trabaja desde hace años con González Rivas, y el rumano Mugurel Bosinceanu.
En declaraciones a EFE, Regulo Ávila, cirujano torácico del hospital Ruber Internacional, insiste en la importancia de que la operación se realice a través de un único orificio por donde pasan hasta tres brazos del robot Da Vinci: «Se han hecho operaciones con cinco incisiones, pero jamás con una».
González Rivas, con amplia experiencia, pone en valor a su fundación que no solo opera en países en vías de desarrollo, también empieza a hacerlo en España gracias, en esta ocasión, al Ruber Internacional, que asume el coste médico.
En ocho días se planificó
Pavler Carpio, de 66 años, llegó al hospital Ruber Internacional el 25 de diciembre. Lo hizo en avión, procedente de Venezuela, vía Colombia, por los problemas de cierre del espacio aéreo, con un diagnóstico que conoció hace unos meses tras una tomografía en su país, donde el tumor se consideró inoperable.
Carpio contó con la colaboración de su hija, la ginecóloga venezolana Sol Carpio que, a través de Instagram, contactó con el doctor González Rivas.
«En 24 horas me llamó y en ocho días se planificó la operación», dice satisfecha la hija, inmensamente agradecida a la fundación y al equipo que ha operado a su padre.
La hija de Carpio también pone en valor el libro de González Rivas ‘Curando el mundo’, donde enseña su técnica mínimamente invasiva para operaciones de pulmón (ha intervenido a más de 7 000 pacientes de 129 países). Ahora da un paso más.
01 enero 2025 | Fuente: EFE | Tomado de | Noticia

