may
13
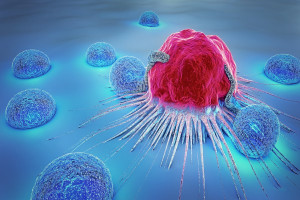
El cáncer de páncreas es uno de los tumores más letales. La tasa de supervivencia al adenocarcinoma ductal de páncreas, la forma más frecuente de la enfermedad, se sitúa en un 8,6%, el porcentaje más bajo de todos los tumores comunes, según datos de la Sociedad Española de Oncología Médica.
A pesar de los avances en la investigación sobre este tipo de cáncer hay muchas incógnitas por responder. La mayoría de las veces se diagnostica cuando ya está en fases avanzadas. La última novedad reseñable la firma un equipo que ha conseguido revelar por qué se inicia la mecha de este tipo de cáncer. Los detalles del proceso se publican en el último número de la revista Science.
Es conocido que en los tumores de páncreas, como en otros tipos de cáncer, son claves las mutaciones en el oncogén KRAS. El equipo que ahora publica novedades sobre la enfermedad, formado por investigadores del Memorial Sloan Kettering Cancer Centre (MSKCC), de Nueva York, y la investigadora Direna Alonso-Curbelo, que ahora trabaja en el Instituto de Investigación Biomédica de Barcelona (IRB), también demostró anteriormente el papel inductor que cumplen en el desencadenamiento de la enfermedad factores externos como por ejemplo, una lesión en el tejido que provoque inflamación. Ahora, los científicos han demostrado que para el proceso también es fundamental la identidad celular, la capacidad de algunas células para responder a la influencia de los oncogenes y la inflamación.
Las interacciones entre mutaciones genéticas y factores externos, subrayan los investigadores, modifican la identidad de algunas subpoblaciones de células, las transforman. Y, como consecuencia de esto, la capacidad de estas células para comunicarse e interactuar con otras células de su entorno aumenta enormemente, lo que contribuye a favorecer el desarrollo del cáncer.
Alta plasticidad
Concretamente, los científicos han demostrado que en el páncreas existen subpoblaciones de células diversas que tienen una alta plasticidad y responden mucho más a los factores genéticos y no genéticos que predisponen al cáncer. Según sus datos, esas células tienen, por un lado, un epigenoma diferente y específico; y, por otro, una capacidad incrementada para poder responder y mandar señales a su entorno.
Impulsadas por la influencia de las mutaciones y la inflamación, esas células generan redes de comunicación aberrante, provocando un bucle de retroalimentación que conduce al desarrollo y progresión del cáncer.
En modelos de ratón, el equipo demostró que era posible bloquear la citada comunicación aberrante y que esas conversaciones entre células cumplían un papel fundamental en el desarrollo del cáncer. «Nuestros análisis demostraron que estas redes de comunicación expansivas que se establecen en las fases iniciales del cáncer de páncreas son funcionalmente relevantes y dirigen la tumorigénesis pancreática en ratones», señala Alonso-Curbelo.
Métodos computacionales
Así, la investigación combinó sofisticados modelos de ratón genéticamente modificados y métodos computacionales avanzados para mapear los distintos estados celulares que conducen al cáncer y desentrañar las características de las subpoblaciones de células individuales del páncreas en cada fase de la progresión del tumor.
El área computacional de la investigación ha estado dirigida por Cassandra Burdziak, estudiante de doctorado en el laboratorio de la doctora Pe’er, en el MSKCC; mientras que la parte experimental y conceptual ha sido liderada por la propia Alonso-Curbelo, que inició la investigación durante su estancia en la institución neoyorkina.
El hallazgo coincide en su publicación con otro artículo que aparece esta semana en Nature donde se han mostrado resultados prometedores de una vacuna experimental basada en tecnología de ARN mensajero, la misma que se utilizó en las vacunas contra la covid-19, contra el cáncer de páncreas más agresivo.
Los resultados de un ensayo clínico en fase I realizado en 16 pacientes, muestran que las vacunas, personalizadas, son capaces de inducir una respuesta inmunitaria contra el cáncer.
Los primeros resultados del estudio han demostrado que la vacuna induce respuesta inmunitaria sustancial y retrasa potencialmente la recaída de los pacientes en una forma de cáncer, ya que se elaboraron con neoantígenos identificados en sus propios tumores. El tratamiento se administró en combinación con quimioterapia e inmunoterapia.
Mayo 12/2023 (Diario Médico) – Tomado de Oncología – Identidad celular Copyright Junio 2018 Unidad Editorial Revistas, S.L.U.
may
12
Las metástasis son más parecidas desde el punto de vista genómico a los tumores primarios de lo que inicialmente se habría podido esperar, al menos, en algunos tipos de cáncer. De esta forma parece reforzarse la idea de que el microambiente tumoral tiene un protagonismo importante en el desarrollo metastásico.
Es una de las conclusiones de dos estudios importantes publicados en Nature y Nature Genetics, en los que también se ha constatado que los tumores muestran alteraciones de escape al sistema inmunitario ya desde estadios muy tempranos.
Así lo señala Francisco Martínez Jiménez, primer autor de ambos estudios que ha desarrollado en el Centro de Medicina Molecular de la Universidad de Utrecht, y es actualmente jefe del Grupo de Inmunogenómica Computacional del Vall d’Hebron Instituto de Oncología (VHIO), que forma parte del Campus Vall d’Hebron, además de ser líder de la unidad de Minados de Datos de la Fundación Médica Hartwig.
A pesar de los muchos esfuerzos por comprender la contribución de los cambios genómicos al desarrollo de metástasis, el conocimiento sobre esta cuestión es aún limitado, de ahí la importancia de caracterizar las diferencias genómicas entre los cánceres primarios y metastásicos y cuantificar su impacto en la resistencia a las terapias «para poder comprender y aprovechar las intervenciones terapéuticas que establecen terapias más efectivas y personalizadas”, explica Francisco Martínez.
Para afrontar estas preguntas, investigadores del Centro de Medicina Molecular e Instituto Oncode de la Universidad de Utrecht y la Fundación Médica Hartwig han generado el mayor conjunto de datos armonizados de secuenciación completa de genomas de tumores de pacientes con cáncer. Este conjunto de datos abarca más de 7.000 muestras de tumores primarios y metastásicos no apareados de 71 tipos de cáncer, incluidos 23 tipos de cáncer con una gran representación en ambos estadios clínicos.
Una de las observaciones relevantes de los estudios ahora publicados es que las diferencias entre los tumores primarios y metastásicos dependen en gran medida del tipo de tumor. «En algunos tipos de tumores como por ejemplo el de páncreas las diferencias genómicas entre los tumores primarios y metastásicos son sutiles. En cambio, en otros como próstata, tiroides y algunos tipos de cáncer de mama hay diferencias genómicas muy importantes”, explica este investigador.
Papel del microambiente
Dicho esto los estudios liderados por Francisco Martínez constatan «a gran escala una tendencia dominante en el campo de la investigación de la metástasis, como es que su proceso de generación no puede ser explicado por una alteración genómica específica sino por un proceso evolutivo en el que posiblemente juegue un papel muy relevante la interacción de las células tumorales con el microambiente que rodea al tumor”.
No obstante, estos estudios sí han permitido la identificación de un conjunto de alteraciones genómicas enriquecidas en los tumores metastáticos y que podrían estar asociadas a la adquisición de resistencia a determinadas tratamientos contra el cáncer. “Es un primer paso importante, pero se necesitan estudios clínicos dedicados para validar su relevancia clínica en pacientes”, explica el jefe del Grupo de Inmunogenómica Computacional del VHIO.
Capacidad de escape al sistema inmune
En paralelo, los investigadores han estudiado cómo los tumores son capaces de escapar de la vigilancia impuesta por el sistema inmune en distintas fases de la enfermedad. Esta capacidad de escape a menudo involucra alteraciones genómicas específicas del tumor en las vías relacionadas con el sistema inmunitario.
“Sabemos que los tumores tienen la capacidad de ser invisibles al sistema inmune, pero queríamos comprender qué alteraciones genómicas le confieren esta capacidad y cómo de frecuentemente las detectamos en distintos tipos de cáncer y en distintas fases de la evolución tumoral”, señala Francisco Martínez.
Y los resultados de este análisis han revelado que uno de cada cuatro pacientes tiene alteraciones genómicas en el tumor directamente asociadas con el escape del reconocimiento del sistema inmunitario. Sin embargo, los investigadores han vuelto a constatar diferencias sustanciales entre distintos tipos de cáncer. Mientras que, en algunos, como en carcinoma cervical, más de la mitad de los pacientes tienen estas alteraciones, en otros la prevalencia es prácticamente nula.
Tumores primarios y metastáticos
Una observación llamativa a partir de la comparación entre tumores primarios y metastáticos es que apenas existen diferencias entre ambas etapas, ni en la frecuencia ni el tipo de alteraciones de escape del sistema inmune observadas. “Esto nos lleva a pensar que la mayoría de los tumores probablemente adquieren la capacidad de evadir el sistema inmune en etapas muy tempranas de su evolución”, explica Francisco Martínez.
Otro hallazgo relevante es que el tipo y la frecuencia de alteraciones genéticas de escape está directamente relacionada con la cantidad de mutaciones que presenta el tumor, de modo que en aquellos con poca carga de mutaciones prácticamente no se observan alteraciones genéticas de escape, mientras que en aquellos con carga mutacional media y alta se observan frecuentemente alteraciones que parcialmente truncan el reconocimiento por parte del sistema inmunitario.
Y tumores con carga mutacional muy alta (comúnmente denominados como hipermutados o ultrahipermutados) presentan un tipo de alteraciones muy específicas que tienden a truncar completamente el reconocimiento por parte del sistema inmunitario.
“Ahora que tenemos una idea más completa del panorama de alteraciones genéticas de escape que hacen al tumor invisible al sistema inmune, el siguiente paso es investigar si estas alteraciones tienen una influencia en la respuesta tratamiento de inmunoterapia”, avanza el jefe del Grupo de Inmunogenómica Computacional del VHIO.
Mayo 12/2023 (Diario Médico) – Tomado de Oncología – ‘Nature’ y ‘Nature Genetics’ Copyright Junio 2018 Unidad Editorial Revistas, S.L.U. Todos los derechos reservados.
may
12
Un tratamiento contra el cáncer que se enfoca en tumores sólidos y estimula el sistema inmunitario se ha mostrado seguro en humanos y se puede combinar con inmunoterapias aprobadas para mejorar sus efectos, según los resultados de un primer ensayo en humanos llevado sobre 115 pacientes con cánceres avanzados.
El régimen combinado también ha mostrado signos prometedores de activación inmunitaria, lo que podría mejorar potencialmente las respuestas al tratamiento en personas con cánceres metastásicos que normalmente no responden a la inmunoterapia, según los datos publicado en el último Science Translational Medicine.
Los anticuerpos anti-PD-L1 y otras inmunoterapias contra el cáncer funcionan activando las células T del sistema inmune que combaten el cáncer. Sin embargo, muchos pacientes no responden a las terapias con inhibidores de puntos de control inmunitarios, también llamados check-points, lo que pone de relieve la necesidad de desarrollar estrategias de tratamiento más eficaces.
Un enfoque potencial implica el uso de agentes coestimuladores, proteínas que añaden un ‘plus’ a los tratamientos de inmunoterapia, como el coordinado por especialistas del Cancer Center Clínica Universidad de Navarra, junto con la compañía farmacéutica Roche. Es un estudio pionero de inmunoterapia en pacientes con tumores sólidos avanzados, en el que se ha ensayado la nueva proteína de activación dirigida 4-1BB (RO7122290) usando otra proteína (FAP) como diana. Los resultados citados en la publicación anteriormente mencionada muestran su capacidad de estimular la respuesta inmune antitumoral en este tipo de tratamientos.
La molécula ensayada en pacientes es producto de las investigaciones del Centro de Innovación de Roche en sus sedes de Suiza, Reino Unido y Alemania, coordinadas por Pablo Umaña.
En el ensayo clínico participaron 115 pacientes que recibieron dosis semanales intravenosas de esta terapia como agente único o en combinación con atezolizumab en cinco hospitales españoles.
En el artículo se pone de manifiesto que actualmente más del 80% de los pacientes no responden adecuadamente o muestran resistencia a la inmunoterapia con anticuerpos monoclonales inmunomoduladores. Por ello, este equipo investigador ha activado el receptor 4-1BB como opción terapéutica, ya que su «actividad coestimuladora para la respuesta inmunitaria antitumoral constituye uno de los principales mecanismos en investigación para incrementar la eficacia de los tratamientos», señala Ignacio Melero, codirector de Inmunología e Inmunoterapia en la Clínica Universidad de Navarra y en el Cima de la misma universidad, que ha sido uno de los investigadores principales de este ensayo.
Aumentar las respuestas
La estimulación de este receptor en los pacientes ha mostrado una mayor proliferación de células T y una formación de memoria, longevidad y citotoxicidad de estas células, lo que aumenta la inmunidad antitumoral de estos pacientes.
En este primer estudio en fase clínica de escalada de dosis se ha evaluado la seguridad, tolerabilidad y actividad antitumoral preliminar en pacientes con tumores sólidos avanzados o metastásicos con resultados que han llevado a este agente biespecífico a ensayos fase 1b-2 actualmente en curso. Melero destaca, de hecho, que la portada de la publicación representa imágenes de microscopia que demuestran, en biopsias seriadas, «cómo el tratamiento incrementa muy notoriamente en los tumores la densidad de células inmunitarias con capacidad para destruirlo».
El investigador indica a Diario Médico que en este ensayo clínico se han probado tanto el agente nuevo biespecífico como la combinación de este con el anticuerpo anti-PD-L1 atezolizumab, observándose que ejerce «funciones que incrementan el infiltrado de linfocitos T intratumorales y su grado de activación en ambas circunstancias en un número limitado de pacientes tratados previamente con múltiples líneas. Se ha observado actividad de control del crecimiento tumoral y, en algunos casos, respuestas objetivas».
En este ensayo clínico, los investigadores han probado, por tanto, el agente coestimulador biespecífico llamado RO7122290, que reconoce la proteína de activación de fibroblastos-α (FAP) para atacar el tumor sólido y también funciona como un agonista 4-1BB para activar las células T. Han participado 115 pacientes con tumores avanzados o metastásicos, de los cuales 65 recibieron dosis semanales de RO7122290 y 50 recibieron el compuesto junto con el anticuerpo anti-PD-L1 aprobado atezolizumab.
Los ensayos, indica Melero, se han llevado a cabo en la población habitual de los ensayos fase 1: pacientes sin otra alternativa de tratamiento, todavía con buen estado general y, generalmente, después de haber recibido varias líneas terapéuticas a las que la enfermedad ha progresado. «Aún no está enfocado a un tipo de tratamiento de tumor, aspecto que precisamente constituye el objetivo de los ensayos fase 2 que es están realizando ahora».
Hace 25 años, el equipo ya demostró, en ensayos con ratón, que este receptor 4-1BB aumentaba la respuesta inmunitara frente al cáncer, hecho que en estos momentos se está explotando en distintas estrategias, sobre todo en combinación.
Mayo 11/2023 (Diario Médico) – Tomado de Oncología – Ensayo multicéntrico en ‘Science Translational Medicine’ Copyright Junio 2018 Unidad Editorial Revistas, S.L.U. Todos los derechos reservados.
may
11
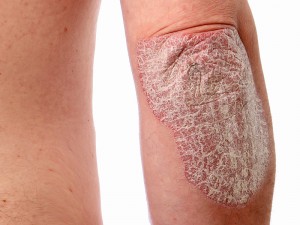
Trece hospitales de la Comunidad Valenciana están inmersos en un estudio multidisciplinar que pretende evaluar la adherencia, eficacia y persistencia de los tratamientos biológicos prescritos a pacientes con psoriasis moderada-grave en seguimiento durante un año. Para ello, los tres investigadores principales, Raul Ferrando, jefe del Servicio de Farmacia del Hospital General Universitario de Castellón; Antonio Martorell, jefe de Dermatología del Hospital de Manises, de Valencia, y Joaquín Borrás, farmacéutico de la Unidad de Pacientes Externos del Hospital de Sagunt, de Valencia, pensaron que, para facilitar el registro de datos clínicos, farmacoterapéuticos y de calidad de vida era necesario crear una app. Pero no una aplicación cualquiera sino una que permitiera que el farmacéutico, el dermatólogo y el paciente pudieran introducir datos, cada uno en su campo. Y así lo hicieron y la han llamado PsorUp, ya disponible en IOS y Android, y es de registro solo para los investigadores y pacientes incluidos en el ensayo.
Para aclarar conceptos, Ferrando recuerda a CF que la adherencia es cuando «el paciente se toma la medicación de forma adecuada». Esto está directamente asociado a la eficacia, pues «hay una evidencia clara de que, si un paciente es adherente, la eficacia del tratamiento es mayor y, como consecuencia de esa eficacia, el tratamiento se mantiene en el tiempo sin cambios, que es la persistencia», explica.
«Esta trilogía era lo que pretendíamos valorar en los tratamientos biológicos de la psoriasis moderada-grave -prosigue- y pensamos que eso se podía gestar de una manera más fácil con la creación de una app, que nos permitiera obtener esos datos e implicar a todos los participantes en este acto sanitario, que son el dermatólogo, el farmacéutico hospitalario y el paciente».
Así, el dermatólogo introduce todos los datos clínicos del paciente y el seguimiento de los resultados de salud a través de las escalas de psoriasis. «Hablamos de datos relacionados con el diagnóstico de la enfermedad, qué tratamientos ha llevado, qué es lo que se prescribe, cómo se encuentra el paciente, cuáles son sus escalas de valoración clínica, si el paciente va mejor o peor… Y son datos que actualiza en las sucesivas visitas que tenga con el paciente».
El farmacéutico, por su parte, registra los tratamientos que se le da y dónde se administra, «ya que puede ser en el hospital, en consulta o se la puede administrar el propio paciente…», aclara. La fecha de recogida y cómo será la recogida, entre otros datos relacionados con la adherencia, haciendo test de Morisky Green. Además, se le pregunta si se le olvida alguna vez o si tiene algún problema.
El paciente también cuenta en esta app, pues, al inicio y en cada una de las visitas siguientes, va introduciendo datos sobre cómo se encuentra, siguiendo escalas de calidad de vida. «Es lo que se conoce como PRO (resultados en salud percibidos por el paciente). Le preguntamos por su calidad de vida, si la psoriasis le está afectando en su día a día, si tiene molestias o picor… Todo vinculado a su percepción, no a la del médico, que él ya pone la suya. Y es que, el clínico puede ver que no hay una afectación cutánea en el cuerpo, pero el paciente puede percibir que no está bien, ya sea emocionalmente o físicamente, y esto hay que alinearlo para ver si los resultados del tratamiento están siendo óptimos».
Según Ferrando, «la potencia de la app radica en la suma de toda esta información» y lo que la diferencia respecto a otras es que «la van a tocar todos: el dermatólogo, el farmacéutico y el paciente, que la van a nutrir de información». A lo que Martorell añade: «A día de hoy no existe una aplicación como el modelo PsorUp, que ponga al paciente en el centro del proceso, lo que permitirá incrementar su proactividad, dándole el papel protagonista que siempre debe de tener». Es más, asegura que «PsorUp es la primera app incluida en las tiendas de IOS y Google a nivel global enfocada a mejorar conocimientos de la adherencia terapéutica de los pacientes con psoriasis incluidos en un proyecto de investigación». Asimismo, califica de «hito colaborativo» que el contenido de la app se haya preparado de forma conjunta por dermatólogos y farmacéuticos hospitalarios de varios centros de la Comunidad Valenciana.
El farmacéutico especialista concreta que los investigadores harán un seguimiento de un año, en función de las visitas programadas por el dermatólogo. En cada una de ellas se hará el registro de datos por parte de los implicados.
Al final de la investigación, verán si la app ha servido para recoger todos los datos y si les ha permitido hacer un seguimiento de la adherencia, la persistencia y la evaluación de los resultados en salud.
Mayo 11/2023 (Diario Médico) – Tomado de Farmacia Hospitalaria – En investigación Copyright Junio 2018 Unidad Editorial Revistas, S.L.U. Todos los derechos reservados.
may
10
Utilizando un vector de confirmación de procesos, los investigadores desarrollaron y optimizaron un método de cromatografía de exclusión por tamaño (SEC) con UV y dispersión multiángulo de la luz (MALS) para medir el nivel de cápsides vacías durante la fabricación. En un nuevo estudio, los investigadores demostraron que la SEC-MALS superaba a otros métodos analíticos y se correlacionaba bien con los valores de ultracentrifugación analítica de la velocidad de sedimentación (SV-AUC) de partículas llenas-vacías. El estudio se publica en la revista Human Gene Therapy.
Las capacidades analíticas deben poder cuantificar los niveles de cápsides vacías y llenas en los virus adenoasociados (AAV) fabricados durante el desarrollo de la terapia génica en fase preclínica.
Bryan Troxell, de StrideBio, y sus coautores, demostraron que el SEC-MALS era lineal, exacto y preciso, al tiempo que cumplía las recomendaciones de control de calidad de la cromatografía. Además, en comparación con otros ensayos indicadores de estabilidad, el SEC-MALS tuvo un rendimiento similar al de la PCR digital de gotitas, el ensayo inmunoenzimático de cápsides y los ensayos de infectividad en estudios de estrés acelerado.
«Los datos confirman que la SEC-MALS es una técnica analítica sólida para el avance de los programas de terapia génica«, afirman los investigadores.
«Cada vez está más claro que las cápsides vacías de los vectores representan contaminantes indeseables en los productos de terapia génica AAV de grado preclínico y clínico», afirma el Editor Jefe Terence R. Flotte, MD, Catedrático Celia e Isaac Haidak de Educación Médica y Decano, Rector y Vicerrector Ejecutivo de la Facultad de Medicina Chan de la Universidad de Massachusetts. «La capacidad de medir con precisión el nivel de estos contaminantes es un paso importante para mejorar la calidad y consistencia de estos productos».
Mayo 10/2023 (MedicalXpress) – Tomado de Genetics Copyright Medical Xpress 2011 – 2023 powered by Science X Network.
Traducción realizada con la versión gratuita del traductor www.DeepL.com/Translator
may
10
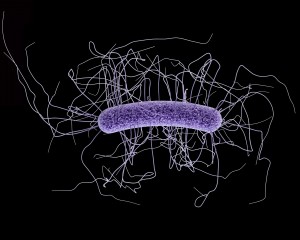
Un equipo de bioquímicos de la Universidad de Notre Dame ha hallado una posible nueva forma de tratar a los pacientes infectados por Clostridium difficile, un tipo de bacteria que causa graves problemas gastrointestinales. En su estudio, publicado en Proceedings of the National Academy of Sciences, el grupo buscó en bases de datos médicas moléculas antibacterianas que pudieran funcionar mejor en pacientes con infecciones por C. difficile.
Las infecciones por C. difficile pueden provocar desde pequeñas molestias hasta episodios potencialmente mortales: cada año mueren unas 13.000 personas. Una vez infectados (muy a menudo mientras están hospitalizados por otra causa), los pacientes suelen recibir un antibiótico para tratar la infección. Desgraciadamente, los antibióticos son cada vez menos eficaces a medida que C. difficile desarrolla resistencias.
Actualmente sólo se utiliza uno: la vancomicina. Otro problema es que C. difficile produce esporas que no son eliminadas por el antibiótico, lo que significa que muchas personas sufren reinfecciones. La vancomicina no funciona bien en estos pacientes, y menos aún en infecciones posteriores. Por estas razones, el equipo de Indiana se propuso encontrar un tratamiento más eficaz para estas infecciones.
El trabajo consistió en buscar en bases de datos antibacterianas moléculas que se sabe que se unen a una proteína específica asociada a C. difficile. Así se llegó a dos compuestos: los oxadiazoles 1 y 2. Las pruebas in vitro demostraron que ambos eran eficaces para eliminar la C. difficile cuando se administraban a la misma dosis que la vancomicina.
A continuación, el equipo comprobó la rapidez con la que se absorbían en el torrente sanguíneo si se administraban por vía oral. El oxadiazol 1 se absorbía con rapidez, lo que lo hacía inadecuado para combatir las bacterias intestinales. En cambio, el oxadiazol 2 se absorbía lentamente, lo que lo convertía en el candidato ideal para una nueva terapia contra las infecciones por C. difficile. En ratones, previno la muerte un 30% mejor que la vancomicina.
El estudio también descubrió que el oxadiazol 2 ayudaba a prevenir la pérdida de peso mejor que la vancomicina. Y lo mejor de todo es que las pruebas fecales no mostraron indicios de esporas: tras tres semanas de pruebas, ninguno de los ratones presentaba reinfecciones.
Mayo 10/2023 (MedicalXpress) – Tomado de Medications – Gastroenterology Copyright Medical Xpress 2011 – 2023 powered by Science X Network.
Traducción realizada con la versión gratuita del traductor www.DeepL.com/Translator