may
13
Según un estudio presentado en el 25º Congreso Europeo de Endocrinología, celebrado en Estambul, unos niveles elevados de cortisol, la hormona del estrés, durante el tercer trimestre del embarazo pueden mejorar el habla y el lenguaje en los tres primeros años de vida del niño. Los resultados ayudan a los investigadores a comprender mejor el papel del cortisol en el desarrollo tanto fetal como infantil.
El desarrollo del lenguaje durante la primera infancia puede indicar lo bien que se desarrolló el sistema nervioso del bebé en el útero. La exposición prenatal al cortisol -una hormona esteroidea que ayuda al organismo a responder al estrés- dirige el crecimiento del feto y también afecta a su desarrollo cerebral. Sin embargo, aún se desconocen los efectos del cortisol en el desarrollo temprano del lenguaje.
En este estudio, investigadores del Hospital Universitario de Odense analizaron datos sobre los niveles de cortisol de 1.093 mujeres danesas durante su tercer trimestre de embarazo y sobre las habilidades del habla y el lenguaje de 1.093 niños daneses de entre 12 y 37 meses, procedentes de la Cohorte Infantil de Odense. Descubrieron que los niños expuestos a altos niveles de cortisol en el útero podían decir más palabras entre los 12 y los 37 meses, mientras que las niñas comprendían mejor más palabras entre los 12 y los 21 meses.
«Que sepamos, éste es el primer estudio que investiga la relación entre los niveles de cortisol materno y el desarrollo del lenguaje en los niños a lo largo del tiempo, teniendo en cuenta también el sexo del niño y el nivel educativo de la madre», afirma la Dra. Anja Fenger Dreyer, que participó en el estudio.
Y añade: «Hemos tenido acceso a una gran cohorte de estudio, métodos de análisis de alta calidad y covariables relevantes, lo que convierte nuestro estudio en una importante contribución a la comprensión fisiológica de la exposición prenatal al cortisol en la maduración fetal y el desarrollo infantil.»
El equipo evaluará a continuación si los niños expuestos a un cortisol elevado en el útero tienen más probabilidades de presentar puntuaciones más altas en el cociente intelectual (CI). Además de los datos sobre los niveles de cortisol materno y el desarrollo temprano del lenguaje, la cohorte infantil de Odense también dispone de datos sobre pruebas de inteligencia realizadas a niños de 7 años. «Se sabe que el desarrollo temprano del lenguaje en los niños predice la función cognitiva en etapas posteriores de la vida, como la atención, la memoria y el aprendizaje, por lo que queremos investigar si la exposición prenatal al cortisol también está asociada a las puntuaciones de CI de los niños de 7 años», afirma la Dra. Fenger Dreyer.
Mayo 13/2023 (EurekaAlert!) – Tomado de News Releases – Reports and Proceedings EUROPEAN SOCIETY OF ENDOCRINOLOGY Copyright 2023 by the American Association for the Advancement of Science (AAAS).
may
13
Un equipo de neurocientíficos de la Universidad Médica de Carolina del Sur (MUSC) ha identificado cambios en la actividad de unas células cerebrales conocidas como neuronas piramidales, que contribuyen a la búsqueda de drogas en un modelo preclínico de trastorno por consumo de opiáceos. Tras interrumpir el acceso a la heroína, estas neuronas se volvieron más excitables. La actividad de estas neuronas se normalizó bloqueando la enzima proteína cinasa A (PKA). La inhibición de esta enzima también redujo el comportamiento de búsqueda de opiáceos. La doctora Jacqueline McGinty, catedrática de Neurociencia, y el doctor Saurabh Kokane, becario postdoctoral en el laboratorio de McGinty, publicaron recientemente los hallazgos de su equipo en la revista Journal of Neuroscience.
El riesgo de sobredosis de opiáceos puede aumentar al volver a buscar y consumir drogas, o recaer, tras un periodo sin consumirlas, o de abstinencia.
«La prevención del retorno al consumo es la clave del éxito en el desarrollo de tratamientos eficaces para los trastornos por consumo de sustancias», afirma Kokane.
«Tras décadas de investigación sobre el trastorno por consumo de opiáceos, existen tres fármacos aprobados por la FDA, pero sólo reducen la gravedad de los síntomas de desintoxicación y no impiden la vuelta al consumo. Por lo tanto, existe una clara necesidad de más opciones de tratamiento», afirmó. «En la actualidad, carecemos de un conocimiento exhaustivo de los efectos de los opiáceos, como la heroína, sobre las neuronas que impulsan el retorno al consumo. Comprender mejor estos cambios puede conducir a opciones de tratamiento adicionales».
El laboratorio McGinty del MUSC identificó tipos específicos de neuronas piramidales que contribuyen a la recaída. Descubrieron que estas neuronas en una región específica del cerebro, la corteza prefrontal prelímbica, experimentan cambios moleculares y funcionales durante la abstinencia de heroína, un opioide de uso común, que alteran su función. El córtex prelimbico es una de las áreas del cerebro implicadas en la toma de decisiones y el control del comportamiento. Los opiáceos pueden alterar el funcionamiento normal de esta parte del cerebro y, en una persona con trastorno por consumo de opiáceos, esta interferencia puede conducir a la búsqueda compulsiva de drogas.
Es importante destacar que, en este estudio preclínico, los investigadores demuestran que la restauración de la función normal de estas neuronas mediante la inhibición de una enzima clave durante la abstinencia de heroína puede prevenir la búsqueda de drogas en un modelo de roedor.
Restablecer el control
Kokane y McGinty creen que el restablecimiento de la actividad normal en las neuronas del córtex prelímbico puede prevenir la recaída inducida por pistas, pero es necesario seguir investigando.
«Necesitamos comprender con más detalle los cambios que se producen en las neuronas durante la abstinencia de heroína y determinar cómo conducen a la recaída», afirma Kokane.
El estudio del MUSC también descubrió que en el córtex prelímbico, donde la abstinencia aumenta la actividad neuronal, el bloqueo local de la enzima PKA devolvía la actividad neuronal a niveles normales, estando más activa durante este proceso de abstinencia.
Este hallazgo condujo a los investigadores del MUSC a una nueva idea: Quizá la inhibición de la PKA podría restablecer el control.
«Cuando infundimos el inhibidor de la PKA en el córtex prelímbico durante la abstinencia de heroína, observamos una disminución de la recaída inducida por señales», afirma Kokane.
Al bloquear la PKA, los investigadores han descubierto una forma de restablecer el control del córtex prelímbico durante la abstinencia de opiáceos en un modelo de roedor. Y lo que es más importante, el restablecimiento del control en el cerebro también condujo a un mejor control conductual, ya que disminuyó la búsqueda de heroína.
«Nuestros hallazgos ofrecen una nueva diana molecular para el desarrollo de futuras farmacoterapias», afirma Kokane. «Estamos en una fase muy temprana de esta investigación, pero tiene potencial. Nuestros hallazgos sugieren que la investigación debería orientarse hacia el desarrollo de farmacoterapias que se dirijan específicamente a los cambios funcionales que se desarrollan durante la abstinencia de heroína en tipos concretos de neuronas, como los que identificamos en el córtex prelímbico.»
Hasta entonces, el equipo está entusiasmado por continuar su investigación preclínica para arrojar luz sobre el control prelímbico de la búsqueda de opiáceos y la recaída y descubrir objetivos adicionales.
«Es importante tener en cuenta que el cerebro se adapta constantemente al entorno y que los cambios que hemos documentado en el córtex prefrontal durante la abstinencia de heroína, aunque persistentes, no son necesariamente permanentes y pueden revertirse», afirma McGinty.
Mayo 13/2023 (MedicalXpress) – Tomado de Neuroscience – Addiction Copyright Medical Xpress 2011 – 2023 powered by Science X Network
may
13
Cáncer de cabeza y cuello (CCC) es un término genérico que engloba varios tipos de cáncer, entre ellos el más frecuente, el carcinoma de células escamosas de cabeza y cuello (CCECC). Los pacientes con CCC pueden ser tratados con una combinación de cirugía, radioterapia y/o quimioterapia. Sin embargo, el tratamiento no siempre es eficaz.
Rosemary Millen, primera autora compartida de un artículo publicado recientemente en la revista Med, explica: «Estos tratamientos provocan efectos secundarios graves, por lo que algunos pacientes no pueden terminarlos. Inclusive después de someterse a un tratamiento tan duro, el 60% de los pacientes recae». La limitada eficacia de los tratamientos podría explicarse en parte por el hecho de que la composición genética del tumor difiere mucho de un paciente a otro. En consecuencia, la terapia más adecuada es diferente para cada paciente.
«Los clínicos disponen actualmente de herramientas limitadas para distinguir adecuadamente este hecho. Por tanto, existe una necesidad urgente de mejores biomarcadores: indicadores que podamos medir en cada paciente individual para determinar de qué tratamiento se beneficiaría más. En el mejor de los casos, este enfoque personalizado evitaría sobrecargar innecesariamente a los pacientes con tratamientos que podrían no funcionar, y conduciría a un mejor pronóstico», explica Else Driehuis, autora correspondiente del artículo.
Creación de un biobanco
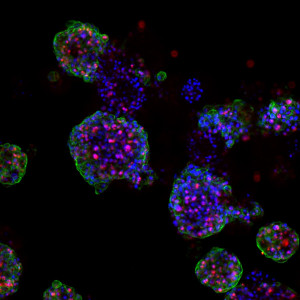
Un primer paso hacia esos tratamientos personalizados es desarrollar mejores modelos que reflejen con mayor precisión la variabilidad del tumor. Por ello, los investigadores crearon un biobanco de organoides de CCC: versiones en miniatura de tumores de pacientes cultivados en el laboratorio. Millen afirma: «En última instancia, el objetivo de este biobanco sería utilizar los organoides para guiar las decisiones de tratamiento personalizado en la clínica. Por supuesto, antes de poder hacerlo, primero necesitamos investigar si la respuesta al tratamiento en los organoides se correlaciona con la respuesta observada en los pacientes.»
El equipo pudo cultivar organoides de CCC a partir de los tejidos de los pacientes y confirmó que estos «mini tumores» se parecían mucho a los tumores de los pacientes, ya que conservaban las mismas características histológicas y genéticas. Millen afirma: «A continuación, tratamos los organoides con varios tipos de terapia y medimos la eficacia del tratamiento determinando cuántas células de los organoides morían. El siguiente paso fue correlacionar esto con la respuesta al tratamiento en los pacientes».
Comparación de organoides y pacientes
Tras tratar los organoides con radioterapia, el equipo demostró que la respuesta de los organoides se asemejaba a la de los pacientes. «Por tanto, los organoides tienen potencial para predecir los resultados en los pacientes. La correlación entre la respuesta de los organoides y la de los pacientes existía en los casos en que éstos recibían radioterapia adyuvante, es decir, se utilizaba radiación además de la resección quirúrgica del tumor. En los casos en que los pacientes recibieron radioterapia como tratamiento primario, tenemos que investigarlo más a fondo», explica Millen.
Los investigadores también estudiaron el efecto de la quimiorradioterapia, una combinación de radiación y quimioterapia. «Aquí demostramos que dos fármacos quimioterápicos específicos, el cisplatino y el carboplatino, tienen un efecto radiosensibilizador en los organoides. Esto significa que hacen que las células tumorales sean más sensibles a la radioterapia. Estos resultados son coherentes con lo que vemos en la clínica y, por tanto, subrayan de nuevo el potencial predictivo de los organoides en este escenario», afirma Driehuis.
Implicaciones clínicas
Algunos de los descubrimientos realizados por el equipo podrían tener implicaciones para los pacientes de CCC en un futuro próximo. Por ejemplo, demostraron que el fármaco cetuximab hacía que los organoides tumorales fueran menos sensibles a la radioterapia.
Driehuis explica: «Esto es sorprendente, porque la combinación de este fármaco y la radioterapia se administra a algunos pacientes de CCC en la clínica hoy en día. En los pacientes es difícil distinguir las contribuciones individuales del fármaco y la radioterapia al efecto global de este tratamiento combinado, pero en los organoides podemos separarlas».
«Nuestros resultados encajan con datos publicados recientemente que muestran que la supervivencia de los pacientes tratados con cetuximab y radioterapia es peor en comparación con el tratamiento con radioterapia sola. La implicación clínica de estos hallazgos sería que es mejor esperar con cetuximab hasta después de la radioterapia, pero este cambio en el momento del tratamiento es algo que habría que probar en los pacientes, por supuesto.»
El equipo también demostró que un inhibidor de la PRMT5, un nuevo fármaco que ya se está probando en ensayos clínicos para otros tipos de cáncer, podría ser eficaz en un subgrupo de pacientes con CCC.
Millen afirma: «Secuenciamos el ADN de los organoides para investigar la relación entre mutaciones genéticas específicas y la respuesta a los tratamientos. Al hacerlo, descubrimos que los tumores con pérdida del gen CDKN2A respondían al tratamiento con este nuevo fármaco. Sería muy interesante comprobar si este efecto se da también en los pacientes, sobre todo teniendo en cuenta que esta mutación está presente en más del 50% de los casos de CCECC.»
Driehuis concluye: «En conjunto, nuestros resultados ponen de relieve la relevancia clínica de los organoides derivados de tejido tumoral de pacientes. Uno de los próximos pasos sería diseñar un ensayo clínico, para utilizar realmente los organoides para guiar las decisiones de tratamiento en pacientes con CCC.»
Mayo 13/2023 (MedicalXpress) – Tomado de Oncology & Cancer – Biomedical technology Medical Xpress 2011 – 2023 powered by Science X Network.
may
13
El cáncer de páncreas es uno de los tumores más letales. La tasa de supervivencia al adenocarcinoma ductal de páncreas, la forma más frecuente de la enfermedad, se sitúa en un 8,6%, el porcentaje más bajo de todos los tumores comunes, según datos de la Sociedad Española de Oncología Médica.
A pesar de los avances en la investigación sobre este tipo de cáncer hay muchas incógnitas por responder. La mayoría de las veces se diagnostica cuando ya está en fases avanzadas. La última novedad reseñable la firma un equipo que ha conseguido revelar por qué se inicia la mecha de este tipo de cáncer. Los detalles del proceso se publican en el último número de la revista Science.
Es conocido que en los tumores de páncreas, como en otros tipos de cáncer, son claves las mutaciones en el oncogén KRAS. El equipo que ahora publica novedades sobre la enfermedad, formado por investigadores del Memorial Sloan Kettering Cancer Centre (MSKCC), de Nueva York, y la investigadora Direna Alonso-Curbelo, que ahora trabaja en el Instituto de Investigación Biomédica de Barcelona (IRB), también demostró anteriormente el papel inductor que cumplen en el desencadenamiento de la enfermedad factores externos como por ejemplo, una lesión en el tejido que provoque inflamación. Ahora, los científicos han demostrado que para el proceso también es fundamental la identidad celular, la capacidad de algunas células para responder a la influencia de los oncogenes y la inflamación.
Las interacciones entre mutaciones genéticas y factores externos, subrayan los investigadores, modifican la identidad de algunas subpoblaciones de células, las transforman. Y, como consecuencia de esto, la capacidad de estas células para comunicarse e interactuar con otras células de su entorno aumenta enormemente, lo que contribuye a favorecer el desarrollo del cáncer.
Alta plasticidad
Concretamente, los científicos han demostrado que en el páncreas existen subpoblaciones de células diversas que tienen una alta plasticidad y responden mucho más a los factores genéticos y no genéticos que predisponen al cáncer. Según sus datos, esas células tienen, por un lado, un epigenoma diferente y específico; y, por otro, una capacidad incrementada para poder responder y mandar señales a su entorno.
Impulsadas por la influencia de las mutaciones y la inflamación, esas células generan redes de comunicación aberrante, provocando un bucle de retroalimentación que conduce al desarrollo y progresión del cáncer.
En modelos de ratón, el equipo demostró que era posible bloquear la citada comunicación aberrante y que esas conversaciones entre células cumplían un papel fundamental en el desarrollo del cáncer. «Nuestros análisis demostraron que estas redes de comunicación expansivas que se establecen en las fases iniciales del cáncer de páncreas son funcionalmente relevantes y dirigen la tumorigénesis pancreática en ratones», señala Alonso-Curbelo.
Métodos computacionales
Así, la investigación combinó sofisticados modelos de ratón genéticamente modificados y métodos computacionales avanzados para mapear los distintos estados celulares que conducen al cáncer y desentrañar las características de las subpoblaciones de células individuales del páncreas en cada fase de la progresión del tumor.
El área computacional de la investigación ha estado dirigida por Cassandra Burdziak, estudiante de doctorado en el laboratorio de la doctora Pe’er, en el MSKCC; mientras que la parte experimental y conceptual ha sido liderada por la propia Alonso-Curbelo, que inició la investigación durante su estancia en la institución neoyorkina.
El hallazgo coincide en su publicación con otro artículo que aparece esta semana en Nature donde se han mostrado resultados prometedores de una vacuna experimental basada en tecnología de ARN mensajero, la misma que se utilizó en las vacunas contra la covid-19, contra el cáncer de páncreas más agresivo.
Los resultados de un ensayo clínico en fase I realizado en 16 pacientes, muestran que las vacunas, personalizadas, son capaces de inducir una respuesta inmunitaria contra el cáncer.
Los primeros resultados del estudio han demostrado que la vacuna induce respuesta inmunitaria sustancial y retrasa potencialmente la recaída de los pacientes en una forma de cáncer, ya que se elaboraron con neoantígenos identificados en sus propios tumores. El tratamiento se administró en combinación con quimioterapia e inmunoterapia.
Mayo 12/2023 (Diario Médico) – Tomado de Oncología – Identidad celular Copyright Junio 2018 Unidad Editorial Revistas, S.L.U.
may
13
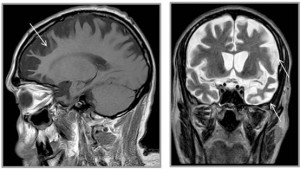
La tomografía por emisión de positrones (PET) de amiloide, muy usada en investigación, tiene también utilidad diagnóstica en pacientes con pérdida de memoria, algo que habían apuntado ya estudios previos pero que ahora se ha confirmado con un ensayo clínico controlado y aleatorizado llamado Estudio de Diagnóstico y Gestión del Paciente de Amypad (Amypad-DPMS), en el que, por parte española, ha participado el Barcelonaβeta Brain Research Center (BBRC), centro de investigación de la Fundación Pasqual Maragall.
Según ha informado hoy el BBRC, el estudio muestra un diagnóstico de alta certeza en el 40% de los pacientes dentro de los tres meses de la visita inicial a la clínica. «Esto corresponde a un porcentaje 3,5 veces superior a pacientes en los que no se habían realizado la PET de amiloide. Además, la PET de amiloide cambió el diagnóstico inicial en el 44% de los casos, frente a solo el 11% en el grupo sin esta prueba».
Para todas las fases de la enfermedad
El estudio, publicado en JAMA Neurology, muestra además que la utilidad diagnóstica de la PET de amiloide se observó «consistentemente» en pacientes beneficiados por la evaluación de biomarcadores (con un deterioro cognitivo leve) y también en los que estaban en una etapa temprana de disfunción clínica, que experimentaban solo quejas cognitivas subjetivas, y en los que ya se hallaban en una etapa tardía de la enfermedad, con demencia.
«Este nuevo ensayo clínico proporciona evidencias sólidas que respaldan la implementación temprana de esta prueba, ya que su uso está asociado a diagnósticos certeros», según Giovanni B. Frisoni, director del Centro de la Memoria del Hospital Universitario de Ginebra e investigador principal del estudio.
«Un diagnóstico seguro y de confianza es fundamental para la eficacia de las terapias modificadoras de la enfermedad, especialmente fármacos antiamiloide, cuya efectividad podría disminuir con el avance de la enfermedad», añade.
Juan Domingo Gispert, responsable del Grupo de Investigación en Neuroimagen del BBRC, que ha liderado la participación del centro en Amypad, ha explicado a este diario, por su parte, que el 40% es «bajo» -«en realidad se buscaba un nivel de certeza muy alto, del 90%»- pero es “reproducible” y está en línea con la dificultad de diagnóstico etiológico que de por sí tienen en enfermedades como el Alzheimer.
Lo que la PET de amiloide permite ver es la presencia o no de placas de la proteína beta amiloide en el cerebro. Si las hay, la prueba es positiva, y si no las hay, negativa. «Esto funciona muy bien en el entorno clínico», asegura el experto.
El resultado de la PET de amiloide es especialmente relevante ante personas con demencia atípica como pueden ser los jóvenes, indica Domingo. También dice que esta tecnología ofrece resultados similares a los de la punción lumbar para el diagnóstico del Alzheimer, que es algo que ya destacó un metaanálisis de 2018. No obstante, destaca que la PET de amiloide resultaría más cara que la punción lumbar y estaría menos accesible para todos los pacientes candidatos a un estudio de imagen con ella.
Para este estudio participaron 844 pacientes de ocho unidades o clínicas de memoria europeos. «Se trata de un estudio prospectivo, multicéntrico, aleatorizado y controlado, y es el más grande de Europa para evaluar el impacto clínico de esta herramienta de diagnóstico en participantes de clínicas de memoria», subraya Daniele Altomare, investigador postdoctoral senior y coordinador del estudio en el Laboratorio de Neuroimagen del Envejecimiento en la Universidad de Ginebra y primer autor del trabajo.
Entre los pacientes reclutados, 794 realizaron la visita a los tres meses y, por lo tanto, fueron considerados para el análisis del resultado principal; algunos experimentaban deterioro cognitivo subjetivo y mayor riesgo de enfermedad de Alzheimer preclínica (239), mientras que otros mostraban deterioro cognitivo leve (318) o demencia (237).
Mayo 12/2023 (Diario Médico) – Tomado de Radiodiagnóstico – Diagnóstico por la imagen Copyright Junio 2018 Unidad Editorial Revistas, S.L.U.
may
12
Las metástasis son más parecidas desde el punto de vista genómico a los tumores primarios de lo que inicialmente se habría podido esperar, al menos, en algunos tipos de cáncer. De esta forma parece reforzarse la idea de que el microambiente tumoral tiene un protagonismo importante en el desarrollo metastásico.
Es una de las conclusiones de dos estudios importantes publicados en Nature y Nature Genetics, en los que también se ha constatado que los tumores muestran alteraciones de escape al sistema inmunitario ya desde estadios muy tempranos.
Así lo señala Francisco Martínez Jiménez, primer autor de ambos estudios que ha desarrollado en el Centro de Medicina Molecular de la Universidad de Utrecht, y es actualmente jefe del Grupo de Inmunogenómica Computacional del Vall d’Hebron Instituto de Oncología (VHIO), que forma parte del Campus Vall d’Hebron, además de ser líder de la unidad de Minados de Datos de la Fundación Médica Hartwig.
A pesar de los muchos esfuerzos por comprender la contribución de los cambios genómicos al desarrollo de metástasis, el conocimiento sobre esta cuestión es aún limitado, de ahí la importancia de caracterizar las diferencias genómicas entre los cánceres primarios y metastásicos y cuantificar su impacto en la resistencia a las terapias «para poder comprender y aprovechar las intervenciones terapéuticas que establecen terapias más efectivas y personalizadas”, explica Francisco Martínez.
Para afrontar estas preguntas, investigadores del Centro de Medicina Molecular e Instituto Oncode de la Universidad de Utrecht y la Fundación Médica Hartwig han generado el mayor conjunto de datos armonizados de secuenciación completa de genomas de tumores de pacientes con cáncer. Este conjunto de datos abarca más de 7.000 muestras de tumores primarios y metastásicos no apareados de 71 tipos de cáncer, incluidos 23 tipos de cáncer con una gran representación en ambos estadios clínicos.
Una de las observaciones relevantes de los estudios ahora publicados es que las diferencias entre los tumores primarios y metastásicos dependen en gran medida del tipo de tumor. «En algunos tipos de tumores como por ejemplo el de páncreas las diferencias genómicas entre los tumores primarios y metastásicos son sutiles. En cambio, en otros como próstata, tiroides y algunos tipos de cáncer de mama hay diferencias genómicas muy importantes”, explica este investigador.
Papel del microambiente
Dicho esto los estudios liderados por Francisco Martínez constatan «a gran escala una tendencia dominante en el campo de la investigación de la metástasis, como es que su proceso de generación no puede ser explicado por una alteración genómica específica sino por un proceso evolutivo en el que posiblemente juegue un papel muy relevante la interacción de las células tumorales con el microambiente que rodea al tumor”.
No obstante, estos estudios sí han permitido la identificación de un conjunto de alteraciones genómicas enriquecidas en los tumores metastáticos y que podrían estar asociadas a la adquisición de resistencia a determinadas tratamientos contra el cáncer. “Es un primer paso importante, pero se necesitan estudios clínicos dedicados para validar su relevancia clínica en pacientes”, explica el jefe del Grupo de Inmunogenómica Computacional del VHIO.
Capacidad de escape al sistema inmune
En paralelo, los investigadores han estudiado cómo los tumores son capaces de escapar de la vigilancia impuesta por el sistema inmune en distintas fases de la enfermedad. Esta capacidad de escape a menudo involucra alteraciones genómicas específicas del tumor en las vías relacionadas con el sistema inmunitario.
“Sabemos que los tumores tienen la capacidad de ser invisibles al sistema inmune, pero queríamos comprender qué alteraciones genómicas le confieren esta capacidad y cómo de frecuentemente las detectamos en distintos tipos de cáncer y en distintas fases de la evolución tumoral”, señala Francisco Martínez.
Y los resultados de este análisis han revelado que uno de cada cuatro pacientes tiene alteraciones genómicas en el tumor directamente asociadas con el escape del reconocimiento del sistema inmunitario. Sin embargo, los investigadores han vuelto a constatar diferencias sustanciales entre distintos tipos de cáncer. Mientras que, en algunos, como en carcinoma cervical, más de la mitad de los pacientes tienen estas alteraciones, en otros la prevalencia es prácticamente nula.
Tumores primarios y metastáticos
Una observación llamativa a partir de la comparación entre tumores primarios y metastáticos es que apenas existen diferencias entre ambas etapas, ni en la frecuencia ni el tipo de alteraciones de escape del sistema inmune observadas. “Esto nos lleva a pensar que la mayoría de los tumores probablemente adquieren la capacidad de evadir el sistema inmune en etapas muy tempranas de su evolución”, explica Francisco Martínez.
Otro hallazgo relevante es que el tipo y la frecuencia de alteraciones genéticas de escape está directamente relacionada con la cantidad de mutaciones que presenta el tumor, de modo que en aquellos con poca carga de mutaciones prácticamente no se observan alteraciones genéticas de escape, mientras que en aquellos con carga mutacional media y alta se observan frecuentemente alteraciones que parcialmente truncan el reconocimiento por parte del sistema inmunitario.
Y tumores con carga mutacional muy alta (comúnmente denominados como hipermutados o ultrahipermutados) presentan un tipo de alteraciones muy específicas que tienden a truncar completamente el reconocimiento por parte del sistema inmunitario.
“Ahora que tenemos una idea más completa del panorama de alteraciones genéticas de escape que hacen al tumor invisible al sistema inmune, el siguiente paso es investigar si estas alteraciones tienen una influencia en la respuesta tratamiento de inmunoterapia”, avanza el jefe del Grupo de Inmunogenómica Computacional del VHIO.
Mayo 12/2023 (Diario Médico) – Tomado de Oncología – ‘Nature’ y ‘Nature Genetics’ Copyright Junio 2018 Unidad Editorial Revistas, S.L.U. Todos los derechos reservados.