may
20
 Nueve ciudades de Ecuador serán escenario hoy de caminatas para promover la lactancia materna en el país andino y se llevarán a cabo de forma simultánea.
Nueve ciudades de Ecuador serán escenario hoy de caminatas para promover la lactancia materna en el país andino y se llevarán a cabo de forma simultánea.
La iniciativa, promovida por la Secretaría Técnica Ecuador Crece Sin Desnutrición Infantil, se desarrolla en saludo al Día Mundial de la Lactancia Materna, que se conmemora el próximo martes.
Las caminatas se desarrollarán en las ciudades de Quito, Guayaquil, Guaranda, Puyo, Santo Domingo, Esmeraldas, Machala, Macas y Tena.
En estos espacios también habrá ferias de servicios del Gobierno Nacional y de los municipios. Estarán presentes el Ministerio de Salud, el Ministerio de Inclusión Económica y Social, entre otros.
Un 40,8 % de las mujeres embarazadas o madres conoce la importancia de la lactancia como uno de los principales beneficios para prevenir la desnutrición crónica infantil, según datos de la Organización Panamericana de la Salud.
También la Organización Mundial de la Salud considera que la lactancia materna prolongada reduce el riesgo de sobrepeso y obesidad en un 13 %, contribuye a combatir las enfermedades no transmisibles causadas por la obesidad y disminuye el riesgo de diabetes en 35 %.
18 mayo 2024|Fuente: Prensa Latina |Tomado de |Noticia
abr
3
 Puede ser un potencial preventivo de la leucemia linfoblástica aguda (LLA). No obstante, se debe profundizar en los mecanismos biológicos subyacentes.
Puede ser un potencial preventivo de la leucemia linfoblástica aguda (LLA). No obstante, se debe profundizar en los mecanismos biológicos subyacentes.
Se asocia una mayor duración de la lactancia materna exclusiva con un menor riesgo de cáncer infantil, incluida la leucemia linfoblástica aguda (LLA), ¿el cáncer más común en la infancia? La respuesta parece ser sí, según los datos de un último estudio que recoge JAMA.
Trabajos anteriores ya han sugerido que la lactancia materna protege contra los cánceres infantiles, en particular la leucemia linfoblástica aguda (LLA). Sin embargo, la evidencia proviene únicamente de estudios de casos y controles.
En este estudio de cohorte, la duración más prolongada de la lactancia materna exclusiva se ha asociado con un riesgo reducido de LLA-BCP infantil, (leucemia precursora de células B infantiles), «lo que corrobora los resultados de investigaciones previas de casos y controles en este campo. Sin embargo, para informar sobre futuras intervenciones preventivas, las siguientes investigaciones deberían centrarse en los posibles mecanismos biológicos subyacentes a la asociación observada», según la coordinadora del estudio, Signe Holst Søegaard, de la Sociedad Danesa del Cáncer en Copenhague, Dinamarca, y especialista en cáncer infantil y enfermedades infecciosas pediátricas.
Este trabajo ha investigado si la duración de la lactancia materna exclusiva se asocia con el riesgo de desarrollar leucemia linfoblástica aguda y otros cánceres infantiles. En concreto, los resultados de esta cohorte para LLA-BCP «se alinean con la reducción de aproximadamente un 30% del riesgo de LLA en niños amamantados exclusivamente durante al menos 4 meses frente a los que nunca fueron amamantados, en análisis conjuntos recientes de estudios internacionales de casos y controles que incluyeron a más de 10.000 niños con LLA», explica la coordinadora.
Datos del registro infantil de salud
En este estudio de cohorte poblacional que incluyó a 309.473 niños daneses, la lactancia materna exclusiva durante al menos 3 meses o más se asoció con un menor riesgo de cánceres hematológicos infantiles, particularmente LLA de precursores de células B, pero no con riesgo de tumores sólidos o del Sistema Nervioso Central (SNC), hecho que, según los autores, sugiere que «una duración más prolongada de la lactancia materna puede ser un factor potencial en la prevención de la LLA de precursores de células B infantil».
Para el análisis se incluyeron todos los niños nacidos en Dinamarca entre enero de 2005 y diciembre de 2018 con información disponible -del Registro Nacional de Salud Infantil de Dinamarca- sobre la duración de la lactancia materna exclusiva.
Se excluyeron niños en los que faltaba información sobre el peso al nacer, edad gestacional, edad y nivel educativo. Tampoco se incluyen niños con síndrome de Down debido a su mayor riesgo de leucemia con una biología distinta.
De los 309.473 niños analizados, 332 niños (el 0,1%) fueron diagnosticados con cáncer en edades comprendidas entre el año y los 14 años, con una edad media de 4 años en el momento del diagnóstico. De estos, 124 (un 37,3%) fueron diagnosticados con cánceres hematológicos (un 65,3% fueron LLA, de los cuales un 91,4% fueron LLA de precursores de células B). Un 13,3% presentaron tumores del SNC, un 24,1% tumores sólidos y un 25,3% presentó otras neoplasias no especificadas.
En comparación con la duración de la lactancia materna exclusiva de menos de 3 meses, la lactancia materna exclusiva durante 3 meses o más se asoció con un menor riesgo de cánceres hematológicos, lo que se atribuyó en gran medida a un menor riesgo de LLA-BCP, pero no con riesgo de tumores del SNC o tumores sólidos.
Mecanismos implicados
Sobre los mecanismos que establecen la potencial relación entre lactancia materna exclusiva y duradera y LLA infantil, la investigación detalla que los modelos actuales postulan que el desarrollo infantil de LLA-BCP comienza, a menudo, antes del nacimiento, cuando -y por razones desconocidas- un evento genético inicial da lugar a un clon preleucémico (como ETV6-RUNX1 ).
La prevalencia de la preleucemia en los recién nacidos es un aspecto que aún se debate, pero lo más probable es que la LLA-BCP se desarrolle solo en una pequeña proporción de niños nacidos con preleucemia”, explica Holst Søegaard, quien recuerda que durante mucho tiempo se ha especulado que, en estos niños, la transformación maligna de un clon preleucémico en LLA es desencadenada por una respuesta inmune desregulada a las infecciones.
Ver artículo: Bailey HD. Exploring Exclusive Breastfeeding and Childhood Cancer Using Linked Data. JAMA Netw Open[Internet]. 2024[citado 02 abr 2024];7(3): e243075. doi:10.1001/jamanetworkopen.2024.3075
02 abril 2024| Fuente: Diario Médico| Tomado de | Medicina| Ginecología y Obstetricia
oct
21
 Se describe el papel en la lactancia de una proteína que también es clave en el cáncer de mama.
Se describe el papel en la lactancia de una proteína que también es clave en el cáncer de mama.
La producción de leche en mamíferos es un proceso crucial para el organismo, perfeccionado a lo largo de la evolución. Los mecanismos moleculares que lo regulan son sofisticados, y se siguen investigando. Un nuevo estudio publicado en Nature Communications da un paso más para esclarecerlos, al profundizar en el papel de una proteína, RANK, que es esencial para el funcionamiento de las glándulas mamarias y también es clave en el cáncer de mama.
La producción de leche en mamíferos tiene lugar en el tejido epitelial mamario, formado por dos tipos principales de células: luminales y basales. Las luminales recubren la primera capa de los conductos mamarios y están implicadas en la generación en sí de la leche; las basales rodean a las luminales y originan la contracción que hace fluir la leche durante la lactancia.
Hay que tener en cuenta que los dos linajes de células, basales y luminales, proceden de las basales, que se diferencian en luminales en el embrión. Sin embargo, tras el nacimiento se especializan: las células basales solo generan basales y las luminales solo dan lugar a células luminales.
Una proteína implicada en el cáncer de mama
El nuevo estudio, dirigido por Eva González-Suárez, jefa del Grupo de Transformación y Metástasis del Centro Nacional de Investigaciones Oncológicas (CNIO), describe el comportamiento y la interacción de estos dos linajes celulares durante el embarazo y la lactancia y el papel de la proteína RANK.
Esta proteína centra el interés de González-Suárez desde que ella misma descubriera en 2010 que tiene un papel clave en el desarrollo del cáncer de mama. Actualmente el grupo cuenta con financiación del Consejo Europeo de Investigación (ERC) para desarrollar una nueva generación de fármacos contra el cáncer de mama dirigidos a bloquear la señalización a través de la proteína RANK.
La principal aportación del nuevo estudio ahora publicado, destaca González-Suárez, es «la creación de modelos animales con la proteína RANK eliminada solo en las células luminales o solo en las basales. Así se ha podido discriminar su función en cada tipo de células», algo que hasta ahora se desconocía.
El estudio muestra que las consecuencias de la eliminación de RANK sobre la funcionalidad de la glándula mamaria son distintas dependiendo de si las ratonas experimentan su primera gestación o la segunda, o si no han estado preñadas.
No hay leche en la primera gestación, pero sí en la segunda
Cuando se elimina RANK en las células luminales antes de que haya habido gestación, estas células empiezan a diferenciarse de forma aberrante en otras responsables de la fabricación de la leche en sí, llamadas alveolares. Pero la primera lactancia resulta fallida, porque estas células alveolares aberrantes no son capaces de producir leche.
En la segunda gestación las células luminales son aún más disfuncionales. Esto alerta a las células basales, que recuperan su capacidad de diferenciarse en células luminales alveolares, ahora sí competentes para producir leche. La lactancia, en esta segunda gestación, resulta por tanto exitosa. Es decir, gracias a esa «acción de rescate» de las células basales, que sí expresan RANK, tiene lugar una lactancia funcional. «Esa capacidad de bipotencia de las células basales es capaz de despertar en un contexto fisiológico, para restaurar un proceso tan importante como lactancia», explica González-Suárez.
Para la autora responsable del artículo «resulta muy interesante que, al no tener RANK, las células luminales se diferencien en alveolares de forma aberrante, incluso en ratones hembra que no han entrado aún en gestación. Y también es relevante esa diferencia entre lo que ocurre en la primera y la segunda gestación». En cuanto a la posibilidad de que estos procesos tengan un paralelismo en la lactancia humana, considera que «es probable, pero harían falta estudios para determinarlo».
Los coautores principales del artículo son la investigadora postdoctoral que co-lidera el estudio, Ana Sofía Rocha, del Instituto de Investigación Biomédica Bellvitge (IDIBELL), y Alejandro Collado-Solé, estudiante de doctorado en el Centro Nacional de Investigaciones Oncológicas (CNIO), ambos del grupo de Eva González-Suárez.
Referencia
Rocha AS, Collado-Sol, A, Graña-Castro O, Redondo Pedraza J, Soria Alcaide G, Cordero A, et al. Luminal Rank loss decreases cell fitness leading to basal cell bipotency in parous mammary glands. Nat Commun[Internet].2023[citado 20 oct 2023];14(1):6213. doi: 10.1038/s41467-023-41741-5.
21 octubre 2023 | Fuente: IMMedico| Tomado de Obstetricia y Ginecología
sep
15
 Un equipo de investigadoras del Vall d’Hebron Instituto de Oncología (VHIO) de Barcelona (España) ha comprobado que la leche materna contiene ADN de tumores de mama, lo que abre la puerta a que se pueda utilizar como una biopsia líquida para diagnosticar el cáncer en etapas tempranas.
Un equipo de investigadoras del Vall d’Hebron Instituto de Oncología (VHIO) de Barcelona (España) ha comprobado que la leche materna contiene ADN de tumores de mama, lo que abre la puerta a que se pueda utilizar como una biopsia líquida para diagnosticar el cáncer en etapas tempranas.
El estudio, publicado en la revista ‘Cancer Discovery’, parte de la preocupación de una paciente con cáncer de mama que temía haber transmitido la enfermedad a su bebé durante la lactancia, pues fue diagnosticada poco después de haber dejado de dar el pecho a su segunda hija y estando embarazada de su tercera. La jefa de la Unidad de Mama del Hospital Vall d’Hebron e investigadora del VHIO, Cristina Saura, ha explicado que esa paciente trajo una muestra de leche materna que tenía guardada en su congelador. ‘Si bien le dijimos que no había riesgo de transmitir el tumor, decidimos analizar la muestra a la búsqueda de marcadores que pudieran ayudarnos en la investigación’, ha relatado.
Las investigadoras observaron que, en esta bolsa, recogida unos 18 meses antes del diagnóstico, ya había ADN del tumor, conocido como ADN tumoral circulante (ADNct). Tirando del hilo, las investigadoras recogieron muestras de leche materna y sangre de más pacientes con cáncer de mama diagnosticadas durante el embarazo o el postparto, así como de mujeres sanas que estaban en curso de lactancia materna.
De 15 casos de mujeres con cáncer de mama ya diagnosticado durante el embarazo o en el postparto, en 13 de ellas se detectó en la leche la misma mutación que en el tumor que padecían; en cambio, en muestras de sangre solo una era positiva. ‘En tumores localizados, la liberación de ADN en la sangre es bajita y está muy diluido, pero en la lecha materna vemos que hay una cantidad más fácil de detectar, por lo que es una potencial herramienta de diagnóstico’, ha indicado Saura.
El siguiente paso es iniciar un estudio más amplio para recoger muestras de leche materna de 5 000 mujeres sanas a nivel mundial que se hayan quedado embarazadas con 40 años o más, o bien de cualquier edad que sean portadoras de mutaciones que aumentan su riesgo de padecer cáncer de mama (BRCA1, BRCA2, PALB2, RAD51C/D). El objetivo es corroborar si el cáncer de mama se puede detectar en una fase más temprana en la leche materna, incluso antes que mediante técnicas de imagen o analíticas de sangre.
Si los resultados son los esperados, Saura ha aventurado que se podría hacer un cribado a través de la leche materna a todas las mujeres después de dar a luz, al igual que se hace con los recién nacidos en la conocida como prueba del talón para detectar un grupo de enfermedades. ‘Pensamos que tendría utilidad, porque el cribado poblacional de cáncer de mama es a partir de los 50 años, mediante una mamografía, y esta nueva prueba se posicionaría en una población -más joven- en la que no estamos haciendo pruebas; y contra antes diagnostiquemos el cáncer, más posibilidad tenemos de curarlo’, ha subrayado.
Referencia
Saura S, Ortiz C, Matito J, Arenas JE, Suñol A, Martín A, et al. Early-Stage Breast Cancer Detection in Breast Milk. Cancer Discov 2023; https://doi.org/10.1158/2159-8290.CD-22-1340
Fuente: (Prensa Latina) – Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
ago
24
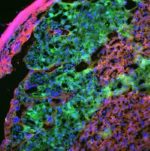 Investigadores de la Universidad de Cambridge han obtenido las primeras evidencias de que, durante el embarazo, el feto utiliza un gen paterno para controlar el suministro de nutrientes desde la placenta.
Investigadores de la Universidad de Cambridge han obtenido las primeras evidencias de que, durante el embarazo, el feto utiliza un gen paterno para controlar el suministro de nutrientes desde la placenta.
Durante el embarazo, el metabolismo materno se adapta para suministrar nutrientes que favorezcan el crecimiento y desarrollo fetal. La placenta, órgano temporal formado por células del feto y de la madre, actúa como intermediaria entre la madre y el feto y facilita el intercambio de nutrientes y oxígeno entre ambos. Conforme progresa el embarazo, el feto aumenta sus demandas de nutrientes para promover su crecimiento, lo que se opone, en cierto modo, a las necesidades maternas de mantener los nutrientes necesarios para su salud y prepararse para la lactancia y posibles posteriores embarazos.
A partir de estudios en ratones un equipo de la Universidad de Cambridge ha encontrado que IGF2, una señal endocrina similar a la insulina, modifica el metabolismo materno y distribución de recursos hacia el feto. Además, la señalización mediada por Igf2 participa en el desarrollo de diversos tejidos como la placenta, el hígado y el cerebro. En un estudio previo, el equipo había identificado el papel de IGF2 en el desarrollo de la vasculatura de la placenta para adaptarse al crecimiento del embrión.
Un gen de expresión paterna
Interesantemente, IGF2 está codificada por un gen con impronta genómica, de forma que únicamente la copia paterna está activa en la placenta. “Si la función de Igf2 del padre es inactivada en las células señalizadoras, la madre no produce suficiente cantidad de glucosa y lípidos disponible para su circulación”, señala Jorge Lopez-Tello, Investigador en el Departamento de Fisiología, Desarrollo y Neurociencia, así como primer firmante del trabajo, publicado en Cell Metabolism. “Por lo tanto, estos nutrientes llegan al feto en cantidades insuficientes y el feto no crece adecuadamente”.
Los investigadores plantean que la expresión de Igf2 con impronta genética en la placenta puede haber evolucionado como una estrategia para movilizar nutrientes hacia el feto en crecimiento. En este contexto, Igf2 y placenta tienen un papel central en el conflicto materno-fetal por los recursos maternos.
Impacto a largo plazo de los defectos en Igf2
Los investigadores también han determinado que la reducción en la señalización mediada por Igf2 en la placenta tiene consecuencias metabólicas postnatales. Los ratones deficientes para Igf2 mostraron un crecimiento restringido e hipoglucémico, con efectos que se extendieron a la edad adulta.
“Nuestra investigación pone de relieve lo importante que es la distribución controlada de nutrientes hacia el feto para la salud de la descendencia a lo largo de toda su vida, y el papel directo que desempeña la placenta”, ha señalado Amanda Sferruzzi, catedrática en Fisiología Fetal y de la Placenta en la Universidad de Cambridge. “La placenta es un órgano asombroso. Al final del embarazo, la madre expulsa la placenta, pero los recuerdos de cómo estaba funcionando la placenta dejan un legado duradero en la forma en que se han desarrollado los órganos fetales y en cómo van a funcionar a lo largo de la vida”.
El siguiente paso de los investigadores será determinar con mayor detalle cómo Igf2 controla las hormonas de la placenta implicadas en regulación de nutrientes y crecimiento de los órganos e identificar la función exacta de estas hormonas.
Fuente: Genética Médica News
Referencia: Lopez-Tello J, et al. Fetal manipulation of maternal metabolism is a critical function of the imprinted Igf2 gene. Cell Metab. 2023 Jul 11;35(7):1195-1208.e6. doi: http://dx.doi.org/10.1016/j.cmet.2023.06.007
https://www.sciencedirect.com/science/article/pii/S1550413123002176?via%3Dihub
ago
23
 Hace mucho tiempo que se sabe que la lactancia materna ayuda a mantener a los recién nacidos sanos y protegidos frente a diversas enfermedades. Pero ciertos azúcares presentes en la leche materna también podrían ayudar a prevenir infecciones antes del nacimiento del bebé. Los investigadores que publican informes en ACS Central Science han descubierto que estos azúcares pueden detener una infección prenatal habitual que afecta a los tejidos humanos y a ratones preñados. Esto podría ayudar a evitar partos prematuros u otras complicaciones sin necesidad de suministrar antibióticos en el futuro.
Hace mucho tiempo que se sabe que la lactancia materna ayuda a mantener a los recién nacidos sanos y protegidos frente a diversas enfermedades. Pero ciertos azúcares presentes en la leche materna también podrían ayudar a prevenir infecciones antes del nacimiento del bebé. Los investigadores que publican informes en ACS Central Science han descubierto que estos azúcares pueden detener una infección prenatal habitual que afecta a los tejidos humanos y a ratones preñados. Esto podría ayudar a evitar partos prematuros u otras complicaciones sin necesidad de suministrar antibióticos en el futuro.
Algunas bacterias que pueden afectar los embarazos de forma más frecuente son los estreptococos del grupo B (EGB). Las infecciones por EGB no tratadas pueden provocar efectos adversos, como neumonía neonatal o parto prematuro. Los tratamientos existentes se basan principalmente en antibióticos, que pueden dar lugar a cepas resistentes. Sin embargo, muchos de los compuestos ya presentes en la leche materna humana, como los oligosacáridos de la leche materna (HMO, por sus siglas en inglés), tienen efectos antibacterianos.
Steven Townsend, Jennifer Gaddy y sus colegas previamente exploraron los efectos antibacterianos de los HMO y descubrieron que podían inhibir el crecimiento de los EGB in vitro y en determinadas células reproductoras. Sin embargo, los investigadores debían demostrar cómo funcionan los azúcares en diferentes tejidos e in vivo antes de poder utilizar estos compuestos para potenciar los antibióticos existentes, o considerarlos como una nueva opción de tratamiento. Los investigadores pasaron entonces a estudiar la actividad de los HMO en las infecciones por EGB en ratones preñados y en tejidos humanos.
En primer lugar, analizaron los efectos protectores de los HMO en tejidos humanos infectados por EGB, utilizando tanto tejidos fetales vivos como un modelo organoide de la vagina. Al añadir un compuesto de HMO diseñado para imitar la composición de los azúcares de la leche materna, las bacterias no pudieron adherirse ni formar colonias.
A continuación, probaron el compuesto de HMO en ratones preñados infectados con EGB. Los ratones tratados presentaron un nivel de inflamación relativamente típico, cantidades reducidas de bacterias en distintos tejidos reproductivos y no hubo casos de partos prematuros, rotura de membranas ni muertes maternas. En su conjunto, estos resultados demuestran que los HMO pueden tener efectos antimicrobianos sin la administración de antibióticos adicionales. Los investigadores afirman que este trabajo podría permitir el uso de estos azúcares como opción viable de tratamiento para las infecciones por EGB y para prevenir resultados adversos en el embarazo.
Fuente: EurekaAlert
Referencia: Rebecca E. Moore, Sabrina K. Spicer, Jacky Lu, Schuyler A. Chambers, Kristen N. Noble, Jonathan Lochner, Rebecca C. Christofferson, Karla A. Vasco, Shannon D. Manning, Steven D. Townsend, and Jennifer A. Gaddy. The Utility of Human Milk Oligosaccharides against Group B Streptococcus Infections of Reproductive Tissues and Cognate Adverse Pregnancy Outcomes. ACS Central Science Article ASAP. Aug 2023. DOI: 10.1021/acscentsci.3c00101

