abr
17
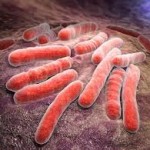 La tuberculosis (TB) sigue siendo hoy un importante problema de salud pública a nivel mundial, y la comunidad científica prosigue los estudios y ensayos para lograr más vacunas contra la enfermedad.
La tuberculosis (TB) sigue siendo hoy un importante problema de salud pública a nivel mundial, y la comunidad científica prosigue los estudios y ensayos para lograr más vacunas contra la enfermedad.
La vacuna BCG es actualmente la única autorizada contra la TB, y aunque es eficaz contra las formas graves en niños pequeños, no ofrece protección a adolescentes ni adultos.
El reto ahora de los científicos es lograr un inyectable que funcione en todas las edades, subraya un artículo publicado por la revista The British Medical Journal.
Un equipo de investigadores de la India evaluó dos nuevas vacunas contra la tuberculosis, denominadas VPM1002 e Immuvac.
Ambas –según la fuente- pueden proteger contra todas las formas de TB (pulmonar y extrapulmonar), prevenir la infección latente (inactiva) y generar una respuesta inmunitaria contra la bacteria que la provoca.
El Consejo Indio de Investigación Médica de Delhi aseguró que ellas para prevenir la TB son seguras en su uso en adultos y niños, pero no ofrecen protección contra todas las formas de la mencionada dolencia.
Los científicos explicaron que ninguno de los inyectables ofreció protección general contra la TB ni previno la infección latente por la misma.
Resaltaron que ambas demostraron la capacidad de prevenir la progresión a tuberculosis activa en aquellos que desarrollaron tuberculosis latente.
“Los investigadores descubrieron que, si bien ninguna de las dos vacunas demostró eficacia contra la tuberculosis total ni contra la tuberculosis pulmonar (TBP), una de ellas, la VPM1002, mostró eficacia de un 50,4 % contra la TBP en todos los grupos de edad, incluidos los de 36 a 60 años con un 79,5 %”, precisó el artículo.
Estos hallazgos –destacan los expertos- sugieren un beneficio potencialmente significativo para la salud pública, ya que la tuberculosis extrapulmonar, que afecta a órganos más allá de los pulmones, suele estar asociada a un mayor riesgo de mortalidad que la TBP.
Un hallazgo prometedor fue la protección observada contra la tuberculosis en niños de seis a menos 14 años, donde VPM1002 proporcionó protección contra todos los tipos de tuberculosis, tanto pulmonar como extrapulmonar.
En tanto, la Immuvac proporcionó protección solo contra la tuberculosis extrapulmonar en el grupo de edad de seis a menos de 10 años.
Aclaran los científicos, que ninguna de las vacunas protegió a los niños y adultos con bajo peso.
10 marzo 2026 | Fuente: Prensa Latina | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2026. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
ene
5
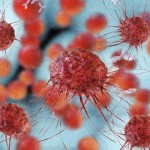 Un método de purificación de sangre afronta su primera prueba como vacuna contra el cáncer, mediante un ensayo clínico que pretende utilizar células tumorales completas inactivadas por luz ultravioleta (UV) como inmunoterapia.
Un método de purificación de sangre afronta su primera prueba como vacuna contra el cáncer, mediante un ensayo clínico que pretende utilizar células tumorales completas inactivadas por luz ultravioleta (UV) como inmunoterapia.
El estudio que comenzará este mes en California modificará células de cáncer de ovario y las devolverá a las pacientes para estimular una respuesta inmunitaria contra los tumores, reflejó la revista Science. En algunas partes del mundo, la sangre donada o sus componentes, como las plaquetas, se desinfectan con UV y riboflavina (vitamina B2) antes de transfundirlas a los pacientes.
Los investigadores buscan utilizar esta técnica, conocida como proceso Mirasol, que puede neutralizar diversos virus, bacterias y parásitos, para combatir el cáncer, inactivar las células tumorales y reintroducirlas en el organismo en busca de desencadenar una respuesta inmunitaria beneficiosa.
El método fue probado en ratones y perros y este mes comenzará un ensayo de fase 1 en pacientes con cáncer de ovario, con la esperanza de que desacelere o prevenga las recaídas en combinación con otras terapias, dijo el químico Ray Goodrich de la Universidad Estatal de Colorado.
Algunos estudiosos están escépticos, pues los intentos de crear vacunas con células cancerosas completas tienen un largo historial de fracasos, alegó Lawrence Fong, inmunólogo y oncólogo del Centro Oncológico Fred Hutchinson.
Ray Goodrich comenzó a trabajar en un método para desinfectar la sangre como estudiante de posgrado a fines de la década de 1980, cuando la contaminación del suministro de sangre por VIH era de gran preocupación.
Tras casi una década, él y sus colegas hallaron como solución mezclar sangre con riboflavina, que se adhiere a las moléculas de ADN y ARN, y luego exponer el líquido a luz ultravioleta, lo cual provoca que la riboflavina reaccione con el material genético de los microbios y lo dañe.
Este método impide que los patógenos se reproduzcan, aunque también daña las plaquetas, los glóbulos rojos y las proteínas del plasma, por lo cual los pacientes pueden requerir transfusiones adicionales.
La idea de una vacuna surgió cuando Goodrich observó que, tras el proceso Mirasol, los glóbulos blancos se inactivaban, pero permanecían intactos.
Los investigadores llevan más de 50 años intentando desarrollar vacunas que contengan células cancerosas completas, pero las formulaciones que llegaron a ensayos clínicos produjeron una respuesta inmunitaria deficiente, y ninguna vacuna fue aprobada para humanos, aunque hay una disponible para mascotas.
El próximo ensayo clínico busca reclutar ocho pacientes con cáncer de ovario en recaída, que serán sometidas a cirugía para extirpar los tumores y luego los científicos expondrán las células tumorales a riboflavina y luz ultravioleta, y las combinarán con un aditivo inmunoestimulante para producir una vacuna personalizada.
Las participantes recibirán tres dosis de vacuna y los expertos evaluarán los efectos secundarios y la respuesta inmunitaria.
02 enero 2026 | Fuente: Prensa Latina | Tomado de | Noticia
abr
16
 El Grupo canadiense de Ensayos Oncológicos (CCTG) se vio obligado a eliminar el lenguaje inclusivo de los documentos asociados a investigaciones con financiamiento estadounidense, por indicación de Washington, destaca hoy la prensa local. De acuerdo con el reporte del diario The Globe and Mail, la directora de cumplimiento del CCTG, Jessica Sleeth, anunció cambios en los protocolos de la organización, entre ellos «la sustitución de la palabra género por la palabra sexo, la eliminación de los términos intersexual y género si es diferente al de nacimiento, y otras modificaciones similares».
El Grupo canadiense de Ensayos Oncológicos (CCTG) se vio obligado a eliminar el lenguaje inclusivo de los documentos asociados a investigaciones con financiamiento estadounidense, por indicación de Washington, destaca hoy la prensa local. De acuerdo con el reporte del diario The Globe and Mail, la directora de cumplimiento del CCTG, Jessica Sleeth, anunció cambios en los protocolos de la organización, entre ellos «la sustitución de la palabra género por la palabra sexo, la eliminación de los términos intersexual y género si es diferente al de nacimiento, y otras modificaciones similares».
Los participantes en los ensayos financiados por Estados Unidos sólo tendrán la opción de identificarse como hombres o mujeres, según lo establece la orden ejecutiva firmada por el presidente Donald Trump el pasado 20 de enero.
La presidenta del CCTG, Janet Dancey, afirmó que su preferencia como investigadora oncológica «siempre ha sido liderar ensayos que reflejen el compromiso del grupo con la diversidad y comprender los efectos del cáncer y su tratamiento en los pacientes y en cada individuo. Sin embargo, esta no es la prioridad de la administración Trump».
Dancey dijo que los equipos de atención médica informarán a los pacientes voluntarios sobre los cambios y algunos podrían optar por no participar.
Por su parte la bioeticista Françoise Baylis, profesora de investigación emérita de la Universidad de Dalhousie, calificó la directiva de la administración Trump de profundamente ofensiva y factualmente incorrecta.
«Se ha trabajado mucho, durante mucho tiempo, para que la gente comprenda la diferencia entre sexo y género», dijo.
También Judy Illes, profesora de neurología y neuroeticista de la Universidad de Columbia Británica, aseguró que los cambios revertirían «décadas de investigación científicamente validada que han demostrado diferencias importantes en el cuerpo y el cerebro según el género».
«Amenazan con restablecer prácticas discriminatorias en la atención médica para el cáncer y otras afecciones médicas, y en la sociedad en general», enfatizó.
Los institutos de investigación en Salud de Canadá destacan la diferencia entre sexo y género y recomiendan explícitamente a quienes solicitan investigación que integren ambos en el diseño y la práctica de la investigación cuando corresponda.
Un artículo de 2016 publicado en la Revista de la Asociación Médica Americana (JAMA por sus siglas en inglés) señaló que ambos no son mutuamente excluyentes y que pueden influir, por ejemplo, en cómo una persona selecciona, responde, metaboliza y se adhiere a un régimen farmacológico específico.
Según su sitio web, el CCTG está integrado por más de 85 instituciones miembros, que comprenden más de 2 100 investigadores canadienses, y ha facilitado más de 600 ensayos. Aproximadamente 3 000 pacientes voluntarios participan cada año en ensayos dirigidos por CCTG para recibir potencialmente mejores tratamientos que también podrían beneficiar a otros en el futuro.
11 abril 2025 | Fuente: Prensa Latina | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2025. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
jun
28
 La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos recomendó el miércoles a los fabricantes de fármacos y dispositivos médicos medidas para mejorar la diversidad racial, étnica y de otro tipo en sus ensayos clínicos.
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos recomendó el miércoles a los fabricantes de fármacos y dispositivos médicos medidas para mejorar la diversidad racial, étnica y de otro tipo en sus ensayos clínicos.
El proyecto de guía incluye sugerencias, para las empresas y los investigadores que llevan a cabo pruebas, sobre cómo establecer objetivos para la inscripción en el estudio, separados por grupo de edad, etnia, sexo y raza, y describir cómo pretenden alcanzar esos objetivos, dijo la FDA.
El objetivo es mejorar la composición de la población de pacientes en los ensayos clínicos que han tenido una menor participación de algunos grupos, incluidos los estadounidenses de raza negra, a pesar de las tasas más altas de ciertas enfermedades en los grupos subrepresentados que en la población general.
La FDA señaló que los objetivos de un estudio, o el «plan de acción para la diversidad», deben establecerse teniendo en cuenta la prevalencia estimada de la enfermedad para la que se evalúa el fármaco o dispositivo.
«Estos planes pueden ayudar a garantizar que los patrocinadores piensen de forma crítica e intencionada en las múltiples características de la población de pacientes que pretenden tratar a la hora de diseñar su estudio clínico», dijo Richard Pazdur, director del Centro de Excelencia de Oncología de la FDA.
Las directrices de la FDA, que no son jurídicamente vinculantes, suelen ser seguidas por las empresas que buscan la aprobación de la agencia para sus productos.
(Reporte de Manas Mishra y Bhanvi Satija en Bengaluru; edición en español de Javier López de Lérida)
26 junio 2024|Fuente: Reuters |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
may
21
 La ciencia celebra hoy el Día Internacional de los Ensayos Clínicos, para divulgar en qué consiste la labor de la investigación para conseguir una vacuna o un medicamento para una enfermedad concreta.
La ciencia celebra hoy el Día Internacional de los Ensayos Clínicos, para divulgar en qué consiste la labor de la investigación para conseguir una vacuna o un medicamento para una enfermedad concreta.
La fecha conmemora el primer ensayo clínico de la historia realizado por el doctor escocés James Lind en 1747 y que sentó las bases para la investigación clínica.
Aquel estudio trataba de identificar la ausencia de la vitamina D como la causa del escorbuto que afectaba a los marineros de la Armada Británica.
En la actualidad, el desarrollo de un nuevo medicamento o vacuna debe pasar por distintas fases, de forma que el proceso puede durar varios años, hasta que el fármaco esté disponible.
20 mayo 2024|Fuente: Prensa Latina |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
feb
15
 El Hospital Universitario La Paz ha presentado el proyecto ‘CAR4SAR’, el primer ensayo clínico en el mundo realizado con un CAR-T alogénico (procedente de un donante) para sarcomas pediátricos, aunque también comprenderá a adolescentes y jóvenes adultos.
El Hospital Universitario La Paz ha presentado el proyecto ‘CAR4SAR’, el primer ensayo clínico en el mundo realizado con un CAR-T alogénico (procedente de un donante) para sarcomas pediátricos, aunque también comprenderá a adolescentes y jóvenes adultos.
Con motivo del Día Internacional del Cáncer Infantil, que se celebra el 15 de febrero, se ha presentado el proyecto, que ha sido liderado por el hospital madrileño y que se ha puesto en marcha en la Unidad CRIS del centro. Con el nombre ‘CAR4SAR’, esta terapia totalmente personalizada se elabora de forma individualizada para cada enfermo.
Se produce a partir de la sangre de un donante familiar de la que se extraen unas células, los linfocitos T de memoria, a los que, mediante ingeniería genética, se les dota de un receptor antígeno quimérico (CAR por sus siglas en inglés) del tipo NKG2D, capaz de reconocer y atacar sus múltiples células tumorales.
‘Es un fármaco vivo e inteligente que actúa cuando está la diana y desaparece cuando no está’, ha destacado el jefe de Servicio de Hemato-Oncología Pediátrica, Antonio Pérez Martínez, quien ha liderado el ensayo clínico en fase temprana de terapias CAR-T en tumores sólidos.
Participarán 15 pacientes en el ensayo El propio Pérez Martínez ha informado que el ensayo comenzará en breve y en él participarán 15 pacientes que serán tratados con CAR-T alogénico, después de que no hayan respondido a dos líneas de tratamiento anteriores. ‘No se trata de un tratamiento específico para un tumor en concreto, ataca a una vía que es común para otros tumores. En concreto, es un CAR-T de nueva generación que no tiene una única diana, es ‘multitarget’ y llega a reconocer hasta seis dianas’, ha afirmado el especialista. Asimismo, durante la presentación del ensayo, Pérez Martínez ha resaltado la importancia de que el CAR-T sea alogénico, es decir, que procede de otro individuo, que suele ser un familiar cercano. ‘Los CAR-T suelen ser autólogos, es decir, los que proceden del propio paciente. En este tipo de terapias, un 20 por ciento de los pacientes no pueden producir un CAR-T autólogo.
Esto se debe a que los pacientes no tienen linfocitos T, ya que, por los tratamientos a los que se han sometido, los han agotado. Además, existe otra complicación y es que, aunque los pacientes tengan linfocitos T, la calidad estos no es buena, también debido a los tratamientos que ha recibido’.
Tratamiento de los sarcomas Los sarcomas son un tipo de tumor que representa el 10 por ciento de los cánceres pediátricos y para los que hay pocas alternativas de tratamiento. Actualmente, en los pacientes con la enfermedad localizada y de riesgo estándar, la supervivencia es del 70-80 por ciento.
Para aquellos con enfermedad grave, que sufren recaídas, o los que desarrollan metástasis, la tasa de supervivencia es del 30 por ciento. El tratamiento actual consiste en cirugía local, radioterapia y poliquimioterapia, pero, según los expertos es ineficaz en estadios avanzados, lo que empeora su calidad de vida. El inicio de este ensayo, es un paso para la mejora del tratamiento y pronóstico de estos niños.
En un futuro, se prevé extender el tratamiento CAR-T a otros tumores sólidos pediátricos con baja tasa de éxito con las terapias convencionales. ‘Las CAR-T están cambiando el paradigma, no solo en el cáncer, sino en otras enfermedades que hasta el momento no tienen tratamiento’, ha señalado Pérez Martínez.
Asimismo, han colaborado en el proyecto instituciones académicas asistenciales, como el Centro Nacional de Investigaciones Oncológicas (CNIO), el Instituto de Salud Carlos III (ISCIII), el Hospital Universitario Central de Asturias (HUCA) y la Fundación CRIS contra el Cáncer.
Además, al tratarse la CAR-T de un organismo modificado genéticamente, el ensayo ha recibido la autorización de fabricación por parte de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) y del Ministerio para la Transición Ecológica y el Reto Demográfico.
14 de febrero 2024| Fuente: Europa Press| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A

