jul
25
 Unas inyecciones que se administran dos veces al año para tratar el sida mostraron una eficacia del 100 % en la prevención de nuevos contagios en mujeres, según resultados de un estudio publicados el miércoles.
Unas inyecciones que se administran dos veces al año para tratar el sida mostraron una eficacia del 100 % en la prevención de nuevos contagios en mujeres, según resultados de un estudio publicados el miércoles.
No se produjeron contagios entre las niñas y mujeres jóvenes que recibieron las dosis en un estudio de unas 5 000 personas en Sudáfrica y Uganda, según los investigadores. En un grupo que recibió pastillas diarias de prevención, en torno al 2 % terminó contrayendo el VIH de parejas sexuales infectadas.
«Ver este nivel de protección es impresionante», dijo sobre las inyecciones Salim Abdool Karim, director del centro de investigación sobre sida en Durban, Sudáfrica, que no participó en el estudio.
El fármaco, producido por la estadounidense Gilead y comercializado como Sunlenca, está autorizado en Estados Unidos, Canadá, Europa y otros lugares, pero sólo como tratamiento contra el VIH. La compañía dijo que estaba esperando a los resultados de la prueba en hombres antes de pedir autorización para utilizarlo como protección ante infecciones.
Los resultados en mujeres se publicaron el miércoles en la New England Journal of Medicine y se comentaron en una conferencia sobre el sida en Múnich. Gilead pagó el estudio y parte de los investigadores eran empleados de la compañía. Debido a los resultados inesperadamente alentadores, el estudio se detuvo antes de tiempo y todas las participantes recibieron las inyecciones, también conocidas como lenacapavir.
Aunque hay otras formas de impedir la infección de VIH, como los preservativos o las píldoras diarias, el uso consistente ha sido un problema en África. En el nuevo estudio, sólo en torno al 30 % de las participantes que recibieron las píldoras preventivas Truvada o Descovy de Gilead las tomaban, y esa cifra se redujo con el tiempo.
La perspectiva de una inyección dos veces al año «son noticias bastante revolucionarias» para nuestros pacientes, dijo Thandeka Nkosi, que ayudó a dirigir la investigación de Gilead en la Fundación de Salud Desmond Tutu en Masiphumelele, Sudáfrica. «Da a los participantes una opción y simplemente elimina todo el estigma en torno a tomar las píldoras» para prevenir el VIH.
Los expertos que trabajan para detener la expansión del sida están emocionados por las inyecciones de Sunlenca pero les preocupa que Gilead no haya llegado a un acuerdo aún sobre un precio asequible para los que más lo necesitan. La compañía dijo que buscaría un «programa de licencias voluntarias», lo que sugería que sólo unos pocos productores de medicamentos genéricos estarían autorizados a fabricar el fármaco.
«Gilead tiene una herramienta que podría cambiar la trayectoria de la epidemia del VIH», dijo Winnie Byanyima, directora ejecutiva de la agencia de la ONU contra el sida, con sede en Ginebra.
Dijo que su organización había instado a Gilead a compartir la patente de Sunlenca con un programa respaldado por la ONU que negocia contratos generales para que fabricantes de genéricos hagan versiones baratas de medicamentos para países más pobres en todo el mundo. Como tratamiento del VIH, el fármaco cuesta más de 40 000 dólares al año en Estados Unidos, aunque el precio individual puede variar.
En un comunicado el mes pasado, Gilead dijo que era demasiado pronto para saber cuánto costaría utilizarlo como prevención en países más pobres. El doctor Jared Baeten, vicepresidente de Gilead para desarrollo clínico, dijo que la firma ya estaba hablando con fabricantes de genéricos y comprendía «lo profundamente importante que es que actuemos con rapidez».
Otro medicamento de prevención del VIH, Apretude, que se toma cada dos meses, está autorizado en algunos países, también en África. Se vende por unos 180 dólares por paciente al año, que sigue siendo demasiado costoso para la mayoría de países en desarrollo.
Byanyima dijo que entre las personas que más necesitan protección duradera hay mujeres y niñas víctimas de violencia doméstica y hombres gays en países donde las relaciones homosexuales están penalizadas. Según UNAIDS, el 46 % de las nuevas infecciones de VIH en 2022 eran de mujeres y niñas, que eran tres veces más propensas a contraer el VIH que los hombres en África.
Byanyima comparó las noticias sobre Sunlenca con el descubrimiento hace décadas de fármacos contra el sida que hicieron que la infección del VIH pasara de ser una sentencia de muerte a una enfermedad crónica. En su momento, el presidente sudafricano Nelson Mandela suspendió las patentes para permitir un acceso más amplio al medicamento. El precio bajó más tarde, de unos 10 000 dólares por paciente a unos 50 dólares.
Olwethu Kemele, trabajadora médica en la Fundación de Salud Desmond Tutu predijo que las inyecciones podrían incrementar el número de personas que reciben en busca de prevención contra el VIH y detener la expansión del virus. A menudo, señaló, las mujeres jóvenes esconden las pastillas para evitar preguntas de novios y familiares. «Hace que para las chicas sea difícil continuar», explicó.
En un reporte sobre el estado de la epidemia global publicado esta semana, Unaids (Onusida) dijo que se habían infectado menos personas de VIH en 2023 que en cualquier momento desde la década de 1980. En todo el mundo, unos 1,3 millones de personas se contagian de VIH y más de 600 000 mueren cada año, en su mayoría en África. Aunque se han hecho avances significativos en el continente, las infecciones de VIH suben en el este de Europa, América Latina y Oriente Medio.
En otra investigación presentada en la conferencia sobre sida, Andrew Hill, de la Universidad de Liverpool, y otros colegas estimaron que una vez se expanda la producción de Sunlenca para tratar a 10 millones de personas, el precio debería caer a unos 40 dólares por tratamiento. Señaló que es crítico que las autoridades de salud consigan acceso al medicamento lo antes posible.
«Esto es lo más cerca que puedes estar a una vacuna del VIH», dijo.
24 julio 2024|Fuente: AP |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
jun
28
 La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos recomendó el miércoles a los fabricantes de fármacos y dispositivos médicos medidas para mejorar la diversidad racial, étnica y de otro tipo en sus ensayos clínicos.
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos recomendó el miércoles a los fabricantes de fármacos y dispositivos médicos medidas para mejorar la diversidad racial, étnica y de otro tipo en sus ensayos clínicos.
El proyecto de guía incluye sugerencias, para las empresas y los investigadores que llevan a cabo pruebas, sobre cómo establecer objetivos para la inscripción en el estudio, separados por grupo de edad, etnia, sexo y raza, y describir cómo pretenden alcanzar esos objetivos, dijo la FDA.
El objetivo es mejorar la composición de la población de pacientes en los ensayos clínicos que han tenido una menor participación de algunos grupos, incluidos los estadounidenses de raza negra, a pesar de las tasas más altas de ciertas enfermedades en los grupos subrepresentados que en la población general.
La FDA señaló que los objetivos de un estudio, o el «plan de acción para la diversidad», deben establecerse teniendo en cuenta la prevalencia estimada de la enfermedad para la que se evalúa el fármaco o dispositivo.
«Estos planes pueden ayudar a garantizar que los patrocinadores piensen de forma crítica e intencionada en las múltiples características de la población de pacientes que pretenden tratar a la hora de diseñar su estudio clínico», dijo Richard Pazdur, director del Centro de Excelencia de Oncología de la FDA.
Las directrices de la FDA, que no son jurídicamente vinculantes, suelen ser seguidas por las empresas que buscan la aprobación de la agencia para sus productos.
(Reporte de Manas Mishra y Bhanvi Satija en Bengaluru; edición en español de Javier López de Lérida)
26 junio 2024|Fuente: Reuters |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
may
18
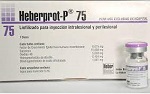 El Heberprot-P, medicamento desarrollado por Cuba y hoy único de su tipo en el mundo para combatir la úlcera del pie diabético, podría estar en el mercado de Estados Unidos en 2028, anticipó el doctor Lee Weingart.
El Heberprot-P, medicamento desarrollado por Cuba y hoy único de su tipo en el mundo para combatir la úlcera del pie diabético, podría estar en el mercado de Estados Unidos en 2028, anticipó el doctor Lee Weingart.
Presidente de la compañía biotecnológica estadounidense Discovery Therapeutics Caribe (DTC), con sede en Cleveland (Ohio), Weingart confirmó en declaraciones a Prensa Latina en esta capital que tienen la aprobación de la Administración de Medicamentos y Alimentos (FDA) para comenzar la fase 3 de esos estudios clínicos.
«Hemos podido operar al amparo de una excepción al embargo (bloqueo), que permite proyectos conjuntos de investigación médica en los que participamos nosotros y las organizaciones cubanas, así que hemos utilizado esa disposición para sacar adelante este proyecto», dijo.
Adelantó que en el estudio participarán alrededor de «180 pacientes en unos 25 centros» del país y «creemos que tardaremos unos 18 meses en realizarlo. Esperamos estar en el mercado con este medicamento aprobado por la FDA a mediados de 2028″.
A una pregunta de la reportera acerca de la población con esta afectación de salud aquí, el doctor Weingart afirmó que “38,4 millones de estadounidenses padecen diabetes, de ellos 1,6 millones cada año desarrollarán una úlcera de pie diabético”.
De esa cifra «160 000 resultarán en una amputación y de ellos 80 000 morirán en los próximos cinco años, así pues, si se sigue el ciclo, cada año 80 000 personas mueren por las complicaciones de una úlcera del pie diabético lo que hace que sea la octava causa de muerte en Estados Unidos y más mortal que ciertos tipos de cáncer», advirtió.
El experto asistió la víspera a un evento promocionado por la embajada de Cuba en Estados Unidos, en el que se expusieron las posibilidades colaboración bilateral en los sectores de la biomedicina y las investigaciones biotecnológicas.
Las presentaciones en la reunión las realizaron el doctor Mitchell Valdés, director del Centro de Neurociencias de Cuba y miembro de la Academia de Ciencias de la isla, el distinguido profesor Mark M. Rasenick y Weingart.
En el auditorio estaban la congresista demócrata Jan Schakowsky, el doctor Peter Agre, Premio Nobel de Química 2003, entre otras personalidades.
Schakowsky y la congresista Barbara Lee hicieron circular en 2013 una carta entre sus colegas pidiendo al Departamento de Hacienda que emitiera una licencia a un grupo que quería realizar un ensayo clínico de Heberprot-P en Estados Unidos, explicó.
Seis años más tarde la congresista Lee interrogó al comisario de la FDA sobre por qué el Heberprot-P no estaba disponible todavía en el país, «así que siento que estamos haciendo realidad lo que se pensó debió suceder en 2013 y en 2019″, acotó.
DTC, que se dedica a mejorar los resultados de salud de los estadounidenses mediante el desarrollo de terapias regenerativas para enfermedades graves y potencialmente mortales, al hacer el anuncio de la FDA a inicios de mayo expresó que logró un hito importante que refleja el progreso en su programa clínico.
El fármaco cubano, que ayuda a cerrar heridas difíciles de curar en pacientes diabéticos, fue desarrollado hace dos décadas y su uso fue autorizado ya en 26 países.
Otras colaboraciones de investigación médica entre Estados Unidos y Cuba tienen lugar entre el Roswell Park Cancer Institute (RPCI) y el Centro de Inmunología Molecular de Cuba para estudios sobre ese mal.
En 2022, el RPCI se convirtió en el primero en obtener la autorización de la FDA para ensayos clínicos en Estados Unidos con terapia cubana.
17 mayo 2024|Fuente: Prensa Latina |Tomado de |Noticia
abr
27
Según el estudio más de 200.000 personas en todo el mundo padecen Esclerosis Lateral Amiotrófica (ELA), una enfermedad progresiva del sistema nervioso que afecta a las células nerviosas del cerebro y la médula espinal.
Actualmente no existe cura para la ELA. La mayoría de las personas que padecen la enfermedad mueren en un plazo de tres a cinco años de diagnóstico de insuficiencia respiratoria. Alrededor del 10% de los enfermos de ELA viven más de 10 años. Alrededor del 20% de los casos de ELA familiar están causados por una mutación en el gen SOD1.
¿Qué es la ELA?
La ELA ataca específicamente a un tipo de células nerviosas denominadas motoneuronas. A medida que las neuronas motoras disminuyen, el sistema nervioso deja de ser capaz de enviar mensajes a los músculos, lo que provoca que éstos se debiliten y dejen de funcionar. A medida que la enfermedad avanza, los enfermos de ELA acaban siendo incapaces de mantenerse en pie o caminar sin ayuda, así como tampoco pueden utilizar las manos ni los brazos. Las personas con ELA también pueden experimentar dificultades para hablar, comer y respirar.
La mayoría de los casos de ELA se consideran esporádicos, lo que significa que se dan en personas sin antecedentes familiares de la enfermedad. Sin embargo, alrededor del 10% de los casos de ELA se consideran familiares, lo que significa que la enfermedad es hereditaria.
Según el Dr. Toby Ferguson, vicepresidente y director de la Unidad de Desarrollo Neuromuscular de Biogen, la SOD1-ALS es una forma genética rara de ELA diagnosticada en aproximadamente 330 personas en Estados Unidos.
«Puede avanzar rápidamente, siempre es mortal y puede tener un impacto devastador en las familias durante generaciones», declaró a Medical News Today. «De aprobarse, el tofersén representaría un nuevo avance científico para la comunidad de la ELA al ser el primer y único tratamiento dirigido a una causa genética de la ELA. Esperamos que esto allane el camino para nuevos avances en esta implacable enfermedad.»
¿Cómo funciona el tofersén?
Ferguson explicó que tofersen es un oligonucleótido antisentido (ASO) que se está evaluando para el tratamiento de la SOD1-ALS.
«Los ASO son cadenas cortas y sintéticas de nucleótidos diseñadas para unirse selectivamente al ARN diana y regular la expresión génica», explicó. «En las personas con SOD1-ALS, las mutaciones en el gen SOD1 hacen que su organismo genere una forma tóxica de la proteína SOD1. Esta forma tóxica de la proteína SOD1 provoca la degeneración de las motoneuronas, lo que da lugar a una debilidad muscular progresiva.»
«Tofersen está diseñado para unirse y degradar el ARNm de SOD1 en un esfuerzo por reducir la producción de la proteína SOD1″, añadió Ferguson.
Resultados de la fase 3
Ferguson dijo que los datos integrados de 12 meses del ensayo clínico de fase 3 VALOR y su extensión abierta (OLE) han mostrado reducciones en neurofilamento – un marcador de daño a las neuronas y neurodegeneración.
«Existe una amplia bibliografía que indica que los niveles de neurofilamento son pronósticos de la progresión de la enfermedad y la supervivencia, con niveles más altos asociados con (una) disminución más rápida de la función clínica y una supervivencia más corta», añadió Ferguson. «La combinación de estos resultados de biomarcadores y los datos de resultados clínicos proporcionan pruebas adicionales del potencial de tofersen para ralentizar eficazmente la progresión de la SOD1-ALS».
Biogen afirma en su comunicado de prensa que tofersén no alcanzó el criterio de valoración primario de cambio desde el valor basal hasta la semana 28 en la Escala Revisada de Valoración Funcional de la Esclerosis Lateral Amiotrófica (ALSFRS-R). Sin embargo, los investigadores descubrieron que tofersén provocaba un menor deterioro de la función motora, la función respiratoria, la fuerza muscular y la calidad de vida en personas con SOD1-ALS.
El proceso de aprobación
El 22 de marzo, el Comité Asesor sobre Fármacos para el Sistema Nervioso Central y Periférico de la FDA presentó su propia evaluación de la eficacia del tofersén.
Según un comunicado de prensa de Biogen, el comité asesor declaró que la eficacia del fármaco experimental no era suficiente. Sin embargo, el comité consultivo declaró que la capacidad de tofersen para reducir la concentración plasmática de la cadena ligera de neurofilamentos (NfL) es «razonablemente probable» que proporcione un beneficio clínico a las personas con SOD1-ALS.
«Se trata de un avance monumental en el campo de la ELA, en el que las medidas objetivas sensibles a los cambios inducidos por el tratamiento, especialmente en las fases iniciales de la enfermedad, son muy demandadas», afirmó Ferguson. «Nos encontramos aquí en gran parte debido al trabajo que la comunidad de la ELA ha realizado para caracterizar el comportamiento del neurofilamento durante la última década».
«Aunque la idoneidad del neurofilamento como posible sustituto se evaluará caso por caso, esperamos que los datos del programa tofersen sean un catalizador adicional para el uso del neurofilamento y otros biomarcadores novedosos en el futuro», añadió.
Abril 26/2023 (Medical News Today) – Tomado de Latest News Copyright 2023 Healthline Media UK Ltd, Brighton, UK.
Traducción realizada con la versión gratuita del traductor www.DeepL.com/Translator
feb
5
Un método más amable y discreto para uno de los exámenes más temidos en la medicina está por llegar: reguladores estadounidenses aprobaron una cámara que es del tamaño de un bocado que ayudará a ver el intestino grueso de pacientes que tienen dificultades para realizarse colonoscopías tradicionales. Read more
ene
21
La Administración de Alimentos y Medicamentos de Estados Unidos, regulador del sector, apuró la aprobación de un nuevo y controvertido fármaco para tratar algunas formas de tuberculosis resistentes a otros tratamientos. Read more

