mar
24
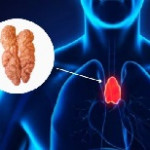 El timo es un órgano pequeño ubicado en el pecho, detrás del esternón. Su función principal es ayudar a desarrollar y educar las células T, esenciales para el sistema inmunológico.
El timo es un órgano pequeño ubicado en el pecho, detrás del esternón. Su función principal es ayudar a desarrollar y educar las células T, esenciales para el sistema inmunológico.
Hasta muy reciente, pocos imaginaban que el timo podía influir tanto en la salud y la longevidad. Científicos de los Estados Unidos, Países Bajos, Alemania, Dinamarca y Reino Unido sugieren que la salud de ese órgano está asociada a vivir más años y a tener menos riesgo de cáncer y enfermedades cardiovasculares.
Las implicaciones van más allá de la prevención: la salud del timo también parece tener un papel en la respuesta a tratamientos innovadores como la inmunoterapia.
La investigación fue publicada en la revista Nature. Fue llevada a cabo por científicos del Programa de Inteligencia Artificial en Medicina de Mass General Brigham y la Escuela de Medicina de Harvard, el Departamento de Oncología Radioterápica del Hospital Brigham and Women y el Instituto Dana-Farber de Cáncer, Estados Unidos.
También colaboraron investigadores de la Universidad de Maastricht, en Países Bajos, la Universidad Goethe de Frankfurt, Alemania, el Hospital Universitario de Aarhus, en Dinamarca, y el Colegio Universitario de Londres y el Instituto Francis Crick, en el Reino Unido.
Contaron con el financiamiento de los Institutos Nacionales de Salud, el Consejo Europeo de Investigación y la Fundación DFG de Alemania.
La importancia del timo después de la infancia
Durante años, el timo se consideró fundamental solo en la niñez porque produce y educa células T, que defienden al cuerpo de infecciones. Después de la pubertad, el timo se encoge y pierde actividad, y por eso se pensaba que su función en adultos era irrelevante.
Pero el nuevo estudio desafió esa idea. Los investigadores quisieron saber si el estado del timo en adultos podría influir en la salud general, la longevidad y la respuesta a terapias avanzadas como la inmunoterapia.
Partieron de la hipótesis de que la diversidad de células T disminuye con la edad y que eso podría estar ligado al deterioro inmunológico.
Hasta ahora, la mayoría de los trabajos en adultos se basaban en análisis de sangre con grupos pequeños, lo que limitaba sus resultados.
Esa investigación analizó a decenas de miles de personas con el objetivo de comprobar si la salud tímica tiene un papel central en la protección frente a enfermedades y en la calidad de vida.
El objetivo central fue diseñar una forma confiable y no invasiva de medir la salud tímica en adultos, usando tomografías computarizadas.
Luego, correlacionaron ese resultado con datos de salud y longevidad en cohortes de gran tamaño.
Cómo se midió la salud tímica
Los investigadores crearon un modelo de inteligencia artificial que analiza imágenes de tomografías y calcula un puntaje de salud tímica.
El sistema examinó el tamaño, la forma y la composición del órgano en más de 25 000 adultos del ensayo nacional de tamizaje de cáncer de pulmón y más de 2.500 del Estudio Framingham del Corazón.
A quienes tenían un puntaje alto se los asoció con cerca del 50% menos riesgo de muerte, 63% menos riesgo de morir por enfermedades cardiovasculares y 36% menos riesgo de desarrollar cáncer de pulmón respecto de quienes tenían un puntaje bajo.
“Estas asociaciones se mantuvieron significativas luego de ajustar por edad y otros factores de salud”, detallaron los investigadores.
El análisis mostró que la inflamación crónica, el tabaquismo y el exceso de peso se relacionan con una peor salud tímica.
Los resultados sugieren que el estilo de vida y la inflamación sistémica pueden influir en la capacidad del sistema inmune para enfrentar amenazas durante la vida.
En otra etapa, los investigadores analizaron a más de 1.200 pacientes con cáncer tratados con inmunoterapia. En este grupo, quienes tenían mejor salud tímica presentaron 37% menos riesgo de progresión del cáncer y 44% menos riesgo de morir.
Los resultados sugieren que el timo podría ser un factor no considerado al evaluar la respuesta a la inmunoterapia.
Sugirieron que mejorar la comprensión y el monitoreo de la salud tímica podría ayudar a los médicos a valorar el riesgo de enfermedades y decidir tratamientos.
Perspectivas para la salud tímica
Tras los resultados, los investigadores recomendaron prestar más atención a la salud tímica en adultos y explorar nuevas formas de proteger este órgano.
Aclararon que, aunque ciertos factores de vida se asociaron con la función del timo, no se probó si cambiar hábitos mejora su salud. Por eso, deberían hacerse más investigaciones.
El equipo ya estudia si la exposición involuntaria a radiación en tratamientos de cáncer de pulmón afecta la función tímica.
Consultado por Infobae el médico Ramiro Heredia, especialista en medicina interna del Hospital de Clínicas José de San Martín de la Universidad de Buenos Aires, opinó: “El timo es un órgano fundamental para el sistema inmunológico, especialmente durante la infancia. En esa etapa, los médicos le prestamos una mayor atención. Con el tiempo, suele perder relevancia fisiológica porque, de manera natural, es reemplazado por tejido adiposo y sus funciones las asume el resto del sistema inmune periférico”.
La investigación publicada en Nature «presenta hallazgos que llaman la atención y pueden motivar nuevos estudios. En personas donde la masa tímica se conserva mejor a lo largo de la vida, se observaron resultados positivos, como menor mortalidad cardiovascular, menor incidencia de cáncer, menor mortalidad general y mayor respuesta a tratamientos como la inmunoterapia para cánceres avanzados», señaló.
“Este tipo de estudios, al ser observacionales, no permiten establecer relaciones de causalidad, pero sí abren la puerta a futuras investigaciones sobre el tema. Todo esto resulta prometedor para comprender mejor el papel del timo en la salud adulta”, sostuvo Heredia.
19 marzo 2026 | Fuente: Infobae | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2026. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
feb
2
 La desnutrición en personas que sufren algún cáncer oscila entre el 15 y 40 %, es decir que llega a afectar a 4 de cada 10 enfermos, e incluso puede alcanzar al 80 % en fases avanzadas, una situación que perjudica el sistema inmune, favorece infecciones, empeora la respuesta a los tratamientos y provoca deterioro funcional, factores asociados a menor supervivencia.
La desnutrición en personas que sufren algún cáncer oscila entre el 15 y 40 %, es decir que llega a afectar a 4 de cada 10 enfermos, e incluso puede alcanzar al 80 % en fases avanzadas, una situación que perjudica el sistema inmune, favorece infecciones, empeora la respuesta a los tratamientos y provoca deterioro funcional, factores asociados a menor supervivencia.
La desnutrición o mal nutrición asociada a la enfermedad es una cuestión que afecta a hospitalizados, principalmente a personas con edad avanzada, y para hacer frente a ello existen muchas barreras, que van desde una legislación obsoleta, hasta notables diferencias en los recursos de los hospitales de cada comunidad autónoma, principalmente en lo referente a profesionales que puedan aplicar la mejor terapia nutricional a cada paciente.
Existe, por tanto, una relación directa entre una mala nutrición y la vida media del paciente con cáncer:
hasta un 20 % de los enfermos, es decir 2 de cada 10, fallecen por problemas nutricionales ya que responden mal a los tratamientos y enfrentan peor su enfermedad. Lo ponen de manifiesto especialistas en endocrinología y nutrición, así como oncólogos consultados por EFE, que puntualizan que los problemas nutricionales también dependen mucho del tipo de cáncer y del estadio de la enfermedad.
Se da una prevalencia mayor en pacientes con tumores del tracto digestivo, los sometidos a una cirugía mayor y los que reciben quimioterapia o radioterapia ya que puede afectar a la ingesta, digestión o absorción de los alimentos.
Las estadísticas médicas apuntan también que 1 de cada 3 pacientes con cáncer, un dato que podría ser mayor, llega a perder hasta 10 kilos como consecuencia de su tumor tras ser diagnosticado y más de la mitad pierden un 10 % de su peso, una merma que impacta negativamente en el índice de masa muscular (sarcopenia), un factor asociado a la supervivencia y calidad de vida del paciente.
En una entrevista con EFE, Yolanda Escobar, coordinadora de la sección de Cuidados Continuos de la Sociedad Española de Oncología Médica (SEOM), explica que es importante desde el punto de vista clínico percibir la mal nutrición antes de que se someta al paciente a procesos quirúrgicos o tratamiento y remarca que los comités de tumores en los hospitales deben contar con al menos un profesional para clasificar el riesgo nutricional, en caso de que exista.
Indica que hay un déficit de profesionales en nutrición y endocrinología para personalizar las necesidades de cada persona y cita como ejemplo que un paciente puede estar mal nutrido y ‘sarcopénico’ (es decir tendente a la pérdida de masa muscular) incluso siendo obeso y son perfiles, advierte, que a veces ‘son difíciles de detectar’ por los profesionales oncológicos.
Aumentan las estimaciones de cáncer para 2024 Según estimaciones de SEOM, este año se diagnosticarán 286.664 nuevos casos de cáncer, un 2,6 % más que en 2023, principalmente tumores colorrectales, de mama y de pulmón.
Mientras que la Sociedad Española de Patología Digestiva estima que más del 25% de los nuevos casos de cáncer diagnosticados en España afectarán al aparato digestivo. La desnutrición ensombrece el pronóstico ‘La desnutrición asociada al cáncer ensombrece el pronóstico, empeora la calidad de vida, aumenta las complicaciones de la cirugía, disminuye la tolerancia a la quimio y radioterapia, aumenta la tasa de abandono de tratamientos, aumenta los días de ingreso hospitalario, los reingresos y encarece muy significativamente el coste del proceso’, cuenta a EFE Francisco Botella Romero, coordinador del Área de Nutrición de la Sociedad Española de Endocrinología y Nutrición (SEEN).
Comenta, al igual que la coordinadora de SEOM, que la dieta es un tratamiento médico que debe ser adaptado a cada caso y aclara que para algunos se recomienda una dieta densa en calorías y para otros una rica en proteínas, pero, en resumen, dicen ambos, la mediterránea ofrece un amplio abanico de opciones para cubrir requerimientos nutricionales.
Ambos expertos advierten sobre las modas del ayuno o dietas como la cetogénica (baja en carbohidratos y rica en grasas, vegetales y proteínas) ya que no se recomiendan en la gran mayoría de pacientes con cáncer y menos si hay riesgo de desnutrición.
Ojo a los suplementos nutricionales ‘milagro’ Desde la SEOM, Escobar precisa que los suplementos nutricionales se suelen prescribir si el paciente no puede llegar a los requerimientos nutricionales habituales como consecuencia de su enfermedad o factores previos y, en la misma línea que la SEEN, apuesta por los que tengan evidencia científica contrastada y puedan ser una opción terapéutica.
La mayoría de los suplementos de venta libre o los denominados ‘milagro’ no tienen eficacia demostrada, advierte el profesional de la SEEN.
El ayuno puede ser perjudicial Sobre el ayuno intermitente, un hábito de moda y muy promovido en las redes sociales por los denominados gurús de la salud y el bienestar, la experta de la SEOM lo ve contraproducente en la gran mayoría de los casos y apunta que aún no hay una evidencia científica sólida que respalde sus beneficios en enfermos con cáncer.
Es más, señala que no tiene sentido en pacientes con mal nutrición ya que cuando pierden hasta un 30% de su composición corporal se observa una mayor toxicidad asociada a los fármacos contra el cáncer, así como peor respuesta a los tratamientos. Por su parte, Botella aclara que un ayuno de ‘corto periodo’ puede ayudar a tolerar los efectos secundarios de algunos quimioterápicos, pero no se recomienda por ‘el gravísimo riesgo de desnutrición’ que conllevan algunos tipos de cáncer: solo debería realizarse bajo control médico y en casos muy seleccionados, concluye.
2 febrero 2024| Fuente: EFE| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A
ene
6
 Los investigadores y colaboradores de Mayo Clinic han identificado una proteína expresada en células inmunitarias que podría desempeñar un rol clave en el desarrollo de la esclerosis lateral amiotrófica (ELA), también conocida como enfermedad de Lou Gehrig. El equipo también descubrió que un tratamiento inmunomodulatorio que bloquea la proteína era capaz de restaurar la función motriz en modelos preclínicos. Los hallazgos indican que la proteína, conocida como integrina α5 (pronunciado integrina alfa 5), es un posible blanco terapéutico para la ELA. Read more
Los investigadores y colaboradores de Mayo Clinic han identificado una proteína expresada en células inmunitarias que podría desempeñar un rol clave en el desarrollo de la esclerosis lateral amiotrófica (ELA), también conocida como enfermedad de Lou Gehrig. El equipo también descubrió que un tratamiento inmunomodulatorio que bloquea la proteína era capaz de restaurar la función motriz en modelos preclínicos. Los hallazgos indican que la proteína, conocida como integrina α5 (pronunciado integrina alfa 5), es un posible blanco terapéutico para la ELA. Read more
oct
11
 Para alivio de todos, y tras el fin de la emergencia sanitaria, ya se habla cada vez menos de la pandemia de covid-19. Sin embargo, queda un tema polémico: el de la covid persistente (o long covid en inglés).
Para alivio de todos, y tras el fin de la emergencia sanitaria, ya se habla cada vez menos de la pandemia de covid-19. Sin embargo, queda un tema polémico: el de la covid persistente (o long covid en inglés).
Unos dicen que se trata de una invención y que sólo está en la cabeza de los pacientes. Otros que es una catástrofe en ciernes que volverá a colapsar el sistema sanitario. Para orientarnos en este asunto, en los últimos meses se ha generado información nueva que nos puede evitar caer en uno de esos dos extremos.
En primer lugar, ya tenemos números aproximados sobre la incidencia a nivel poblacional. Se estima que al menos un 10 % de los casos de covid resultan en covid persistente. Si hay contabilizados 650 millones de casos totales en el mundo, esto supone 65 millones de personas. Según la gravedad de la enfermedad el porcentaje varía: es menor (10-30 %) si el curso de la enfermedad fue leve, mientras que en los hospitalizados aumenta hasta un 50-70 %.
De acuerdo con una reciente revisión con datos de diversos estudios y encuestas, alrededor del 80 % son mujeres, el 50 % de los casos tienen edades comprendidas entre los 36 y 50 años (una media de 43 años) y el 30 % no tiene comorbilidades asociadas previas.
Nuestra misión es compartir el conocimiento y enriquecer el debate.
Además de estas estadísticas que nos ayudan a poner el problema en contexto, se ha avanzado mucho en la definición correcta de la covid persistente y sus similitudes con otros síndromes postvirales, lo que facilita el diagnóstico. Y, por último, ya se disciernen posibles métodos de prevención y tratamiento.
¿Qué es la covid persistente y por qué surge?
A pesar de llevar observándose desde el comienzo de la pandemia, el término “covid persistente” todavía genera confusión e incertidumbre. La razón es que no nos hallamos ante una afección limitada a un órgano concreto. En realidad, lo podríamos definir como un síndrome que aparece en ciertas personas tras haber enfermado de covid-19.
Y ¿cuándo se puede decir que alguien sufre de covid persistente? Según la OMS, cuando los síntomas persisten al menos durante 2 meses sin ninguna otra explicación, independientemente de la gravedad con la que hayamos pasado la enfermedad.
El meollo de la cuestión es que esos síntomas no están claramente identificados. Existen hasta 200 diferentes, que pueden requerir la intervención de diversos especialistas médicos.
Esquema de los síntomas de la covid persistente con sus patologías asociadas y los especialistas que las pueden tratar. Adaptado por Matilde Cañelles.
Con semejante lista de síntomas, no es de extrañar que hasta los mismos profesionales tengan dificultades diagnosticando los casos. Para complicar aún más las cosas, el comienzo y duración de los síntomas es variado. Por ejemplo, los síntomas neurológicos suelen aparecer con un retraso de semanas o incluso meses tras pasar la enfermedad. Este tipo de síntomas tiende a empeorar con el tiempo y durar más.
Por otro lado, los síntomas gastrointestinales y respiratorios aparecen antes y es más fácil que acaben desapareciendo. Hay otros síntomas, como dolor de articulaciones y espalda, pérdida de cabello, visión borrosa o hinchazón de las extremidades inferiores, que son más comunes tras un año que a los dos meses.
Por desgracia, muy pocas personas diagnosticadas con covid persistente se recuperan del todo. Es más, según un estudio de 2022, un 85 % de los pacientes que tenían síntomas a los dos meses de pasar la enfermedad, aún los conservaban después de un año.
¿Reservorios de virus, autoinmunidad o un sistema inmune alterado?
Aunque las causas de este síndrome no se conocen a ciencia cierta, se manejan varias hipótesis:
reservorios del virus que “persisten” en los tejidos; disregulación inmunológica;
reactivación de otros virus (Epstein Barr o Herpervirus 6, entre otros);
impacto del SARS-CoV-2 sobre la microbiota;
autoinmunidad;
trombos en los capilares con daño al endotelio;
señalización alterada en el tronco encefálico o el nervio vago.
En resumen, cuando hablamos de covid persistente no hablamos sólo de “cansancio”, sino de una confluencia de patologías que se pueden alargar temporalmente y devenir en enfermedades crónicas –como diabetes, enfermedad coronaria o demencia– de no tratarse a tiempo. Por eso es importante un diagnóstico certero.
Avances en diagnóstico y tratamiento
El diagnóstico se basa principalmente en la duración y persistencia de los síntomas relacionados con la covid-19 (fatiga, dificultad para respirar, dolor en el pecho y confusión mental, entre otros). La valoración suele ser clínica y se basa en la historia médica del paciente y en una evaluación física. Hasta la actualidad, no hay una prueba específica para diagnosticar la covid persistente, aunque un estudio reciente muestra que hay ciertos marcadores específicos en la sangre que se podrían utilizar para su diagnóstico.
Según la Guía Clínica para la atención al paciente con covid persistente (2022), se pueden realizar pruebas adicionales para descartar otras afecciones médicas que podrían estar contribuyendo a estos síntomas. Estas pruebas pueden incluir análisis de sangre específicos en función de los síntomas, estudios de imagen como la resonancia magnética, y pruebas de función pulmonar (espirometría).
En una revisión más actualizada (marzo del 2023), los autores explican que las herramientas de diagnóstico están en su mayoría en desarrollo. Una línea importante son las investigaciones sobre la identificación de biomarcadores que sugieren que los niveles de vesículas extracelulares (orgánulos que se liberan naturalmente de las células), y/o marcadores inmunológicos que indicarían una alta citotoxicidad, podrían ser indicativos de covid persistente.
En cuanto al tratamiento, actualmente no existe uno específico para la covid persistente. Hay diferentes terapias, que son efectivas en función de los síntomas a tratar. Muchos de los métodos curativos utilizados para las personas afectadas con encefalomielitis miálgica/síndrome de fatiga crónica o EM/CFS son efectivos para personas con covid persistente. Algunos suplementos han mostrado buenos resultados en el tratamiento tanto de covid persistente como de EM/SFC, incluyendo coenzima Q10 y d-ribosa, y pueden merecer un estudio adicional.
Resumen de tratamientos en función de los síntomas. Tabla modificada por Nuria E. Campillo del articulo de Davis et al. Nat. Rev. Microbiology 2023, 21, 133-146.
Hacer deporte con covid persistente puede ser contraproducente
Algunos expertos opinan que el ejercicio es perjudicial para los pacientes con covid persistente que tienen EM/SFC o malestar posesfuerzo y que no debe utilizarse como tratamiento. Se basan en un estudio en personas con covid persistente mostrando que la actividad física empeoró la condición del 75 % de los pacientes y menos del 1 % experimentó mejoría. Sin embargo, se necesitan más estudios en esta dirección, ya que en el caso de EM/SFC la terapia de ejercicio aeróbico gradual produce un efecto beneficioso.
En resumen, las opciones de tratamiento actuales se basan en estudios piloto a pequeña escala en covid persistente, o en lo que ha sido efectivo para otras enfermedades.
Todo esto nos muestra que el SARS-CoV-2 pasa por nuestro organismo dejando su huella, a veces mucho más duradera de lo que quisiéramos (no olvidemos que la ME/SFC suele ser un diagnóstico de por vida). Por suerte, gracias a muchos investigadores que han decidido no correr un tupido velo sobre la pandemia, sabemos mucho más sobre las secuelas del virus y cómo hacerlas desaparecer. Pero aún llevará un tiempo el tener una visión completa, tanto a nivel clínico como poblacional.
Referencia
Davis HE, McCorkell L, Moore Vogel JM,Topol EJ. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol[Internet].2023[citado 11 oct 2023]; 21: 133–146. https://doi.org/10.1038/s41579-022-00846-2
11 octubre 2023|Fuente: theconversation| Tomado de Noticias médicas
sep
19
 Aunque actualmente no existen curas para las enfermedades autoinmunes, los investigadores todavía están tratando de encontrar sus causas con la esperanza de desarrollar nuevos tratamientos.
Aunque actualmente no existen curas para las enfermedades autoinmunes, los investigadores todavía están tratando de encontrar sus causas con la esperanza de desarrollar nuevos tratamientos.
Los investigadores desarrollaron recientemente un nuevo tipo de vacuna llamada “vacuna inversa” que mostró potencial para revertir completamente las enfermedades autoinmunes en ratones.
Los científicos pudieron hacer esto sin desactivar el resto del sistema inmunológico.
Investigadores de la Escuela Pritzker de Ingeniería Molecular de la Universidad de Chicago dicen que han desarrollado un nuevo tipo de vacuna llamada «vacuna inversa» a través de un modelo de ratón.
La nueva vacuna pudo revertir por completo enfermedades autoinmunes como la esclerosis múltiple, la diabetes tipo 1 y la enfermedad de Crohn sin desactivar completamente el resto del sistema inmunológico de los ratones.
Se estima que 1 de cada 10 personas en todo el mundo tiene una enfermedad autoinmune, una afección en la que el sistema inmunológico ataca por error a células y tejidos sanos del cuerpo.
En general, actualmente no existen curas para las enfermedades autoinmunes. Los médicos utilizan una variedad de métodos, incluidos medicamentos, cirugía y cambios en el estilo de vida, para controlar los síntomas, a veces denominados «brotes».
Los investigadores aún desconocen las principales causas de las enfermedades autoinmunes. Sin embargo, sí saben que la genética, los factores ambientales y la exposición a ciertas infecciones virales pueden aumentar el riesgo de una persona.
Este estudio se publicó recientemente en la revista Nature Biomedical Engineering.
¿Cómo funciona una vacuna inversa?
Durante este estudio, los investigadores desarrollaron un nuevo tipo de vacuna llamada vacuna inversa.
Según el Dr. Jeffrey Hubbell, profesor de ingeniería de tejidos en la Escuela Pritzker de Ingeniería Molecular de la Universidad de Chicago y autor principal de este estudio, una vacuna regular induce la activación de las células inmunitarias para crear células que puedan matar células infectadas y generar anticuerpos. que pueden unirse y neutralizar virus que los infectarían.
«En cambio, una vacuna inversa puede debilitar dicha inmunidad», explicó Hubbell a Medical News Today.
«En una enfermedad autoinmune, buscamos vacunas inversas que puedan desactivar las células inmunes que han sido autorizadas erróneamente para atacar las propias células e incluso generar células que puedan actuar para reducir aún más la inmunidad, llamadas células T reguladoras», dijo. .
Mediante el uso de la vacuna inversa, los científicos pudieron hacer esto sin desactivar todo el sistema inmunológico del cuerpo.
«En la actualidad, las enfermedades autoinmunes se tratan de una manera que crea una supresión inmune inespecífica, en lugar de una modulación inmune específica de la enfermedad autoinmune», dijo Hubbell. «Claramente, es mejor tener un sistema inmunológico intacto y abordar las moléculas y células específicas que el cuerpo está atacando erróneamente».
«Además, esos enfoques inmunosupresores deben administrarse de forma crónica, mientras que un enfoque de vacuna tiene el potencial de ser duradero y, si la durabilidad es muy buena, incluso curativo», añadió.
Probando la vacuna inversa
Para este estudio, Hubbell y su equipo utilizaron un modelo de ratón de una enfermedad similar a la esclerosis múltiple llamada encefalomielitis autoinmune.
En ambas afecciones, el sistema inmunológico ataca por error a la mielina, que forma una funda protectora alrededor de los nervios del cuerpo, incluidos los de la médula espinal y el cerebro.
Cuando se administró la vacuna inversa, los científicos informaron que el sistema inmunológico dejó de atacar a la mielina. Esto permitió que los nervios comenzaran a funcionar correctamente y revirtió los síntomas de la enfermedad en los ratones.
«El cuerpo tiene una serie de mecanismos para prevenir la autoinmunidad», explicó Hubbell. “Uno de esos mecanismos previene las respuestas autoinmunes a nuestras propias células que envejecen y mueren. Estas células de la sangre son eliminadas por células especializadas del hígado y procesadas de una manera que induce y mantiene la tolerancia a esos restos de células moribundas”.
«En nuestro enfoque, hemos creado moléculas que parecen restos de células moribundas y contienen las proteínas que son atacadas en una enfermedad autoinmune particular», añadió. «Esto secuestra uno de los mecanismos que utiliza el cuerpo para mantener la tolerancia».
¿Qué es una enfermedad autoinmune?
Un sistema inmunológico sano protege al cuerpo de infecciones por virus y bacterias.
A veces, el sistema inmunológico está programado erróneamente para pensar que los tejidos o células sanos del cuerpo son organismos dañinos que necesita atacar. Esto es lo que causa una enfermedad autoinmune.
Existen más de 100 enfermedades autoinmunes. Algunos de los más conocidos son:
esclerosis múltiple, Diabetes tipo 1, artritis reumatoide, lupus, enfermedad celíaca, Enfermedad de Crohn, Tiroiditis de Hashimoto, Síndrome de Sjogren, Enfermedad inflamatoria intestinal, soriasis.
Las enfermedades autoinmunes son enfermedades crónicas. Cada uno tiene sus propios síntomas específicos, aunque la mayoría tiene algunos síntomas comunes como dolor, fatiga, debilidad muscular e inflamación o hinchazón en diferentes partes del cuerpo.
Aunque cada enfermedad autoinmune afecta a una persona de manera diferente, investigaciones anteriores muestran que las personas que tienen una enfermedad autoinmune tienen un mayor riesgo de sufrir enfermedades cardíacas, depresión, daño a órganos y cáncer.
Próximos pasos en la investigación de enfermedades autoinmunes
Cuando se le preguntó qué tan rápido podríamos ver una vacuna inversa para enfermedades autoinmunes disponible para que la usen los médicos, Hubbell dijo que ya se han iniciado las pruebas clínicas para ciertas afecciones.
«El enfoque general presentado en este artículo se encuentra actualmente en pruebas clínicas en la enfermedad celíaca y la esclerosis múltiple, y estamos muy emocionados de ver los resultados que surgirán de esos estudios», dijo. «En mi laboratorio, estamos explorando eso en enfermedades autoinmunes como la esclerosis múltiple, la diabetes tipo 1, el asma alérgica y la alergia alimentaria, así como en la prevención de la inmunidad a los medicamentos utilizados para tratar enfermedades congénitas, que a menudo son inmunogénicas».
Medical News Today también habló con la Dra. Barbara Giesser, neuróloga y especialista en esclerosis múltiple del Pacific Neuroscience Institute del Providence Saint John’s Health Center en California, sobre este estudio.
«Este es un estudio de prueba de concepto en un modelo animal de enfermedad desmielinizante», explicó. “Sugiere que, en lugar de suprimir el sistema inmunológico, el daño a los nervios en la EM podría prevenirse ‘desensibilizando’ ciertas células inmunes a una proteína de mielina. Esto puede tener la ventaja de no aumentar la susceptibilidad a la infección, lo cual es un problema con algunas de las terapias modificadoras de enfermedades más inmunosupresoras que se utilizan actualmente”.
«Este es un estudio preliminar en un modelo de ratón y se necesitan ensayos en humanos para determinar si este enfoque es seguro y eficaz en las personas».
— Dra. Bárbara Giesser
Referencia
Tremain AC, Wallace RP, Lorentz KM, Thornley TB, Antane J, Raczy MR, et al. Synthetically glycosylated antigens for the antigen-specific suppression of established immune responses. Nat Biomed Eng. 2023; 1142–1155. https://doi.org/10.1038/s41551-023-01086-2
https://pubmed.ncbi.nlm.nih.gov/37679570/
17/09/2023
Fuente: (Medical News Today)
may
23
La disfagia (dificultad de grado variable para tragar alimentos sólidos y líquidos) es el síntoma más común en los pacientes con esofagitis eosinofílica a partir de los 12 años, y su frecuencia aumenta en la edad adulta, alcanzando al 84 por ciento en los pacientes diagnosticados a partir de los 60 años.
Así se refleja en un estudio en el que han participado 35 investigadores de cuatro países pertenecientes al ´European Consortium for Eosinophilic Disesases ot the Gastrointestinal Tract (EUREOS)´, coordinados por su presidente, Alfredo J. Lucendo, jefe de Sección de Aparato Digestivo del Hospital de Tomelloso (Ciudad Real).
La investigación ha analizado datos de 1.300 pacientes para comparar las características de la enfermedad en niños y adultos y se ha presentado con motivo del día europeo de la enfermedad, que tiene lugar este lunes.
La esofagitis eosinofílica es una enfermedad crónica mediada por el sistema inmune, que provoca una inflamación del esófago tras su exposición a diferentes componentes de la dieta o, en menor medida, del ambiente. Así, representa la principal causa de disfagia e impactación de alimentos en niños y en adultos jóvenes.
Sus síntomas son complejos y varían ampliamente con la edad de los pacientes, de manera que, en los niños más pequeños, causa principalmente náuseas y vómitos, dolor torácico o abdominal, alimentación lenta, aversión a la comida y, en ocasiones, pérdida de peso. En contraste, la disfagia, la impactación de alimentos en esófago (atragantamientos) y la acidez esofágica son síntomas significativamente más comunes entre los adultos.
El doctor Alfredo J. Lucendo explica que la disfagia, como principal manifestación clínica de esta enfermedad, «es una sensación subjetiva manifestada como dificultad o molestia al tragar y, en el caso de la esofagitis eosinofílica, puede originarse por una reducción del calibre del esófago, o por diversos trastornos motores».
A su juicio, aún se necesita «mucha concienciación» a los médicos de todos los niveles asistenciales y las autoridades sanitarias sobre la importancia de la disfagia y la necesidad de reconocer esta enfermedad como la principal causa de disfagia en niños y adultos hasta los 50 años.
Por ello, Lucendo ha reclamado mayor inversión en investigación para la esofagitis eosinofílica. «No es aceptable que, tras 30 años desde la descripción de la enfermedad, solo contemos con un fármaco aprobado para tratarla, y restringido a algunos pacientes adultos que reúnen ciertas características un tanto arbitrarias definidas por el Ministerio de Sanidad», ha apuntado.
Varios años para tener un diagnóstico
El estudio describe que el tiempo de retraso diagnóstico de la esofagitis eosinofílica en adultos es el doble que en menores y adolescentes.
Concretamente, mientras el tiempo de diagnóstico de los pacientes pediátricos está alrededor de 30 meses (2,5 años), en los adultos este retraso puede llegar a los 62 meses (5 años).
No obstante, también se especifica en el estudio que esta demora se ha reducido en la mayoría de los centros de Europa a la mitad durante la última década, según los datos aportados por la red de investigadores de EUREOS.
Por su parte, la presidenta de la Asociación de Pacientes de Esofagitis Eosinofílica (Aedeseo), Miriam Espinosa, manifiesta que «para el paciente con EOE, el momento de la comida se convierte en una situación asociada al miedo, incertidumbre, dolor y finalmente sufrimiento, al tener dificultad o no poder comer muchos alimentos».
«La persona se siente, muchas veces, limitada y aislada, ya que las actividades sociales y familiares suelen estar centradas en la comida. La oscuridad que supone todo lo relacionado con la comida puede ser abrumadora, llevando, muchas veces, a una sensación de tristeza y depresión», ha advertido.
Mayo 23/2023 (IMmédico) – Tomado de Atención primaria, Gastroenterología – Digestivo Copyright 2023: Publimas Digital

