feb
23
 La serotonina influye directamente en las conexiones sinápticas excitadoras nacientes e inmaduras en la corteza prefrontal, que si se interrumpen o desregulan durante el desarrollo temprano pueden contribuir a diversos trastornos de salud mental.
La serotonina influye directamente en las conexiones sinápticas excitadoras nacientes e inmaduras en la corteza prefrontal, que si se interrumpen o desregulan durante el desarrollo temprano pueden contribuir a diversos trastornos de salud mental.
El desarrollo del cerebro requiere una interacción precisa de neuroquímicos que median la comunicación neuronal y la formación de circuitos. El 5-HT es uno de los neuromoduladores detectados más tempranamente, cuyos niveles corticales alcanzan su punto máximo dos años después del nacimiento en humanos y la primera semana posnatal en roedores.
Los cambios en los niveles gestacionales y posnatales tempranos de 5-HT pueden deberse a muchas causas, entre ellas la privación o el abuso materno, las dietas altas o bajas en triptófano o el uso de medicamentos como los inhibidores selectivos de la recaptación de serotonina (ISRS) que pueden atravesar fácilmente la placenta o pasar a la descendencia a través de la lactancia materna.
En este terreno, un estudio dirigido por investigadores del Campus Médico Anschutz de la Universidad de Colorado (EEUU) se centró en el efecto de la fluoxetina, comúnmente utilizada en medicamentos como Prozac y Sarafem para tratar la depresión y la depresión perinatal, en la corteza prefrontal en desarrollo de ratones, y en observar el impacto que tiene la serotonina en el desarrollo de la corteza prefrontal.
«Si bien se sabe que la serotonina desempeña un papel en el desarrollo del cerebro, los mecanismos responsables de esta influencia, específicamente en la corteza prefrontal, no están claros», aseguró el autor principal, Won Chan Oh, profesor asistente en el Departamento de Farmacología de CU Anschutz.
Los investigadores pudieron constatar que la serotonina influye directamente en las conexiones sinápticas excitadoras nacientes e inmaduras en la corteza prefrontal, que si se interrumpen o desregulan durante el desarrollo temprano pueden contribuir a diversos trastornos de salud mental.
«Nuestra investigación descubre los procesos específicos a nivel sináptico que explican cómo la serotonina contribuye al desarrollo de esta importante región del cerebro durante la exposición a la fluoxetina en las primeras etapas de la vida. Somos los primeros en proporcionar evidencia experimental del impacto directo de la serotonina en la corteza prefrontal en desarrollo en ratones», según el prof. Won Chan Oh.
Para estudiar el efecto, los investigadores observaron el impacto de la deficiencia y el exceso de serotonina en el desarrollo del cerebro en ratones. Descubrieron que la serotonina no sólo participa en la función cerebral general, sino que también tiene un papel específico al influir en cómo las conexiones individuales entre las neuronas cambian y se adaptan, contribuyendo a la capacidad del cerebro para aprender y adaptarse.
«Comprender esta correlación tiene el potencial de ayudar con la intervención temprana y el desarrollo de nuevas terapias para los trastornos del desarrollo neurológico que involucran la desregulación de la serotonina», indicó el prof. Won Chan Oh
Los investigadores planean, a partir de aquí, continuar estudiando el impacto de la fluoxetina y luego examinar su impacto en un cerebro en desarrollo más adelante en la vida.
23 febrero 2024| Fuente: Immédico| Tomado de |Noticia
ago
24
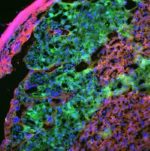 Investigadores de la Universidad de Cambridge han obtenido las primeras evidencias de que, durante el embarazo, el feto utiliza un gen paterno para controlar el suministro de nutrientes desde la placenta.
Investigadores de la Universidad de Cambridge han obtenido las primeras evidencias de que, durante el embarazo, el feto utiliza un gen paterno para controlar el suministro de nutrientes desde la placenta.
Durante el embarazo, el metabolismo materno se adapta para suministrar nutrientes que favorezcan el crecimiento y desarrollo fetal. La placenta, órgano temporal formado por células del feto y de la madre, actúa como intermediaria entre la madre y el feto y facilita el intercambio de nutrientes y oxígeno entre ambos. Conforme progresa el embarazo, el feto aumenta sus demandas de nutrientes para promover su crecimiento, lo que se opone, en cierto modo, a las necesidades maternas de mantener los nutrientes necesarios para su salud y prepararse para la lactancia y posibles posteriores embarazos.
A partir de estudios en ratones un equipo de la Universidad de Cambridge ha encontrado que IGF2, una señal endocrina similar a la insulina, modifica el metabolismo materno y distribución de recursos hacia el feto. Además, la señalización mediada por Igf2 participa en el desarrollo de diversos tejidos como la placenta, el hígado y el cerebro. En un estudio previo, el equipo había identificado el papel de IGF2 en el desarrollo de la vasculatura de la placenta para adaptarse al crecimiento del embrión.
Un gen de expresión paterna
Interesantemente, IGF2 está codificada por un gen con impronta genómica, de forma que únicamente la copia paterna está activa en la placenta. “Si la función de Igf2 del padre es inactivada en las células señalizadoras, la madre no produce suficiente cantidad de glucosa y lípidos disponible para su circulación”, señala Jorge Lopez-Tello, Investigador en el Departamento de Fisiología, Desarrollo y Neurociencia, así como primer firmante del trabajo, publicado en Cell Metabolism. “Por lo tanto, estos nutrientes llegan al feto en cantidades insuficientes y el feto no crece adecuadamente”.
Los investigadores plantean que la expresión de Igf2 con impronta genética en la placenta puede haber evolucionado como una estrategia para movilizar nutrientes hacia el feto en crecimiento. En este contexto, Igf2 y placenta tienen un papel central en el conflicto materno-fetal por los recursos maternos.
Impacto a largo plazo de los defectos en Igf2
Los investigadores también han determinado que la reducción en la señalización mediada por Igf2 en la placenta tiene consecuencias metabólicas postnatales. Los ratones deficientes para Igf2 mostraron un crecimiento restringido e hipoglucémico, con efectos que se extendieron a la edad adulta.
“Nuestra investigación pone de relieve lo importante que es la distribución controlada de nutrientes hacia el feto para la salud de la descendencia a lo largo de toda su vida, y el papel directo que desempeña la placenta”, ha señalado Amanda Sferruzzi, catedrática en Fisiología Fetal y de la Placenta en la Universidad de Cambridge. “La placenta es un órgano asombroso. Al final del embarazo, la madre expulsa la placenta, pero los recuerdos de cómo estaba funcionando la placenta dejan un legado duradero en la forma en que se han desarrollado los órganos fetales y en cómo van a funcionar a lo largo de la vida”.
El siguiente paso de los investigadores será determinar con mayor detalle cómo Igf2 controla las hormonas de la placenta implicadas en regulación de nutrientes y crecimiento de los órganos e identificar la función exacta de estas hormonas.
Fuente: Genética Médica News
Referencia: Lopez-Tello J, et al. Fetal manipulation of maternal metabolism is a critical function of the imprinted Igf2 gene. Cell Metab. 2023 Jul 11;35(7):1195-1208.e6. doi: http://dx.doi.org/10.1016/j.cmet.2023.06.007
https://www.sciencedirect.com/science/article/pii/S1550413123002176?via%3Dihub
oct
26
Una investigación de la Universidad Politécnica de Madrid y el Hospital Universitario de Torrejón establece que la práctica de ejercicio físico moderado por parte de la madre mejora la respuesta del corazón del feto y favorece una mejor recuperación del peso tras el parto. Read more
ene
17
Científicos de Cambridge han identificado una señal clave que el feto utiliza para controlar su suministro de nutrientes desde la placenta, lo que revela un tira y afloja entre los genes heredados del padre y de la madre. El estudio, realizado en ratones, podría explicar por qué algunos bebés no se desarrollan correctamente en el útero. Read more
oct
9
La afectación placentaria, causada por la infección del SARS-CoV-2, produce un comportamiento anómalo del flujo sanguíneo entre la madre y el bebé en desarrollo, debido a la necrosis del trofoblasto. Investigadores españoles han observado que, a pesar de que resulta muy infrecuente, puede ser mortal para el feto. Read more
ago
13
Cuando las luces de los estadios de Brasil se apagaron y terminó la Copa Mundial de la FIFA, en 2014, el virus del Zika quedó instalado en América Latina. Nunca se había registrado un brote de este virus -que se transmite por el mismo mosquito que propaga el dengue- de forma tan virulenta como hasta entonces. Un año después, una alarmante cantidad de bebés nacieron con microcefalia: aunque los síntomas del virus son leves, la infección se agrava si se contagian mujeres embarazadas, ya que atraviesa la placenta y provoca defectos y malformaciones en el cerebro del feto. Read more

