feb
5
 Investigadores del Instituto del Monte de Neurociencia de la Universidad de Rochester (EE.UU.) han descubierto que la microglía puede desencadenar déficits cognitivos tras la exposición a la radiación y puede ser un objetivo clave para prevenir estos síntomas. Estos resultados, que se han publicado en International Journal of Radiation Oncology Biology Physics, se basan en estudios anteriores que demuestran que, tras la exposición a la radiación, la microglía daña las sinapsis, básicas para el comportamiento cognitivo y la memoria.
Investigadores del Instituto del Monte de Neurociencia de la Universidad de Rochester (EE.UU.) han descubierto que la microglía puede desencadenar déficits cognitivos tras la exposición a la radiación y puede ser un objetivo clave para prevenir estos síntomas. Estos resultados, que se han publicado en International Journal of Radiation Oncology Biology Physics, se basan en estudios anteriores que demuestran que, tras la exposición a la radiación, la microglía daña las sinapsis, básicas para el comportamiento cognitivo y la memoria.
Mediante varias pruebas de comportamiento, los investigadores estudiaron la función cognitiva de ratones antes y después de la exposición a la radiación. Los ratones hembra obtuvieron los mismos resultados en todas las pruebas, lo que indica una resistencia a las lesiones por radiación. Sin embargo, los ratones macho no podían recordar o realizar ciertas tareas tras la exposición a la radiación. Este deterioro cognitivo se correlaciona con la pérdida de sinapsis y la evidencia de un exceso de reactividad microglial potencialmente perjudicial tras el tratamiento. Los investigadores se centraron entonces en una vía de la microglía importante para la eliminación de sinapsis. Los ratones con esta microglía mutante no sufrieron deterioro cognitivo tras la radiación. Y otros a los que se administró Leukadherin-1, capaz de bloquear esta misma vía, tampoco sufrieron deterioro cognitivo.
Los investigadores aseguran que esta investigación ofrece una posible diana para desarrollar terapias que prevengan o mitiguen tales déficits en las personas que necesitan radioterapia cerebral.
Ver artículo: Hinkle JJ, Olschowka JA, Willianms JP, O’Banion MK. Pharmacologic Manipulation of Complement Receptor 3 Prevents Dendritic Spine Loss and Cognitive Impairment After Acute Cranial Radiation. Int J Radiat Oncol Biol Phys [ Internet]. 2023[ citado 4 feb 2024]; 16(23): DOI:https://doi.org/10.1016/j.ijrobp.2023.12.017
10 enero 2024| Fuente: Neurología.com| Tomado de | Noticia
ene
11
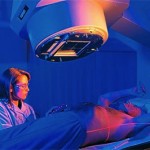 Investigadores del Instituto del Monte de Neurociencia de la Universidad de Rochester (EE.UU.) han descubierto que la microglía puede desencadenar déficits cognitivos tras la exposición a la radiación y puede ser un objetivo clave para prevenir estos síntomas. Estos resultados, que se han publicado en International Journal of Radiation Oncology Biology Physics, se basan en estudios anteriores que demuestran que, tras la exposición a la radiación, la microglía daña las sinapsis, básicas para el comportamiento cognitivo y la memoria.
Investigadores del Instituto del Monte de Neurociencia de la Universidad de Rochester (EE.UU.) han descubierto que la microglía puede desencadenar déficits cognitivos tras la exposición a la radiación y puede ser un objetivo clave para prevenir estos síntomas. Estos resultados, que se han publicado en International Journal of Radiation Oncology Biology Physics, se basan en estudios anteriores que demuestran que, tras la exposición a la radiación, la microglía daña las sinapsis, básicas para el comportamiento cognitivo y la memoria.
Mediante varias pruebas de comportamiento, los investigadores estudiaron la función cognitiva de ratones antes y después de la exposición a la radiación. Los ratones hembra obtuvieron los mismos resultados en todas las pruebas, lo que indica una resistencia a las lesiones por radiación. Sin embargo, los ratones macho no podían recordar o realizar ciertas tareas tras la exposición a la radiación. Este deterioro cognitivo se correlaciona con la pérdida de sinapsis y la evidencia de un exceso de reactividad microglial potencialmente perjudicial tras el tratamiento. Los investigadores se centraron entonces en una vía de la microglía importante para la eliminación de sinapsis. Los ratones con esta microglía mutante no sufrieron deterioro cognitivo tras la radiación. Y otros a los que se administró Leukadherin-1, capaz de bloquear esta misma vía, tampoco sufrieron deterioro cognitivo.
Los investigadores aseguran que esta investigación ofrece una posible diana para desarrollar terapias que prevengan o mitiguen tales déficits en las personas que necesitan radioterapia cerebral.
Referencia: Hinkle JJ, Olschowka JA, Williams JP, Banion MK. Pharmacologic manipulation of complement receptor 3 prevents dendritic spine loss and cognitive impairment after acute cranial radiation. Int J Radiat Oncol Biol Phys[Internet]. 2023[citado 10 ene 2024]; 22:S0360-3016(23)08254-8. doi: 10.1016/j.ijrobp.2023.12.017.
11 enero 2024| Fuente: Neurología.com| Tomado de | Noticia
nov
30
 Un estudio liderado por la Universidad de Barcelona (UB) ha identificado en ratones una proteína, conocida como receptor inmunológico CD300f, que cuando no está presente, se tiende a una esperanza de vida más corta y a patologías asociadas al deterioro cognitivo y el envejecimiento prematuro.
Un estudio liderado por la Universidad de Barcelona (UB) ha identificado en ratones una proteína, conocida como receptor inmunológico CD300f, que cuando no está presente, se tiende a una esperanza de vida más corta y a patologías asociadas al deterioro cognitivo y el envejecimiento prematuro.
Según ha explicado la UB este martes en un comunicado, el estudio de esa proteína presente en células del sistema inmune abre la puerta a conocer más profundamente los procesos de la neurodegeneración en humanos. ‘Nuestro estudio pone en evidencia que alteraciones en células del sistema inmune pueden determinar el grado de envejecimiento saludable en ratones’, ha destacado el investigador que ha liderado el trabajo, Hugo Peluffo, que es miembro de la Facultad de Medicina y Ciencias de la Salud de la UB y del Instituto de Neurociencias de la misma universidad (UBneuro).
Comprender cómo la proteína CD300f puede determinar por sí sola el ritmo de aparición de patologías asociadas al envejecimiento puede ayudar a entender mejor esos procesos y contribuir a diseñar estrategias para regular su acción, ha apuntado Peluffo.
El receptor CD300f es una proteína expresada en células del sistema inmune que modula la inflamación y el metabolismo celular, y el presente estudio revela las primeras evidencias de su papel en el envejecimiento.
El estudio se basa en un seguimiento detallado de distintos grupos de ratones durante 30 meses, una innovación metodológica que ha permitido reflejar el proceso de envejecimiento real de esos animales sin usar modelos de envejecimiento acelerado, que no representan fielmente una acumulación gradual de cambios de edad.
A partir de ahora, el equipo del investigador Peluffo acaba de ganar una de las becas de investigación en alzhéimer de la Fundación Pasqual Maragall, en el que estudiarán el posible papel del receptor inmunológico CD300f en la aparición de esa enfermedad.
La investigación, publicada en la revista ‘Cell Reports’, ha contado con la participación de equipos del Centro Uruguayo de Imagenología Molecular (CUDIM), entre otras instituciones.
Ver más información:
Frances E, Alı´-Ruiz D, Rego N, Malagelada C, Escande C, Peluffo H, et al. CD300f immune receptor contributes to healthy aging by regulating inflammaging, metabolism, and cognitive decline. Cell Reports[Internet].2023[citado 29 nov 2023]; 42(10): 113269. https://doi.org/10.1016/j.celrep.2023.113269
30 noviembre 2023 |Fuente: EFE | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina
nov
1
 La prolongada es un deterioro común post-Covid 19.
La prolongada es un deterioro común post-Covid 19.
Los efectos a largo plazo de la COVID-19 sobre la función cognitiva se han convertido en un área de creciente preocupación. Este artículo proporciona una descripción general de las características, factores de riesgo, posibles mecanismos y estrategias de manejo de la disfunción cognitiva en la condición post-COVID-19 (PCC).
La disfunción cognitiva prolongada es uno de los deterioros más comunes en la condición post-COVID-19 (PCC), afecta entre el 17% y el 28% de los individuos más de 12 semanas después de la infección y persiste en algunos casos durante varios años.
Las disfunciones cognitivas pueden manifestarse como una amplia gama de síntomas que incluyen deterioro de la memoria, déficit de atención, disfunción ejecutiva y velocidad de procesamiento reducida.
Los factores de riesgo para desarrollar PCC, con o sin deterioro cognitivo, incluyen la edad avanzada, las condiciones médicas preexistentes y la gravedad de la enfermedad aguda. Los mecanismos subyacentes aún no están claros, pero los contribuyentes propuestos incluyen neuroinflamación, hipoxia, daño vascular y reactivación del virus latente, sin excluir la posibilidad de una invasión viral directa del sistema nervioso central, lo que ilustra una patología viral compleja.
Síntomas cognitivos
Las funciones de atención permiten la capacidad de procesar información de nuestro entorno y se consideran de naturaleza jerárquica. La atención focalizada y la atención sostenida se consideran funciones de atención fundamentales. Los niveles más altos de atención dependen de funciones ejecutivas y abarcan atención alterna, selectiva y dividida. A pesar de su nombre, la memoria de trabajo también se considera una función de la atención y desempeña un papel importante en la codificación de la memoria y la recuperación de información almacenada en la memoria a largo plazo.
Dado que las funciones de atención sirven como procesos y subsistemas cognitivos fundamentales para otras funciones cognitivas, son cruciales para gestionar nuestra vida cotidiana. Las funciones de atención deterioradas, incluso en los casos de deficiencias leves, afectan directamente el rendimiento tanto en las tareas cotidianas como en la vida laboral.
Las funciones de atención se asocian frecuentemente con la velocidad de procesamiento. Desde una perspectiva neuroanatómica, el tálamo desempeña un papel crucial como centro de redes que respaldan procesos relacionados con la atención, el procesamiento de información, la memoria y las funciones ejecutivas. Sin embargo, en los estudios realizados hasta el momento sobre la COVID-19 no se ha determinado cuál de las funciones de atención se ve más afectada en el PCC, ni en qué medida otras disfunciones cognitivas son independientes o están vinculadas a funciones de atención disminuidas.
Las deficiencias en la atención, la memoria de trabajo y las funciones ejecutivas a menudo tienen efectos secundarios en las pruebas que evalúan la codificación y recuperación de la memoria. En consecuencia, la memoria episódica puede verse afectada indirectamente por el tipo de daño neurológico causado por enfermedades virales, principalmente a través de reducciones en la atención y la velocidad de procesamiento necesarias para la codificación. En el contexto del PCC, aún no está completamente establecido si los resultados observados en las pruebas de memoria se deben a dificultades primarias en el almacenamiento de la memoria o si son efectos secundarios resultantes de un deterioro de la atención y/o de la memoria de trabajo.
Fatiga
La fatiga es un síntoma destacado tanto en el COVID-19 agudo como en el PCC. Las tasas de prevalencia de fatiga post-COVID oscilan entre el 32 % y el 46 % en diferentes estudios y en el metanálisis de seguimientos de 1 año entre el 18 % y el 39 %. Sin embargo, la fatiga es un síntoma multifactorial y vagamente definido presente en diversas afecciones, incluidos trastornos neurológicos, dolor crónico y depresión. También se ha informado de fatiga posinfecciosa después de otras epidemias virales.
En la mayoría de los estudios, la fatiga se informa subjetivamente mediante escalas de autoevaluación diseñadas para capturar un nivel bajo de energía que no es proporcional al nivel de actividad del individuo y que no se alivia con el descanso o el sueño normales. Actualmente, no existe una escala de fatiga validada específicamente para la fatiga post-COVID.
Como COVID-19 es una afección nueva, no es evidente si la fatiga experimentada en el PCC es equivalente y comparte los mismos mecanismos subyacentes que la fatiga en las afecciones neurológicas. En condiciones neurológicas, la disminución de la atención, la disminución de la velocidad de procesamiento y la fatigabilidad se han relacionado con la experiencia de fatiga, pero también han mostrado correlaciones significativas con la depresión y los trastornos del sueño.
Abordaje
Como la variación individual de los deterioros cognitivos es grande, se requiere un examen neuropsicológico y un enfoque multidimensional centrado en la persona. Según la Organización Mundial de la Salud, la evidencia limitada sobre los deterioros cognitivos relacionados con la COVID-19 requiere la implementación de intervenciones de rehabilitación a partir de prácticas establecidas para condiciones similares.
Se recomienda psicoeducación y entrenamiento en habilidades compensatorias. Podrían ser útiles los productos de asistencia y las modificaciones ambientales adaptadas a las necesidades individuales.
En disfunciones específicas de la atención y la memoria de trabajo, el entrenamiento cognitivo (cuidadosamente controlado en cuanto a su intensidad) podría ser eficaz para las personas que no sufren malestar post-esfuerzo.
Es crucial realizar más investigaciones para intervenciones basadas en evidencia específicas para los deterioros cognitivos relacionados con la COVID-19.
Conclusiones
La disfunción cognitiva prolongada es un deterioro común que afecta a las personas con PCC. Los factores de riesgo del PCC en general incluyen el sexo femenino, la edad, las condiciones médicas preexistentes y la gravedad de la enfermedad aguda.
Los mecanismos propuestos que contribuyen al PCC y los deterioros cognitivos incluyen neuroinflamación, hipoxia, daño vascular, reactivación viral latente e invasión viral directa del sistema nervioso central.
El manejo de la disfunción cognitiva en el PCC requiere un enfoque multidimensional que incluya un examen neuropsicológico y rehabilitación individualizada. Aunque la evidencia específica sobre los deterioros cognitivos relacionados con la COVID-19 es limitada, se pueden implementar intervenciones basadas en prácticas establecidas para otras afecciones neurológicas. La OMS recomienda educación, entrenamiento de habilidades, ejercicios cognitivos, productos de asistencia y modificaciones ambientales.
Se recomienda un entrenamiento funcional con un cuidadoso control de la intensidad para las personas que no padecen PEM. Es esencial realizar más investigaciones para intervenciones basadas en evidencia específicas para los deterioros cognitivos relacionados con la COVID-19.
Referencia
Möller M, Borg K, Janson C, Lerm M, Normark J, Niward K, et al. Cognitive dysfunction in post-COVID-19 condition: Mechanisms, management, and rehabilitation. J Intern Med [Internet]. 2023[citado 31 oct 2023]; ;294(5):563-581. doi: 10.1111/joim.13720.
1 noviembre 2023| Fuente: IntraMed |Tomado de Noticias biomédicas
oct
30
 Cada duplicación de los niveles de triglicéridos se asocia con un riesgo 18% menor de desarrollar demencia personas de mayor edad, pero no es probatoria de prevención.
Cada duplicación de los niveles de triglicéridos se asocia con un riesgo 18% menor de desarrollar demencia personas de mayor edad, pero no es probatoria de prevención.
Poblaciones de mayor edad que presentan niveles más elevados de triglicéridos podrían tener un menor riesgo de demencia y un proceso de deterioro cognitivo más lento en el tiempo en comparación con las personas de más edad que tienen niveles más bajos, según los datos de una nueva investigación que acaba de publicarse en Neurology. Sin embargo, aunque el estudio ha encontrado un vínculo, no prueba que niveles más altos de triglicéridos prevengan la demencia.
Los triglicéridos, ácidos grasos que suponen el tipo de grasa más común en sangre, constituyen hasta el 95 % de las grasas de la dieta, que son la principal fuente de energía del cerebro.
Predictor útil en este subgrupo
Según el principal autor del trabajo, Zhen Zhou, profesor de la Universidad de Monash en Melbourne, Australia, los niveles más altos de triglicéridos pueden reflejar una mejor salud general y comportamientos de estilo de vida que protegerían contra la demencia. Los datos de sus hallazgos sugieren que «los niveles de triglicéridos pueden servir como un predictor útil del riesgo de demencia y deterioro cognitivo en poblaciones de mayor edad».
Con datos de asistencia médica se identificaron 18 294 personas con una edad promedio de 75 años que no tenían un diagnóstico previo de enfermedad de Alzheimer o demencia. Los participantes fueron seguidos durante un promedio de seis años, tiempo durante el que 823 personas desarrollaron demencia.
Se analizaron anualmente las mediciones de colesterol total, triglicéridos, colesterol de lipoproteínas de baja densidad (c-LDL) y colesterol de lipoproteínas de alta densidad (c-HDL).
Asimismo, los investigadores dividieron a los participantes en cuatro grupos según los niveles de triglicéridos en ayunas. Del grupo total, el promedio de triglicéridos fue de 106 miligramos por decilitro (mg/dL). Para los adultos, un nivel normal o saludable de triglicéridos es inferior a 150 mg/dL.
Después de ajustar las variables que podrían afectar el riesgo de demencia, incluida la educación y los tratamientos con hipolipemiantes, los profesionales encontraron que cada duplicación de los niveles de triglicéridos se asociaba con un riesgo 18 % menor de desarrollar demencia.
El grupo de triglicéridos más bajos tenía niveles de menos de 62 mg/dL. El segundo grupo tenía niveles de 63 a 106 mg/dL. En comparación con el grupo más bajo, el segundo grupo tenía un 15% menos de probabilidades de desarrollar demencia. El tercer grupo tenía niveles de 107 a 186 mg/dL. En comparación con el grupo más bajo, tenían un 24 % menos de probabilidades de desarrollar demencia. El cuarto grupo tenía niveles de 187 mg/dL o más. En comparación con el grupo más bajo, tenían un 36 % menos de probabilidades de desarrollar demencia.
De las 1.416 personas del grupo con triglicéridos más bajos, 82 personas (el 6 %), desarrollaron demencia y de las 7.449 del segundo grupo, 358 personas (el 5 %), la desarrollaron. De las 7 312 que componían el tercer grupo, 310 (el 4 %), evolucionaron a demencia. Por último, desarrolló demencia el 3 %, 73 personas, del cuarto grupo compuesto por 2 117 personas.
Tener triglicéridos elevados entre ingestas aumenta el deterioro cardiovascular
El riesgo de los triglicéridos es más elevado en mujeres
La actividad del tejido adiposo marrón controla el metabolismo de las lipoproteínas ricas en triglicéridos
Los investigadores también validaron sus resultados en otro conjunto de datos compuesto por 68 200 personas mayores del Reino Unido. Entre ellas, 2 778 personas desarrollaron demencia en un tiempo promedio de 12 años, observándose un resultado consistente que muestra una reducción del 17 % en el riesgo de demencia con cada duplicación de los niveles de triglicéridos.
El trabajo también ha detectado que los niveles más altos de triglicéridos se asociaban con una más lenta disminución en la cognición compuesta; un resultado combinado de pruebas de función global, velocidad psicomotora, lenguaje y función ejecutiva y memoria a lo largo del tiempo.
Una limitación del estudio, apoyado por el Real Colegio Australiano de Médicos Generales y la Fundación de Investigación HCF, fue que solo se observó a personas de 65 años o más que inicialmente no tenían problemas cognitivos, por lo que «los hallazgos no son generalizables a otras poblaciones», considera Zhou, que especifica que necesitan estudios futuros para investigar si «componentes específicos de los triglicéridos pueden promover una mejor función cognitiva, con la esperanza de desarrollar nuevas estrategias preventivas».
Referencia
Zhou Z, Ryan J, Tonkin AM, Zoungas S, Lacaze P, Wolfe R, et al. Association Between Triglycerides and Risk of Dementia in Community-Dwelling Older Adults: A Prospective Cohort Study. Neurology[Internet]. 2023[citado 29 oct 2023]. 10.1212/WNL.0000000000207923; DOI: 10.1212/WNL.0000000000207923
30 octubre 2023 | Fuente: Diario Médico| Tomado de Neurología
oct
23
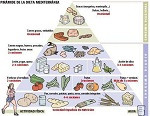 Las mujeres que en la mediana edad (40-60 años) siguen dietas saludables son menos propensas a presentar pérdida de memoria y otros deterioros cognitivos en la vejez, según un estudio basado en el seguimiento médico de más de 5.000 mujeres durante 30 años, y que hoy publica la revista científica Alzheimer’s & Dementia.
Las mujeres que en la mediana edad (40-60 años) siguen dietas saludables son menos propensas a presentar pérdida de memoria y otros deterioros cognitivos en la vejez, según un estudio basado en el seguimiento médico de más de 5.000 mujeres durante 30 años, y que hoy publica la revista científica Alzheimer’s & Dementia.
La investigación, dirigida por científicos de las facultades de medicina de la Universidad de Nueva York y de Columbia, concluye que la modificación del estilo de vida de las mujeres en la mediana edad -con dietas en las que abunden alimentos vegetales ricos en potasio, calcio y magnesio, y haya una mínima cantidad de grasas saturadas, sodio y azúcar- repercute en una mejora de la función cognitiva a partir de los 60 años.
Los científicos han analizado los datos de 5 116 mujeres de las más de 14 000 inscritas en el Estudio de Salud de la Mujer de la Universidad de Nueva York, uno de los más antiguos de este tipo que examina el impacto del estilo de vida y otros factores en el desarrollo de los cánceres más comunes entre las mujeres, así como otras enfermedades crónicas. En su análisis, tomaron como referencia los datos que las participantes dieron sobre su alimentación en cuestionarios llevados a cabo entre 1985 y 1991, cuando se inscribieron en el estudio y tenían, de media, 49 años. La salud de las participantes fue seguida durante más de 30 años (edad media de 79 años), con especial atención a cualquier deterioro cognitivo sufrido cuando se iban haciendo mayores.
Entre otros, realizaron un cuestionario con seis preguntas médicas estándar que son indicativas de un posterior deterioro cognitivo leve, que desemboca en demencia; y que abordan las dificultades para recordar acontecimientos recientes o listas de la compra, comprender instrucciones orales, conversaciones en grupo, o moverse por calles conocidas. En el resultado se vio un detalle significativo: las mujeres que llevaron una dieta más sana de jóvenes, eran un 17 % menos propensas a manifestar deterioro cognitivo de mayores. ‘Tras más de 30 años de seguimiento, hemos visto que cuanto mayor es la prevalencia de una dieta saludable en la mediana edad, menor es la probabilidad de que las mujeres presenten problemas cognitivos mucho más adelante’, señala el autor principal, Yu Chen, investigador y profesor de la Universidad de Nueva York en un comunicado difundido por la revista.
‘Nuestros datos sugieren que es importante llevar una dieta sana siempre, pero especialmente crítico a partir de los cuarenta años para prevenir el deterioro cognitivo en la vejez’, ha añadido el investigador. Aunque habría que realizar más estudios en distintos grupos raciales y étnicos para determinar si los resultados del estudio son generalizables a toda la población, hay investigaciones previstas que ya han demostrado que la hipertensión causada por malos hábitos de alimentación, sobre todo en la mediana edad, supone un factor de riesgo importante en el deterioro cognitivo y demencia en la vejez.
Referencia:
Song Y, Wu F, Sharma S, Clendenen TV, Aldana SI, Afanasyera Y, et al. Mid-life adherence to the Dietary Approaches to Stop Hypertension (DASH) diet and late-life subjective cognitive complaints in women. Alzheimer’s Dement[Internet]. 2023[citado 21 oct 2023]; 1-13. doi: 10.1002/alz.13468.
Fuente: Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.

