jun
8
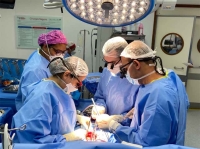 La Organización Mundial de la Salud (OMS) celebró este jueves el Día Mundial de los Pacientes Trasplantados, por la necesidad de millones de pacientes de enfermedades crónicas o terminales de la realización de esta práctica para seguir viviendo.
La Organización Mundial de la Salud (OMS) celebró este jueves el Día Mundial de los Pacientes Trasplantados, por la necesidad de millones de pacientes de enfermedades crónicas o terminales de la realización de esta práctica para seguir viviendo.
Procedimientos como los trasplantes de riñón, hígado, corazón y pulmones son comunes y salvan muchas vidas, en tanto la ciencia médica mejora las técnicas quirúrgicas y los tratamientos postoperatorios, incrementando las tasas de éxito y la calidad de vida de estas personas.
En el transcurso de la pasada 77 Asamblea Mundial de la Salud los delegados aprobaron un nuevo y pionero acuerdo sobre el aumento de la disponibilidad, el acceso ético y la supervisión del trasplante de células, tejidos y órganos humanos, señaló el portal cubano Infomed.
Los datos más recientes de 2022 del Observatorio Mundial de Donación y Trasplante indican que anualmente se realizan más de 150 000 trasplantes (el 10 % o menos de las necesidades mundiales) de órganos sólidos en todo el mundo, una cifra que no obstante supone un aumento del 52 % con respecto a 2010.
Sin embargo, todavía se observa un crecimiento insuficiente y un desarrollo asimétrico en materia de trasplantes en todo el mundo, pues muchos países no cuentan con sistemas adecuados, por ejemplo, en términos de legislación, gobernanza, mano de obra especializada, infraestructura y financiación.
La falta de disponibilidad y de acceso equitativo a los trasplantes puede provocar la muerte o derivar en prácticas poco éticas o ilegales, como el turismo de trasplante y el tráfico de órganos. La resolución pretende mejorar la disponibilidad de los trasplantes, sobre todo en los países con recursos limitados.
Con la resolución se pretende introducir medidas para prevenir y combatir la trata de personas con fines de extracción de órganos y el tráfico de órganos humanos, y proteger a las víctimas y supervivientes de estos delitos reforzando los marcos legislativos.
Los Estados Miembros se comprometieron a adoptar una serie de medidas, entre ellas, integrar las actividades de donación y trasplante en los sistemas de atención de salud, de modo que la donación tras el fallecimiento sea contemplada sistemáticamente como una posibilidad al final de la vida.
Asimismo, proteger a los donantes vivos de la explotación y que reciban una atención de seguimiento adecuada.
La OMS tiene el encargo de elaborar una estrategia mundial sobre donaciones y trasplantes, que se presentará a la Asamblea para su adopción en 2026.
06 junio 2024|Fuente: Prensa Latina |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2023. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
may
14
 Al menos 17 personas, en una lista de espera que hoy rebasa los 100 000, fallecen diariamente en Estados Unidos mientras aguardan por un órgano compatible para trasplante, de acuerdo con cifras citadas por la prensa.
Al menos 17 personas, en una lista de espera que hoy rebasa los 100 000, fallecen diariamente en Estados Unidos mientras aguardan por un órgano compatible para trasplante, de acuerdo con cifras citadas por la prensa.
Hay más de 106 000 personas en la lista de espera nacional de trasplantes y 92 000 (87 %) es por un riñón, dice la American Kidney Fund.
Las estadísticas son recurrentes ahora tras circular la noticia este fin de semana de que casi dos meses después de una cirugía sin precedentes en el país, falleció Richard Slayman, el paciente que recibió el primer trasplante de riñón de cerdo modificado genéticamente.
El equipo de trasplantes del Hospital General de Massachusetts, donde se realizó la operación, expresó en un comunicado la profunda tristeza por la muerte de Slayman, de 62 años.
La novedosa técnica se aplicó en el hombre originario de Weymouth, Massachusetts, por primera vez en un ser vivo porque habían hecho estudios de trasplante de riñón de cerdo a pacientes con muerte cerebral.
El procedimiento marcó un hito en el avance de los trasplantes entre especies diferentes (xenotrasplantes) como una alternativa de vida para aquellos que solo podrían salvarse con un órgano donado.
Slayman se sometió a un trasplante de riñón en 2018, pero experimentó signos de falla renal y tuvo que volver a diálisis en 2023, cuando su condición empeoró y surgió la posibilidad de someterse a este tratamiento experimental.
Los médicos daban una expectativa de vida de otros dos años a Slayman, si el procedimiento resultaba exitoso. No obstante, la familia agradeció al equipo de galenos «sus enormes esfuerzos al frente del xenotrasplante», porque proporcionaron «siete semanas más con Rick, y los recuerdos (…) permanecerán en nuestras mentes y corazones».
13 mayo 2024|Fuente: Prensa Latina |Tomado de |Noticia
mar
23
 Médicos en Boston han trasplantado un riñón de cerdo en un paciente de 62 años, el más reciente experimento en la búsqueda de usar órganos animales en seres humanos. El Hospital General de Massachusetts dijo el jueves que es la primera vez que se trasplanta un riñón de cerdo
Médicos en Boston han trasplantado un riñón de cerdo en un paciente de 62 años, el más reciente experimento en la búsqueda de usar órganos animales en seres humanos. El Hospital General de Massachusetts dijo el jueves que es la primera vez que se trasplanta un riñón de cerdo
genéticamente modificado en una persona con vida. Anteriormente se habían trasplantado riñones de cerdo en donantes con muerte cerebral. Además, dos personas recibieron trasplantes de corazón de cerdo, aunque ambos pacientes murieron a los pocos meses. El nuevo paciente, Richard Slayman, residente de Weymouth, Massachusetts, se está recuperando bien tras la cirugía del sábado y se prevé que reciba el alta en poco tiempo.
El doctor Tatsuo Kawai, el cirujano que llevó a cabo el procedimiento, dijo que el equipo cree que el riñón de cerdo funcionará por al menos dos años. De presentar una falla, Slayman podría volver a las diálisis, dijo el especialista Winfred Williams.
Destacó que a diferencia de los pacientes que recibieron corazones de cerdo y estaban muy enfermos, Slayman ‘de hecho está bastante fuerte’. Slayman tuvo un trasplante de riñón en el hospital en 2018, pero tuvo que volver a hacerse diálisis el año pasado cuando mostró señales de insuficiencia.
Cuando surgieron complicaciones con las diálisis, las cuales requirieron procedimientos frecuentes, los médicos sugirieron colocarle un riñón de cerdo, dijo en un comunicado distribuido por el hospital. ‘Lo consideré no sólo como una manera de ayudarme, sino de generar esperanzas para miles de personas que requieren de un trasplante para sobrevivir’, dijo Slayman, quien trabaja como gerente de sistemas para el Departamento de Transporte de Massachusetts.
La cirugía tomó cuatro horas y había 15 personas en el quirófano, quienes aplaudieron cuando el riñón tomó una coloración rosada y comenzó a producir orina, dijeron los médicos en una conferencia de prensa. ‘Realmente era el riñón más hermoso que hayamos visto’, indicó Kawai.
El doctor Parsia Vagefi, director de cirugía de trasplantes en el Centro Médico UT Southwestern, se refirió al anuncio como ‘un paso importante’. Pero al igual que los médicos de Boston, dijo que se necesitan estudios que involucren a más pacientes de distintos centros médicos antes de que la práctica esté disponible de manera más frecuente.
El experimento marca el paso más reciente en los xenotrasplantes, el término que se utiliza en el intento de curar a pacientes humanos con células, tejidos u órganos de animales.
Durante décadas no funcionó, ya que el sistema inmunológico humano destruía de inmediato el tejido animal. Los intentos más recientes se han realizado con cerdos modificados para que sus órganos se parezcan más a los del ser humano, lo que genera nuevas esperanzas de que algún día sirvan para compensar la escasez de órganos donados. Más de 100.000 personas en Estados Unidos están en lista de espera para un trasplante, en su mayoría enfermos del riñón, y miles mueren cada año antes de que llegue su turno. Los cerdos han sido utilizados desde hace tiempo en la medicina humana, incluidos los injertos de piel y la implantación de válvulas cardiacas. Pero el trasplante de órganos completos es mucho más complejo que utilizar tejido procesado. El riñón que se le implantó a Slayman provino de la compañía eGenesis de Cambridge, Massachusetts. El animal fue modificado genéticamente para retirarle genes porcinos perjudiciales y añadir ciertos genes humanos para mejorar su compatibilidad. El caso de Slayman fue complicado, indicaron los médicos.
Incluso antes de su primer trasplante, el paciente tenía problemas con la diálisis y necesitó de decenas de procedimientos para intentar retirarle coágulos y restaurar el flujo sanguíneo. Se volvió ‘cada vez más desanimado y deprimido por su situación con la diálisis. En cierto punto, literalmente
dijo ‘no puedo seguir así’, comentó su médico, Williams. La Administración de Alimentos y Medicamentos de Estados Unidos otorgó un permiso especial para el procedimiento de Slayman en virtud a las reglas de ‘uso compasivo’.
Nueva York, 22 marzo 2024|Fuente: AP | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
ene
9
 Roy Calne, un pionero en los trasplantes de órganos que dirigió la primera operación de trasplante de hígado en Europa en 1968, murió a la edad de 93 años. La familia de Calne señaló que murió la tarde del sábado en Cambridge, Inglaterra, donde fue profesor emérito de cirugía en la Universidad Cambridge.
Roy Calne, un pionero en los trasplantes de órganos que dirigió la primera operación de trasplante de hígado en Europa en 1968, murió a la edad de 93 años. La familia de Calne señaló que murió la tarde del sábado en Cambridge, Inglaterra, donde fue profesor emérito de cirugía en la Universidad Cambridge.
Nacido en 1930, Calne fue capacitado como médico en el Hospital de Londres de Guy y desarrolló un interés en el trasplante de órganos en la década de 1950, en parte inspirado, según dijo después, por el trabajo de su padre como mecánico de autos. En aquella época le dijeron que el procedimiento sería imposible.
Es considerado uno de los padres de los trasplantes de órganos, junto con el científico estadounidense, doctor Thomas Starzl. Su trabajo en el procedimiento quirúrgico y tratamiento para prevenir el rechazo de órganos inicialmente se realizó en perros.
En 1960, los experimentos en perro de Calne demostraron por primera vez que un medicamento podría evitar el rechazo de órganos. Starzl intentó el primer trasplante de hígado humano en 1963. El paciente murió durante el procedimiento.
Los siguientes pacientes también murieron semanas después de sus trasplantes, pero las cirugías demostraron que los hígados trasplantados podían funcionar. ‘Al principio fue terrible. Tuvimos muchas complicaciones espantosas’, dijo Calne en 1999.
En mayo de 1968, Calne dirigió una operación de trasplante en una mujer de 46 años con cáncer de hígado en el Hospital de Addenbrooke en Cambridge. La paciente murió dos meses después de una infección debido a los medicamentos inmunosupresores que recibió para evitar el rechazo.
Calne se enfocó en encontrar mejores formas para evitar que los cuerpos de los pacientes rechazaran los órganos donados. Ayudó a desarrollar la innovadora medicina ciclosporina, que evita el rechazo, y fue el primer médico en administrarla a sus pacientes de trasplantes. Los medicamentos antirechazo cambiaron las posibilidades de sobrevivir de los pacientes, y los trasplantes de hígado han salvado miles de vidas desde que fueron aceptados ampliamente en la década de 1980.
Enero 9 2024 /Fuente: AP./ Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
oct
24
 Lawrence Faucette se convirtió en la segunda persona en recibir un corazón trasplantado de un cerdo y, un mes después, no muestra señales de que su cuerpo rechace el órgano.
Lawrence Faucette se convirtió en la segunda persona en recibir un corazón trasplantado de un cerdo y, un mes después, no muestra señales de que su cuerpo rechace el órgano.
Ha pasado un mes desde que un hombre de Maryland se convirtió en la segunda persona en recibir un corazón trasplantado de un cerdo, y un video del hospital difundido el viernes lo muestra trabajando duro para reponerse.
Lawrence Faucette estaba a punto de morir por insuficiencia cardiaca y no era elegible para un trasplante de corazón tradicional debido a otras complicaciones de salud cuando los médicos de la Facultad de Medicina de la Universidad de Maryland le ofrecieron esa cirugía altamente experimental.
En las primeras imágenes de Faucette desde el trasplante del 20 de septiembre, un video del hospital muestra al fisioterapeuta Chris Wells instándole a sonreír mientras pedalea para recuperar fuerzas.
“Va a estar difícil, pero triunfaré», contesta Faucette, de 58 años, resoplando pero esbozando una sonrisa.
El equipo de Maryland realizó el año pasado el primer trasplante mundial de un corazón de un cerdo genéticamente modificado a otro hombre moribundo.
David Bennett sobrevivió solamente dos meses antes de que ese corazón dejara de funcionar por razones que no están completamente claras, aunque más tarde se encontraron evidencias de un virus porcino en el interior del órgano.
Lo aprendido en aquel primer experimento produjo varios cambios antes de este segundo intento, entre ellos la mejora de las pruebas de detección de virus.
Los intentos de trasplante de órganos de animales a humanos —los llamados xenotrasplantes— han fracasado durante décadas, ya que el sistema inmunitario de las personas destruía de inmediato el tejido extraño. Ahora los científicos vuelven a intentarlo con cerdos modificados genéticamente para que sus órganos sean más parecidos a los humanos.
En el video del hospital difundido el viernes, los médicos de Faucette dijeron que el corazón de cerdo no ha presentado síntomas de rechazo.
“Su corazón está haciendo todo autónomamente”, dijo el doctor Muhammad Mohiuddin, jefe de xenotrasplantes cardiacos del equipo de Maryland.
Una vocera del hospital dijo que Faucette, de Frederick, Maryland, ha podido levantarse y que los fisioterapeutas lo están ayudando a ganar las fuerzas necesarias para intentar caminar.
Muchos científicos esperan que algún día los xenotrasplantes puedan compensar la enorme carencia de donaciones de órganos humanos. Más de 100 mil personas están en la lista de trasplantes de Estados Unidos, la mayoría a la espera de un trasplante de riñón, y miles morirán esperando.
Un puñado de equipos científicos han probado riñones y corazones de cerdos en monos y en cuerpos humanos donados, esperando aprender lo suficiente para que la Administración de Alimentos y Medicamentos de Estados Unidos les permita realizar estudios formales de xenotrasplantes.
24 octubre 2023| Fuente: Proceso| Tomado de Noticias Medicina | Ciencia -Tecnología
oct
13
 Los investigadores realizaron 69 modificaciones genéticas para lograr evitar el rechazo hiperagudo, la reacción habitual ante un trasplante entre especies diferentes.
Los investigadores realizaron 69 modificaciones genéticas para lograr evitar el rechazo hiperagudo, la reacción habitual ante un trasplante entre especies diferentes.
Obtener órganos de ‘repuesto’, desarrollados en animales y disponibles para el trasplante en humanos, es un objetivo que persiguen diferentes grupos de investigación en todo el mundo.
Aunque en 2022 se llevaron a cabo varios xenotrasplantes experimentales, como la implantación de un corazón de cerdo modificado genéticamente a un paciente de Baltimore que sufría una grave enfermedad cardiaca; este tipo de abordaje todavía está lejos de llegar a la clínica. Antes, se deben solventar desafíos biotecnológicos importantes que plantea el ‘salto’ entre especies, como el rechazo hiperagudo tras el injerto o el riesgo de zoonosis.
Una investigación liderada por científicos de la Universidad de Harvard y la compañía eGenesis allana ese camino al haber conseguido implantar riñones de cerdo editados genéticamente en macacos y lograr unas cifras de supervivencia reseñables. Uno de los ejemplares trasplantados vivió más de dos años con el injerto de riñón. Los detalles de la investigación se publican en la revista Nature.
Para minimizar el riesgo de rechazo y la posibilidad de transmisión de virus porcinos con el trasplante, los investigadores realizaron 69 modificaciones genéticas en el animal donante, un cerdo de Yucatán.
Estas modificaciones pueden agruparse en tres bloques: en primer lugar, eliminaron tres antígenos glicanos, ‘marcadores’ presentes en la superficie de las células que inducen un rechazo inmediato. Además, introdujeron cambios para que las células animales expresaran siete genes humanos con el objetivo de mejorar la tolerancia y neutralizar otros fenómenos asociados al rechazo hiperagudo. Y, por último, inactivaron todas las copias de la genética relacionada con retrovirus porcinos.
En combinación con medicación inmunosupresora, este cóctel de ingeniería genética proporcionó una supervivencia de hasta 758 días a uno de los macacos trasplantados.
CLAVES DEL XENOTRASPLANTE
Una de las principales claves para conseguir esa prolongada supervivencia fue la manipulación para añadir los genes humanizados, implicados en varias vías relacionadas con el rechazo, como la inflamación, la inmunidad innata o la coagulación, tal y como explicaron los investigadores en una rueda de prensa.
Los estudios in vitro, señalan los científicos, mostraron que las células endoteliales renales de los animales con estas ediciones genéticas eran capaces de modular la inflamación de una forma «indistinguible» de las células endoteliales humanas. «Nuestros resultados nos colocan un paso adelante para alcanzar la compatibilidad humana», subrayó Michael Curtis, responsable de eGenesis en el encuentro con la prensa.
Este diseño y desarrollo se trata de una «prueba de concepto» que «apoya el avance hacia el desarrollo clínico» del principal candidato que la compañía eGenesis está diseñando para el trasplante de riñón, denominado EGEN-2784, ha señalado la compañía en un comunicado.
Para Beatriz Domínguez-Gil, directora de la Organización Nacional de Trasplantes (ONT), este diseño «se trata de un modelo que proporciona resultados muy prometedores».
Domínguez-Gil destaca el diseño de modificaciones genéticas que ha permitido alcanzar «una supervivencia prolongada en primates no humanos».
Pero, además, hace hincapié en el hecho de que el desarrollo proporciona «un modelo experimental que nos va a permitir avanzar en el ámbito del xenotrasplante de una forma mucho más segura».
Este diseño permite dar un paso importante «a la hora de demostrar que un abordaje es seguro y eficaz antes de dar el salto a la realización de ensayos clínicos».
Desde esas dos perspectivas, «es un estudio muy novedoso y de mucha relevancia», subraya Domínguez-Gil, que también apunta que la utilización de este tipo de primates no humanos como receptores en los experimentos puede facilitar la traslación posterior de los resultados a la clínica. «Es un modelo probablemente más trasladable a la realidad del humano que los que se han utilizado previamente», destaca.
UN LARGO CAMINO POR RECORRER
De cualquier manera, la directora de la ONT recuerda que «todavía quedan muchísimos pasos en este en ese camino de llevar el xenotrasplante a la clínica».
Queda mucho trabajo por realizar en el ámbito preclínico, subraya Domínguez-Gil. En este sentido, los propios investigadores reconocen en la revista científica que las modificaciones genéticas planteadas deben afinarse para conseguir resultados clínicos.
Pero, además, también hay que abordar las cuestiones éticas que plantea este tipo de procedimientos. «Entre otras cosas, se tiene que decidir cuál es el paciente al que se le va a ofrecer esta opción frente a la alternativa; es decir, qué criterios tiene que cumplir un paciente para entrar en un ensayo clínico de estas características cuando tenemos ya un tipo de trasplante entre humanos muy consolidado, que es una realidad clínica ya habitual y que ofrece extraordinarios resultados», señala.
También hay que abordar cuestiones relacionadas con la protección de los animales, así como la planificación de cómo se va a lograr que estos tratamientos «extraordinariamente costosos» puedan llegar a los pacientes de una forma equitativa, plantea la directora de la ONT.
«Hay muchas cuestiones que avanzar y que tener en cuenta, pero yo creo que en los próximos 10 años sí vamos a ver un salto importante a la clínica de esta opción terapéutica», concluye Domínguez-Gil.
Referencia
Anand RP, Layer JV, Heja D, Hirose T, Lassiter G, Firl D, et al. Design and testing of a humanized porcine donor for xenotransplantation. Nature[Internet]. 2023[citado 12 oct 2023]; 622, 393–401. https://doi.org/10.1038/s41586-023-06594-4
13 octubre 2023│Fuente: El Mundo│ Tomado de Salud

