oct
7
 Investigadores del Massachusetts Institute of Technology (MIT) han desarrollado un «rayo tractor» en miniatura basado en un chip que permitirá estudiar el ADN, clasificar las células e investigar los mecanismos de las enfermedades.
Investigadores del Massachusetts Institute of Technology (MIT) han desarrollado un «rayo tractor» en miniatura basado en un chip que permitirá estudiar el ADN, clasificar las células e investigar los mecanismos de las enfermedades.
El dispositivo, lo suficientemente pequeño como para caber en la palma de la mano, utiliza un haz de luz emitido por un chip fotónico de silicio para manipular partículas a milímetros de la superficie del chip. La luz puede penetrar los cubreobjetos de vidrio que protegen las muestras utilizadas en experimentos biológicos, lo que permite que las células permanezcan en un entorno estéril.
Las pinzas ópticas tradicionales, que atrapan y manipulan partículas utilizando luz, suelen requerir configuraciones de microscopio voluminosas, pero las pinzas ópticas basadas en chips podrían ofrecer una solución más compacta, de fabricación en masa, ampliamente accesible y de alto rendimiento para la manipulación óptica en experimentos biológicos.
Sin embargo, otras pinzas ópticas integradas similares solo pueden capturar y manipular células que están muy cerca o directamente sobre la superficie del chip. Esto contamina el chip y puede estresar las células, lo que limita la compatibilidad con los experimentos biológicos estándar.
Utilizando un sistema llamado matriz óptica en fase integrada, los investigadores del MIT han desarrollado una nueva modalidad de pinzas ópticas integradas que permite atrapar y pinzar células a más de cien veces más distancia de la superficie del chip.
«Este trabajo abre nuevas posibilidades para las pinzas ópticas basadas en chips al permitir atrapar y pinzar células a distancias mucho mayores que las demostradas anteriormente. Es emocionante pensar en las diferentes aplicaciones que podría permitir esta tecnología», dice en un comunicado Jelena Notaros, profesora de Desarrollo Profesional Robert J. Shillman en Ingeniería Eléctrica y Ciencias de la Computación (EECS), y miembro del Laboratorio de Investigación de Electrónica.
La investigación aparece en Nature Communications.
03 octubre 2024|Fuente: Europa Press |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
oct
7
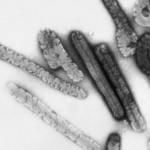 Ruanda iniciará pronto ensayos clínicos de vacunas y tratamientos para hacer frente al brote de la enfermedad del virus de Marburgo declarado el 27 de septiembre , similar al ébola, que ha registrado en el país hasta el momento 36 casos confirmados y 11 muertes, informó el pasado jueves el Ministerio de Sanidad ruandés.
Ruanda iniciará pronto ensayos clínicos de vacunas y tratamientos para hacer frente al brote de la enfermedad del virus de Marburgo declarado el 27 de septiembre , similar al ébola, que ha registrado en el país hasta el momento 36 casos confirmados y 11 muertes, informó el pasado jueves el Ministerio de Sanidad ruandés.
«(Estamos) a punto de empezar ensayos clínicos de vacunas y terapias para proteger a los grupos de alto riesgo», dijo a través de la red social X el secretario de Estado de Sanidad, Yvan Butera, sobre una enfermedad para la que no hay vacuna ni tratamiento específico.
El alto funcionario detalló que se está monitorizando a 410 contactos de los enfermos detectados para «romper las cadenas de transmisión» y que, hasta ahora, cinco pacientes han dado negativo al hacerse un test.
Según los últimos datos difundidos por el Ministerio en un escueto comunicado poco después de la pasada medianoche, 25 personas se encuentran en aislamiento y están recibiendo tratamiento por la enfermedad, al tiempo que las autoridades sanitarias trabajan en el rastreo de contactos y en pruebas diagnósticas.
Para evitar su propagación, las autoridades han recomendado reforzar la higiene y evitar el contacto cercano con personas que presenten los síntomas de la enfermedad, que incluyen fiebre alta, fuertes dolores de cabeza, dolores musculares, vómitos y diarrea.
En otro comunicado difundido el 27 de septiembre con motivo de la declaración del brote, el Ministerio destacó la implementación de «medidas preventivas reforzadas en todos los centros de salud».
La enfermedad del virus de Marburgo es una fiebre hemorrágica viral altamente infecciosa de la misma familia que el ébola.
África fue escenario el pasado año de dos epidemias de Marburgo: una en Guinea Ecuatorial, que causó 17 casos confirmados, incluidos 12 fallecidos; y otra en Tanzania, con al menos nueve casos (ocho confirmados y uno probable) y seis muertos.
Antes, hubo casos en otros países como Ghana, Guinea-Conakri, Uganda, Angola, la República Democrática del Congo (RDC), Kenia y Sudáfrica.
Esta enfermedad es tan mortífera como el ébola y se calcula que en África ha causado la muerte de más de 3 500 personas.
Al igual que el ébola, el virus de Marburgo provoca hemorragias repentinas y puede producir la muerte en pocos días, con un período de incubación de 2 a 21 días y una tasa de mortalidad de hasta el 88 %.
Los murciélagos de la fruta son los huéspedes naturales de este virus, que cuando es transmitido a los humanos puede ser contagiado mediante contacto directo con fluidos como la sangre, saliva, vómitos u orina.
La enfermedad fue detectada en 1967 en la ciudad alemana de Marburgo -origen de su nombre- por técnicos de laboratorio que resultaron infectados cuando investigaban a monos traídos de Uganda.
03 octubre 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
oct
1
 Investigadores de la Universidad Pública de Navarra (UPNA), en colaboración con equipos científico-tecnológicos de Italia, Polonia y Colombia, han desarrollado un biosensor óptico capaz de detectar biomoléculas, como proteínas, ADN o virus, en fluidos biológicos complejos, como el suero humano, «con una precisión y sensibilidad sin precedentes».
Investigadores de la Universidad Pública de Navarra (UPNA), en colaboración con equipos científico-tecnológicos de Italia, Polonia y Colombia, han desarrollado un biosensor óptico capaz de detectar biomoléculas, como proteínas, ADN o virus, en fluidos biológicos complejos, como el suero humano, «con una precisión y sensibilidad sin precedentes».
Este dispositivo, que se evaluó detectando inmunoglobulina G (IgG), un tipo de anticuerpo, en concentraciones «extremadamente bajas, puede servir para el diagnóstico precoz de enfermedades».
Los investigadores de la UPNA implicados en este trabajo, que ha sido publicado en la revista científica Advanced Science, son los catedráticos Ignacio del Villar Fernández e Ignacio R. Matías Maestro, investigadores del Instituto de Smart Cities (ISC), y el estudiante de doctorado Dayron Armas Peña.
El resto del equipo internacional está integrado por especialistas del Instituto de Física Aplicada Nello Carrara de Italia, la Universidad Tecnológica de Varsovia (Polonia) y la Universidad Nacional de Colombia.
El biosensor se basa en una tecnología llamada biofotónica, que utiliza la luz para detectar biomoléculas. Para crear este sensor, el equipo internacional de investigadores ha utilizado nanofilms, que son capas de material extremadamente delgadas (un nanómetro es una millonésima parte de un milímetro) con propiedades ópticas especiales que no se observan en estructuras más grandes.
Estos nanofilms forman lo que se llama un cristal fotónico unidimensional. Este cristal está integrado en una fibra óptica, pulida lateralmente para que la luz interactúe directamente con el entorno externo, donde se encuentran las biomoléculas.
Así, cuando una de ellas se acerca o se adhiere a la superficie pulida de la fibra óptica, afecta a la forma en que la luz se comporta en el cristal fotónico. Estos cambios en la luz son detectados por el sensor, lo que permite identificar la presencia y la cantidad de biomoléculas.
LA «CLAVE DEL ÉXITO»: ALTA SENSIBILIDAD Y PRECISIÓN
Una de las «innovaciones clave» de este biosensor consiste en la elección de nanomateriales con un alto contraste en su índice de refracción (una medida de cómo la luz se desvía al atravesar un material) y bajas pérdidas de luz.
Esto significa que el sensor puede detectar incluso cantidades muy pequeñas de biomoléculas «con una precisión excepcional, lo que es crucial para aplicaciones médicas».
Al lograr un equilibrio entre alta sensibilidad y un parámetro técnico conocido como ancho de banda a media altura (FWHM, por sus siglas en inglés), el dispositivo «puede identificar con claridad las biomoléculas sin confundirlas con otras sustancias».
Esta combinación «mejora significativamente» lo que se conoce como la figura de mérito (FoM, por sus siglas en inglés), un indicador del rendimiento general del dispositivo.
DETECTANDO ENFERMEDADES EN SUS PRIMERAS ETAPAS
En concreto, el rendimiento del biosensor se evaluó detectando el anticuerpo inmunoglobulina G (IgG) en muestras de suero humano. La concentración mínima de una sustancia que el sensor puede detectar se llama límite de detección (LoD, por sus siglas en inglés).
Y el sensor desarrollado por este equipo internacional con participación de la UPNA logró un LoD récord de 70 attomolar (aM), una concentración «extremadamente baja que equivale a detectar una sola molécula entre millones de otras o tener una sola molécula en un océano de un millón de billones de litros de agua».
Este nivel de sensibilidad tiene «importantes implicaciones para el diagnóstico precoz de enfermedades», ya que «permite hallar biomarcadores en cantidades mínimas, cuando las enfermedades apenas comienzan a desarrollarse».
29 septiembre 2024|Fuente: Europa Press |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
sep
24
 Científicos de la Universidad de Southampton, en Inglaterra, preservaron el genoma humano completo en un cristal de memoria 5D, un formato revolucionario de almacenamiento de datos que puede sobrevivir durante miles de millones de años.
Científicos de la Universidad de Southampton, en Inglaterra, preservaron el genoma humano completo en un cristal de memoria 5D, un formato revolucionario de almacenamiento de datos que puede sobrevivir durante miles de millones de años.
Los investigadores esperan que el cristal pueda proporcionar un modelo para rescatar a la humanidad de la extinción dentro de miles, millones o incluso miles de millones de años, si la ciencia lo permite.
También podría utilizarse para crear un registro duradero de los genomas de especies de plantas y animales en peligro de extinción.
A diferencia de otros formatos de almacenamiento de datos que se degradan con el tiempo, los cristales de memoria 5D —desarrollados por el Centro de Investigación de Optoelectrónica— pueden almacenar hasta 360 terabytes de información, publicó el centro universitario en su portal web.
El cristal es equivalente al cuarzo fundido, uno de los materiales más resistentes química y térmicamente de la Tierra, que puede soportar los extremos de congelación, fuego y temperaturas de hasta 1000 °C.
Además de sostener una fuerza de impacto directa de hasta 10 toneladas por centímetro cuadrado y no verse afectado por la exposición prolongada a la radiación cósmica.
El equipo de Southampton, dirigido por el profesor Peter Kazansky, utiliza láseres ultrarrápidos para inscribir con precisión los datos en huecos nanoestructurados, orientados dentro de sílice, con tamaños de características tan pequeños como 20 nanómetros.
A diferencia de marcar solo en la superficie de una hoja de papel 2D o una cinta magnética, este método de codificación utiliza dos dimensiones ópticas y tres coordenadas espaciales para escribir en todo el material, de ahí el «5D» en su nombre.
«El cristal de memoria 5D abre posibilidades para que otros investigadores construyan un repositorio eterno de información genómica a partir del cual se puedan restaurar organismos complejos como plantas y animales si la ciencia lo permite en el futuro», destacó Kazansky.
El cristal está almacenado en el archivo Memory of Mankind, una cápsula del tiempo especial dentro de una cueva de sal en Hallstatt, Austria.
20 septiembre 2024|Fuente: Prensa Latina |Tomado de |Noticia
sep
19
 Una red global de doctores y laboratorios trabaja para detectar la aparición de nuevas amenazas virales, muchas motivadas por el cambio climático, en un intento de evitar la próxima pandemia mundial.
Una red global de doctores y laboratorios trabaja para detectar la aparición de nuevas amenazas virales, muchas motivadas por el cambio climático, en un intento de evitar la próxima pandemia mundial.
Esta coalición de «cazadores de virus», como se llaman a ellos mismos, ha destapado ya una inusual enfermedad transmitida por garrapatas en Tailandia o un brote infeccioso en Colombia propagado por mosquitos.
«La relación de cuestiones por las que nos tenemos que preocupar, como vimos en el covid-19, no es estática», afirma Gavin Cloherty, experto en enfermedades infecciosas que dirige la Coalición de Defensa contra Pandemias de Abbott.
«Tenemos que estar muy atentos a los tipos malos que ya conocemos y que están evolucionando (…) Pero también a si hay nuevos niños en el barrio», dice a la AFP.
La coalición reúne a doctores y científicos en universidades e instituciones sanitarias de todo el mundo, financiados por el gigante de dispositivos médicos y sanitarios Abbott.
Al descubrir nuevas amenazas, la coalición otorga a la empresa una ventaja a la hora de diseñar los test diagnósticos que fueron claves en la respuesta a la pandemia del covid.
Su implicación dota a la coalición de amplios recursos y de la capacidad de detectar y secuenciar, pero también responder a los nuevos virus.
«Cuando encontramos algo, somos capaces de desarrollar rápidamente test de diagnóstico a nivel industrial», dice Cloherty.
«La idea es contener un brote, de forma que podamos prevenir una pandemia», agrega.
La coalición ha secuenciado aproximadamente 13 000 muestras desde que empezó a funcionar en 2021.
En Colombia descubrió un brote de Oropouche, un virus transmitido por jejenes y mosquitos que apenas se había observado previamente.
El trabajo filogenético para trazar el árbol familiar de la cepa reveló que procedía de Perú o Ecuador y no de Brasil, otro foco de esta enfermedad.
«Puedes ver de dónde vienen las cosas. Es importante desde una perspectiva de salud pública», afirma Cloherty.
Vínculo con el cambio climático
Más recientemente, la coalición trabajó con médicos en Tailandia para descubrir que un virus propagado por garrapatas estaba detrás de un misterioso grupo de casos de pacientes enfermos.
«En ese momento no sabíamos qué virus causaba este síndrome», explica Pakpoom Phoompoung, profesor asociado de enfermedades infecciosas en el hospital Siriraj de Bangkok.
El análisis y la secuenciación de muestras tomadas desde 2014 concluyó que muchas eran positivas del virus de fiebre severa con síndrome trombocitopénico (SFTSV).
«Menos de diez paciente habían sido diagnosticados (previamente) con SFTSV en Tailandia (…) No tenemos test PCR de diagnosis, no tenemos serología para el diagnóstico de esta infección viral», cuenta Pakpoom a la AFP.
Diagnosticarla «es difícil, necesita mucha mano de obra y también es costoso».
Pero al mismo tiempo crece la necesidad de controlar estas amenazas porque el cambio climático amplía globalmente el espectro de las enfermedades infecciosas.
El vínculo entre cambio climático y las enfermedades infecciosas ha quedado bien establecido por la ciencia y es multifacético.
Unas condiciones más cálidas permiten que transmisores como los mosquitos puedan vivir en nuevos entornos, el aumento de las lluvias intensas crea más criaderos y los episodios meteorológicos extremos dejan a más personas a la intemperie, donde son más vulnerables.
El impacto humano en el planeta fomenta la expansión y la evolución de las enfermedades infecciosas de otras maneras: la pérdida de biodiversidad fuerza a los virus a evolucionar en nuevos huéspedes y empuja a los animales más cerca de las zonas pobladas.
De Bangkok a Boston
El análisis filogenético de la cepa del SFTSV en Tailandia ofrece un ejemplo de las complejas interrelaciones.
El virus pasó de una especie de garrapata con una reducida presencia geográfica a la garrapata asiática de cuernos largos, más resistente y expandida.
Los análisis sugieren que su evolución estuvo principalmente causada por el uso de pesticidas que redujo la población del primer tipo de garrapata.
Una vez en el nuevo anfitrión, el virus se ha expandido más allá porque las garrapatas asiáticas de cuernos largos pueden vivir en pájaros, que se trasladan más lejos y más rápido.
«Es casi como si fueran una aerolínea», dice Cloherty.
Las huellas del cambio climático se encuentran por todos partes, desde los brotes de dengue en América Latina y el Caribe hasta la propagación del virus del Nilo Occidental en Estados Unidos.
Aunque la coalición se aprovechó de los trabajos previos a la última pandemia, la propagación global del covid-19 fue un potente recordatorio de los riesgos de estas enfermedades.
Pero Cloherty teme que la población ya se está olvidando de estas lecciones.
«Tenemos que estar atentos», afirma. «Algo que pasa ahora en Bangkok puede estar ocurriendo mañana en Boston».
17 septiembre 2024|Fuente: AFP |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
sep
14
 Un equipo científico del Instituto de Investigación Biomédica (IRB) de Barcelona ha identificado cinco factores independientes que predicen la respuesta de pacientes afectados por cáncer a los tratamientos con inmunoterapia.
Un equipo científico del Instituto de Investigación Biomédica (IRB) de Barcelona ha identificado cinco factores independientes que predicen la respuesta de pacientes afectados por cáncer a los tratamientos con inmunoterapia.
Este estudio, publicado en la revista Nature Genetics, ha validado estos cinco factores en más de 1 400 pacientes y diversos tipos de cáncer.
Según ha informado este jueves el IRB Barcelona en un comunicado, el hallazgo ofrece un marco para mejorar la medicina personalizada del cáncer y sugiere que pacientes con algunos tipos de tumores, que generalmente no reciben inmunoterapia actualmente, también podrían ser beneficiarios de la misma.
El equipo de investigadores está dirigido por la doctora Núria López-Bigas y el doctor Abel González-Pérez, del grupo de Genómica Biomédica del IRB Barcelona, que han trabajado en colaboración con científicos de varios centros internacionales.
Los cinco factores identificados son la carga mutacional del tumor, la infiltración efectiva de células T, la actividad del factor de crecimiento transformante beta (TGF-B) en el microambiente tumoral, el tratamiento previo recibido por el paciente y el potencial proliferativo del tumor.
Estos factores se asocian con la respuesta a los inhibidores de puntos de control inmunológico (CPIs) en diferentes tipos de cáncer y han sido validados en seis cohortes independientes, con un total de 1 491 pacientes.
González-Pérez ha indicado que «hasta ahora, muchos estudios se han centrado en identificar biomarcadores individuales, pero nuestros resultados sugieren que muchos de estos biomarcadores podrían ser diferentes versiones de los mismos factores subyacentes».
Además, los investigadores han demostrado que un modelo multivariante que combina los cinco factores permite clasificar a los pacientes con mayor precisión que solo la carga mutacional del tumor, que se usa en la actualidad en la práctica clínica, y predecir quién responderá mejor a la inmunoterapia.
«Este avance podría en el futuro tener importantes implicaciones clínicas, ya que podría evitar que pacientes con baja probabilidad de respuesta sufran los efectos secundarios de los inhibidores de control inmunológico (CPIs), que pueden derivar en enfermedades autoinmunes, y, además, ayudar a reducir el coste de los tratamientos», se afirma en el comunicado.
Uno de los aspectos más destacados de este estudio es la validación de estos cinco factores en seis cohortes independientes de pacientes con cánceres como el de pulmón, colon y melanoma.
Los investigadores esperan en un futuro poder contar con mayor volumen de datos de pacientes para generar modelos más precisos.
La doctora López-Bigas ha considerado que «este estudio representa un paso importante para entender cómo distintas características del tumor y del paciente contribuyen a la respuesta a los CPIs. En el futuro esperamos que estos cinco factores se integren en la práctica clínica para guiar las decisiones terapéuticas».
El estudio ha contado con la colaboración del Vall d’Hebron Instituto de Oncología (VHIO), la Hartwig Medical Foundation en Amsterdam; el Centro de Investigación Biomédica en Red en Cáncer (CIBERONC) del Instituto de Salud Carlos III; Center for Molecular Medicine en la University Medical Center de Utrecht; Princess Margaret Cancer Center de la Universidad de Toronto y la Universidad Pompeu Fabra, de Barcelona.
También ha recibido financiación del programa Excelencia AECC: Metástasis, de la Asociación Española Contra el Cáncer, el European Research Council, el programa Horizon de la Comisión Europea, el Ministerio de Ciencia y Tecnología y la Generalitat de Catalunya.
12 septiembre 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia

