oct
21
 El Gobierno federal de Estados Unidos financiará el estudio clínico de fase III pivotal de un medicamento específico surgido del Clínic de Barcelona.
El Gobierno federal de Estados Unidos financiará el estudio clínico de fase III pivotal de un medicamento específico surgido del Clínic de Barcelona.
El ácido úrico es un neuroprotector y potenciador de la reperfusión cerebral identificado por el equipo de Ángel Chamorro, jefe de la Unidad de Patología vascular cerebral del Hospital Clínic Barcelona-Idibaps, y transferido a una spin-out del mismo centro, llamada FreeOx Biotech, para su desarrollo como medicamento con el nombre de Ox-01.
Este fármaco destinado, por ahora (podría tener indicación en otras enfermedades), para el tratamiento complementario de la trombectomía mecánica en el ictus isquémico ya tiene concedida una patente para ese uso en Estados Unidos, Australia y Corea del norte (en España y resto de la Unión Europea no porque aquí no existe la fórmula de la patente de uso).
El Gobierno federal estadounidense, incluso, va a financiar un estudio clínico de fase III pivotal que, si los resultados no lo contraindican, servirá para que su agencia reguladora FDA apruebe la terapia directamente.
En favor de este medicamento de ácido úrico, según ha informado Chamorro a este diario, hay dos evidencias relevantes. Una, la primera, demostró un beneficio clínicamente relevante en un subgrupo preespecificado de pacientes en el ensayo clínico de fase IIb Urico-ictus, dirigido por él y publicado en The Lancet Neurology.
Y otra, publicada ahora en Science Translational Medicine, que demuestra la eficacia del ácido úrico en la mejora del pronóstico del ictus isquémico.
Este segundo estudio se ha realizado en el marco del muy exigente Stroke Preclinical Assessment Network (SPAN) de Estados Unidos, una red de laboratorios experimentales en isquemia cerebral coordinada por la Keck School of Medicine de la Universidad del Sur de California. Chamorro, que también es asesor científico de FreeOx Biotech y profesor adjunto de la Universidad de Iowa, es uno de los firmantes de este trabajo.
El objetivo del SPAN fue identificar las moléculas más prometedoras para su posterior evaluación en estudios clínicos de fase III pivotales financiados por el Instituto Nacional de Enfermedades Neurológicas e Ictus (NINDS) de los Institutos Nacionales de Salud (NIH) de los Estados Unidos, creador de la red.
En el estudio actual, se seleccionaron seis terapias candidatas en base a investigaciones previas que mostraban evidencia de que podrían ser eficaces en el tratamiento del ictus. Los animales (modelos similares a la tipología de pacientes con accidente cerebrovascular) fueron asignados aleatoriamente al tratamiento y los investigadores de seis laboratorios distintos probaron una de las terapias o un placebo.
Y con ello se identificó que el ácido úrico era el único tratamiento eficaz entre las terapias evaluadas dentro del proyecto, lo que posiciona al Ox-01 en la rampa para el despegue del antes citado ensayo clínico de fase III pivotal en Estados Unidos.
Chamorro explica que el tratamiento del ictus isquémico no está bien completado aún, de ahí la trascendencia de esta prometedora terapia. La trombectomía y los fármacos que se usan actualmente funcionan en arterias de mediano y gran calibre, pero no tanto en microcirculación y tampoco protegen las neuronas del daño por reperfusión. Es ahí donde el ácido úrico, en la fórmula para su uso en humanos que han identificado en el Clínico, resulta potencialmente útil.
Indica que si ese ensayo de fase III tiene resultados positivos no hará falta repetirlo para la aprobación del fármaco por parte de la Agencia Europea de Medicamentos (EMA). No ha precisado la cuantía pero el estudio clínico estadounidense cuenta con financiación pública que aquí (en España) solo estaría al alcance de multinacionales farmacéuticas.
Acuerdo para la producción del fármaco
Pero sí ha informado de que FreeOx Biotech, que tienen la exclusividad de síntesis para el Ox-01 (bajo secreto de fabricación), está buscando un acuerdo con laboratorios con infraestructura específica y suficiente como para poder escalar la producción del producto a su uso convencional en clínica, cuando llegue el momento; «eso no lo podemos hacer en el Clínic», recuerda Chamorro.
Este fármaco para ictus isquémico se usará en infusión al paciente con ictus isquémico al mismo tiempo que se le realiza la trombectomía mecánica, con el objetivo de proteger pequeños vasos capilares y neuronas del cerebro. «Es como un borrador», concluye el clínico y científico.
Referencia
Lyden P, Diniz MA, Bosetti F, Lamb J, Nagarkatti KA, Rogatko A, et al. A multi-laboratory preclinical trial in rodents to assess treatment candidates for acute ischemic stroke. Sci Transl Med[Internet]. 2023[citado 20 oct 2023]; eadg8656(2023). DOI:10.1126/scitranslmed.adg8656
21 octubre 2023 | Fuente: Diarío Médico| Tomado de Neurología
oct
13
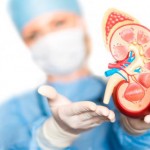 Los investigadores realizaron 69 modificaciones genéticas para lograr evitar el rechazo hiperagudo, la reacción habitual ante un trasplante entre especies diferentes.
Los investigadores realizaron 69 modificaciones genéticas para lograr evitar el rechazo hiperagudo, la reacción habitual ante un trasplante entre especies diferentes.
Obtener órganos de ‘repuesto’, desarrollados en animales y disponibles para el trasplante en humanos, es un objetivo que persiguen diferentes grupos de investigación en todo el mundo.
Aunque en 2022 se llevaron a cabo varios xenotrasplantes experimentales, como la implantación de un corazón de cerdo modificado genéticamente a un paciente de Baltimore que sufría una grave enfermedad cardiaca; este tipo de abordaje todavía está lejos de llegar a la clínica. Antes, se deben solventar desafíos biotecnológicos importantes que plantea el ‘salto’ entre especies, como el rechazo hiperagudo tras el injerto o el riesgo de zoonosis.
Una investigación liderada por científicos de la Universidad de Harvard y la compañía eGenesis allana ese camino al haber conseguido implantar riñones de cerdo editados genéticamente en macacos y lograr unas cifras de supervivencia reseñables. Uno de los ejemplares trasplantados vivió más de dos años con el injerto de riñón. Los detalles de la investigación se publican en la revista Nature.
Para minimizar el riesgo de rechazo y la posibilidad de transmisión de virus porcinos con el trasplante, los investigadores realizaron 69 modificaciones genéticas en el animal donante, un cerdo de Yucatán.
Estas modificaciones pueden agruparse en tres bloques: en primer lugar, eliminaron tres antígenos glicanos, ‘marcadores’ presentes en la superficie de las células que inducen un rechazo inmediato. Además, introdujeron cambios para que las células animales expresaran siete genes humanos con el objetivo de mejorar la tolerancia y neutralizar otros fenómenos asociados al rechazo hiperagudo. Y, por último, inactivaron todas las copias de la genética relacionada con retrovirus porcinos.
En combinación con medicación inmunosupresora, este cóctel de ingeniería genética proporcionó una supervivencia de hasta 758 días a uno de los macacos trasplantados.
CLAVES DEL XENOTRASPLANTE
Una de las principales claves para conseguir esa prolongada supervivencia fue la manipulación para añadir los genes humanizados, implicados en varias vías relacionadas con el rechazo, como la inflamación, la inmunidad innata o la coagulación, tal y como explicaron los investigadores en una rueda de prensa.
Los estudios in vitro, señalan los científicos, mostraron que las células endoteliales renales de los animales con estas ediciones genéticas eran capaces de modular la inflamación de una forma «indistinguible» de las células endoteliales humanas. «Nuestros resultados nos colocan un paso adelante para alcanzar la compatibilidad humana», subrayó Michael Curtis, responsable de eGenesis en el encuentro con la prensa.
Este diseño y desarrollo se trata de una «prueba de concepto» que «apoya el avance hacia el desarrollo clínico» del principal candidato que la compañía eGenesis está diseñando para el trasplante de riñón, denominado EGEN-2784, ha señalado la compañía en un comunicado.
Para Beatriz Domínguez-Gil, directora de la Organización Nacional de Trasplantes (ONT), este diseño «se trata de un modelo que proporciona resultados muy prometedores».
Domínguez-Gil destaca el diseño de modificaciones genéticas que ha permitido alcanzar «una supervivencia prolongada en primates no humanos».
Pero, además, hace hincapié en el hecho de que el desarrollo proporciona «un modelo experimental que nos va a permitir avanzar en el ámbito del xenotrasplante de una forma mucho más segura».
Este diseño permite dar un paso importante «a la hora de demostrar que un abordaje es seguro y eficaz antes de dar el salto a la realización de ensayos clínicos».
Desde esas dos perspectivas, «es un estudio muy novedoso y de mucha relevancia», subraya Domínguez-Gil, que también apunta que la utilización de este tipo de primates no humanos como receptores en los experimentos puede facilitar la traslación posterior de los resultados a la clínica. «Es un modelo probablemente más trasladable a la realidad del humano que los que se han utilizado previamente», destaca.
UN LARGO CAMINO POR RECORRER
De cualquier manera, la directora de la ONT recuerda que «todavía quedan muchísimos pasos en este en ese camino de llevar el xenotrasplante a la clínica».
Queda mucho trabajo por realizar en el ámbito preclínico, subraya Domínguez-Gil. En este sentido, los propios investigadores reconocen en la revista científica que las modificaciones genéticas planteadas deben afinarse para conseguir resultados clínicos.
Pero, además, también hay que abordar las cuestiones éticas que plantea este tipo de procedimientos. «Entre otras cosas, se tiene que decidir cuál es el paciente al que se le va a ofrecer esta opción frente a la alternativa; es decir, qué criterios tiene que cumplir un paciente para entrar en un ensayo clínico de estas características cuando tenemos ya un tipo de trasplante entre humanos muy consolidado, que es una realidad clínica ya habitual y que ofrece extraordinarios resultados», señala.
También hay que abordar cuestiones relacionadas con la protección de los animales, así como la planificación de cómo se va a lograr que estos tratamientos «extraordinariamente costosos» puedan llegar a los pacientes de una forma equitativa, plantea la directora de la ONT.
«Hay muchas cuestiones que avanzar y que tener en cuenta, pero yo creo que en los próximos 10 años sí vamos a ver un salto importante a la clínica de esta opción terapéutica», concluye Domínguez-Gil.
Referencia
Anand RP, Layer JV, Heja D, Hirose T, Lassiter G, Firl D, et al. Design and testing of a humanized porcine donor for xenotransplantation. Nature[Internet]. 2023[citado 12 oct 2023]; 622, 393–401. https://doi.org/10.1038/s41586-023-06594-4
13 octubre 2023│Fuente: El Mundo│ Tomado de Salud
oct
9
 Un equipo de investigación internacional, dirigido por científicos de la Universidad de Bergen, ha lanzado una iniciativa de investigación financiada por la Unión Europea (UE) para descubrir el papel del virus de Epstein-Barr (VEB) en la aparición y progresión la esclerosis múltiple (EM), basándose en avances recientes que implican fuertemente que la infección por el virus de Epstein-Barr es el desencadenante del desarrollo de la esclerosis múltiple.
Un equipo de investigación internacional, dirigido por científicos de la Universidad de Bergen, ha lanzado una iniciativa de investigación financiada por la Unión Europea (UE) para descubrir el papel del virus de Epstein-Barr (VEB) en la aparición y progresión la esclerosis múltiple (EM), basándose en avances recientes que implican fuertemente que la infección por el virus de Epstein-Barr es el desencadenante del desarrollo de la esclerosis múltiple.
La investigación en la que se basa este nuevo proyecto, publicada en Science en 2022, muestra que la infección por el virus de Epstein-Barr (VEB) aumenta en gran medida el riesgo de desarrollar EM y que es casi imposible desarrollar EM sin estar infectado primero por el virus. El objetivo es desarrollar un nuevo tratamiento para la esclerosis múltiple, dirigido al factor subyacente de la enfermedad en lugar de a las consecuencias posteriores. Además, si tiene éxito, identificará a las personas con alto riesgo de desarrollar EM después de la infección por EBV y brindará la posibilidad de realizar una prevención primaria de la enfermedad en personas de alto riesgo. El proyecto tiene el potencial de proporcionar evidencia mecanicista de que el VEB es un requisito previo para el desarrollo y la progresión de la EM, lo que podría formar la base para desarrollar estrategias para erradicar la enfermedad.
Los autores consideran que esta innovadora iniciativa de investigación tiene un gran potencial para mejorar las opciones de tratamiento para las personas que viven con EM. Al explorar la intrincada conexión EBV-MS, también ofrece la oportunidad de una mejor comprensión de la enfermedad y el desarrollo de medidas preventivas. En última instancia, esto conduce a una mejora en la calidad de vida de las personas que viven con EM y acerca un paso más a un futuro libre de la carga de la EM.
Referencia
Robinson WH, Steinman L. Epstein-Barr virus and multiple sclerosis. Science [Internet]. 2022[citado 8 oct 2023]; 375(6578): 264-265. DOI: 10.1126/science.abm7930
9 octubre 2023|Fuente: Neurologia.com| Tomado de Noticia
oct
5
 Los ingenieros del MIT (Instituto Tecnológico de Massachusetts) han creado un modelo computacional que predice cómo responderá el cuerpo humano a diferentes versiones de “insulina sensible a la glucosa” (GRI). El objetivo es poder diseñar GRI novedosos y obtener mejores predicciones sobre si un GRI en particular funcionaría en humanos antes de lanzar un ensayo clínico de alto coste.
Los ingenieros del MIT (Instituto Tecnológico de Massachusetts) han creado un modelo computacional que predice cómo responderá el cuerpo humano a diferentes versiones de “insulina sensible a la glucosa” (GRI). El objetivo es poder diseñar GRI novedosos y obtener mejores predicciones sobre si un GRI en particular funcionaría en humanos antes de lanzar un ensayo clínico de alto coste.
Esta insulina “inteligente” circularía por el cuerpo de forma pasiva y entraría en acción sólo cuando sea necesario. Así, se podría inyectar con menos frecuencia y ayudaría al cuerpo a mantener niveles normales de azúcar en sangre durante períodos de tiempo más prolongados. Cristina Tejera, médico especialista en Endocrinología y Nutrición y miembro del Área de Diabetes de la Sociedad Española de Endocrinología y Nutrición (SEEN), afirma que estas insulinas serían una copia casi perfecta de la insulina endógena que se produce a nivel pancreático. “Disponer de ellas va a suponer un punto de inflexión en el tratamiento de la diabetes que precise insulina. Estos pacientes mejorarán el control glucémico, se disminuirán las complicaciones e incrementarán su calidad de vida”.
En el estudio, publicado en ACS Pharmacology and Translation, el equipo del MIT utilizó el modelo para analizar los resultados de un ensayo clínico de GRI que se suspendió porque el fármaco mostró poco efecto en humanos. Su análisis encontró que el fármaco, que había funcionado bien en estudios con animales, actuaba de manera diferente en el cuerpo humano debido a diferencias en el comportamiento de un receptor de azúcar que ayuda a controlar la acción del fármaco.
Un proceso complejo
Tejera indica que estas insulinas ya llevan un largo recorrido, pero el paso de los resultados obtenidos in vitro a los datos en práctica clínica real está siendo complicado. “Es necesario evaluar su seguridad, la dosis necesaria en cada persona y posibles efectos secundarios”, resalta.
Así, establece algunos de los obstáculos que deben superar este tipo de insulinas. Entre ellos, destaca el detectar la glucemia de forma selectiva y que sus componentes no den lugar a efectos secundarios o algún otro tipo de toxicidad. Además, incide en que tienen que ser capaces de responder en el rango de glucemia fisiológico o bien a un rango de glucemia de seguridad previamente preestablecido. Además, deben actuar de forma reactiva, rápida y reversible a los cambios de la glucemia, de forma que solo trabaje cuando la glucemia está por encima de rango.
El caso de MK-2640
En los últimos años, diferentes compañías farmacéuticas han estado trabajando en el desarrollo de GRI. En 2016, uno llamado MK-2640 llegó a ensayo clínico de fase I porque había mostrado resultados prometedores en estudios preclínicos realizados en animales. Sin embargo, cuando se probó en humanos, mostró un “efecto realmente mediocre”, indica Michael Strano, autor principal del nuevo estudio.
MK-2640 fue diseñado con un nuevo mecanismo de respuesta a la glucosa conocido como aclaramiento competitivo. La insulina está diseñada para unirse a receptores celulares que normalmente se unen a un azúcar llamado manosa. Cuando los niveles de azúcar en sangre son bajos, las moléculas de GRI se unen a estos receptores y se eliminan del cuerpo. Sin embargo, cuando el nivel de azúcar en la sangre aumenta, el GRI no puede unirse a los receptores y permanece en el torrente sanguíneo, donde ayuda a reducir los niveles de azúcar.
Modelar computacionalmente el sistema glucorregulador
Casi al mismo tiempo, el laboratorio de Strano estaba desarrollando una forma de modelar computacionalmente el sistema glucorregulador de humanos y otros animales. El modelo constaba de un conjunto de ecuaciones que describen cómo se comportan la glucosa y la insulina en diferentes compartimentos del cuerpo humano, como los vasos sanguíneos, los músculos y el tejido adiposo. Esto les permite predecir los niveles de glucosa en sangre en órganos como el hígado, el estómago y el cerebro, para una variedad de especies, incluidos los humanos.
“Este es un modelo muy detallado y tiene parámetros que se han ajustado con una gran cantidad de datos clínicos y de animales, por lo que es capaz de recrear fielmente experimentos que los investigadores realizan tanto en humanos como en animales”, sostiene Strano.
Por ejemplo, el modelo se puede utilizar para predecir cómo cambiarán los niveles de azúcar en sangre después de una comida o qué sucederá si se infunde glucosa en el cuerpo, en función de la cantidad de insulina disponible.
Strano y su equipo de estudiantes decidieron ver si su modelo computacional podía revelar por qué el fármaco MK-2640 no funcionó como se esperaba. Así, los investigadores encontraron que las diferencias entre especies en la capacidad de eliminación del receptor de manosa explicaban el débil desempeño del GRI en ensayos en humanos. Debido a esa diferencia, los niveles de GRI no cambiaron significativamente en humanos en comparación con los de los animales.
El modelo también mostró que, si la versión humana del receptor de manosa estuviera sintonizada para funcionar de manera similar a la de los animales, el fármaco probablemente habría funcionado mucho mejor en los ensayos clínicos.
Diseñando mejores medicamentos
El laboratorio de Strano también está trabajando en otra versión del modelo que incorporaría los efectos del glucagón, una hormona que aumenta el azúcar en sangre y puede prevenir una hipoglucemia potencialmente mortal. Los investigadores han teorizado que tratar a estos pacientes con una combinación de insulina y glucagón podría ofrecer un mejor control de los niveles de azúcar en sangre que la insulina sola.
El enfoque general de diseñar fármacos que respondan a condiciones internas del cuerpo también podría ser beneficioso para tratar una amplia variedad de otras enfermedades. “Esto podría conducir a una nueva generación de fármacos que no sólo circulen pasivamente dentro del cuerpo y esperen a actuar, sino que estén sintonizados para alcanzar un determinado criterio de valoración terapéutico y regular su potencia en consecuencia”, afirma Strano.
Las personas con diabetes en España se han incrementado en un 42 por ciento desde 2019. Unas cifras que se ven reflejadas en los casi seis millones de personas que padecen diabetes en nuestro país y que, en 2025, podrían llegar a ser nueve millones. Según Farmaindustria, el tratamiento de la diabetes y sus complicaciones asociadas generan un gasto global de 760.000 millones de euros. En la actualidad, hay más de 470 nuevos medicamentos en fase de investigación, tanto para el tratamiento de la enfermedad como de sus complicaciones. Por ello, la llegada de este tipo de insulinas “inteligentes” a los pacientes podría ser toda una revolución.
Referencia
Fan Yang J, Yang S, Gong X, Bakh NA, Zhang G, Wang AB, et al. In Silico Investigation of the Clinical Translatability of Competitive Clearance Glucose-Responsive Insulins. ACS Pharmacol Transl Sci[Internet]. 2023[citado 4 oct 2023]; XXXX, XXX, XXX-XXX. https://doi.org/10.1021/acsptsci.3c00095
5 octubre 2023 | Fuente: Gaceta Médica| Tomado de Investigación
oct
5
 El Director de la Organización Panamericana de la Salud (OPS) suscribió un nuevo acuerdo de cooperación técnica con autoridades de salud, ciencia y tecnología de Argentina con el fin de fortalecer y aumentar las capacidades de desarrollo y producción futura de vacunas ARNm con destino regional.
El Director de la Organización Panamericana de la Salud (OPS) suscribió un nuevo acuerdo de cooperación técnica con autoridades de salud, ciencia y tecnología de Argentina con el fin de fortalecer y aumentar las capacidades de desarrollo y producción futura de vacunas ARNm con destino regional.
“Con este acuerdo estamos reforzando el ecosistema de producción de vacunas ARNm y dando mayor sustentabilidad” al proyecto de transferencia de tecnología de la OPS/OMS en Argentina, afirmó el Director de la OPS, doctor Jarbas Barbosa. Además, agregó que el desarrollo futuro de estas vacunas en el país “ayudará a reducir la dependencia externa de la región a esta tecnología y avanzar hacia un acceso más equitativo”.
El Director de la Organización Panamericana de la Salud (OPS) suscribió hoy un nuevo acuerdo de cooperación técnica con autoridades de salud, ciencia y tecnología de Argentina con el fin de fortalecer y aumentar las capacidades de desarrollo y producción futura de vacunas ARNm con destino regional.
El acuerdo tiene lugar en el marco de la Plataforma regional para la innovación y producción de vacunas y otras tecnologías sanitarias de la OPS, y complementa el programa de la Organización Mundial de la Salud (OMS) y Medicines Patent Pool (MPP) de transferencia de tecnología para el desarrollo de vacunas ARNm en países de ingresos medios y bajos, que integran Sinergium Biotech, de Argentina, y el Instituto de Inmunobiología Bio-Manguinhos, de Brasil, en calidad de centros regionales.
Ahora, la Administración Nacional de Laboratorios e Institutos de Salud “Dr. Carlos Malbrán” (ANLIS-Malbrán), dependiente del Ministerio de Salud de Argentina, formará parte de la cadena de producción a través del desarrollo de nanopartículas de lípidos, insumos esenciales en la producción de las vacunas ARNm.
La OPS, con apoyo financiero de la Iniciativa Global para la Equidad en Vacunas de Canadá (CanGIVE), contribuirá con la provisión de equipamiento e insumos para que la ANLIS-Malbrán produzca las nanopartículas. Esto también contribuirá a la sostenibilidad de la producción, al no tener que recurrir a proveedores externos para obtener este recurso.
Durante la reunión, la Ministra de Salud de la Nación, Carla Vizzotti, indicó: “Resulta sumamente importante que Argentina haya sido seleccionada junto a Brasil para realizar la transferencia de tecnología de una vacuna de ARN mensajero» y añadió que «después de un largo año de trabajo junto a la Agencia I+D+I, el Malbrán, el Ministerio de Salud y una planta de producción privada llegamos a la firma de este acuerdo que nos permitirá avanzar con equipamiento, fortalecimiento y la transferencia de la tecnología necesaria para favorecer a la región».
Además, el acuerdo incluye a la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación (Agencia I+D+i) que contribuirá con la promoción de estudios y la creación de capacidades en Argentina. En ese sentido, el presidente de la Agencia, Fernando Peirano, expresó que “Argentina tiene garantizado y universalizado el derecho a la salud y esto también puede ser un buen motor para poner en valor nuestra capacidad industrial y científica para desarrollar nuevas soluciones y es por eso que venimos acompañando el proceso”.
La firma tuvo lugar durante la visita oficial del doctor Barbosa a la Argentina que incluirá un recorrido por la planta de Sinergium Biotech para conocer el progreso del proyecto y terminar de suscribir el acuerdo.
Más avances hacia la producción regional de vacunas ARNm
Con el fin de seguir avanzando hacia la producción de vacunas ARNm en la región, la OPS, la Fundación Oswaldo Cruz (Fiocruz) y el Instituto Butantán, principales productores de inmunobiológicos de Brasil, lanzaron recientemente la primera edición de un curso conjunto sobre desarrollo y producción de vacunas que busca fortalecer las capacidades de los recursos humanos en los países del Mercosur.
Asimismo, en julio pasado, la OPS firmó una carta acuerdo con Bio-Maguinhos/ Fiocruz para la realización de ensayos preclínicos de una vacuna ARNm que se está desarrollando en Brasil. Si esta tecnología se demuestra segura y efectiva, podrá licenciarse sin costo para países de bajos y medianos ingresos en la región.
5 octubre 2023 | Fuente: OPS |Tomado de Noticias Nota de prensa
oct
3
 El sistema, desarrollado por el Instituto de Bioingeniería de Cataluña, está fabricado a partir de células de pacientes y es el primer modelo 3D de músculo capaz de reproducir el daño que provoca la distrofia muscular de Duchenne.
El sistema, desarrollado por el Instituto de Bioingeniería de Cataluña, está fabricado a partir de células de pacientes y es el primer modelo 3D de músculo capaz de reproducir el daño que provoca la distrofia muscular de Duchenne.
La Distrofia Muscular de Duchenne (DMD) es la distrofia muscular más común diagnosticada durante la infancia, con alrededor de 20.000 casos nuevos cada año. Se trata de un desorden progresivo del músculo que causa la pérdida de su función de manera que los afectados terminan perdiendo totalmente su independencia y sufriendo problemas médicos graves, con una expectativa de vida promedio de 30 años.
La causa de la enfermedad es una mutación en el gen que codifica la distrofina, una proteína que amortigua el impacto de la contracción de los músculos en la membrana de las células. Debido a que la distrofina está ausente, las células musculares se dañan fácilmente.
En la actualidad, no existe una cura para la DMD y uno de los desafíos principales con los que se encuentra la comunidad investigadora es crear modelos artificiales que consigan recrear de manera eficaz el daño presente en los músculos de los pacientes, para poder estudiar nuevos tratamientos en el laboratorio.
Un estudio del Instituto de Bioingeniería de Cataluña (IBEC) publicado esta semana en la revista Biofabrication, describe el desarrollo de un modelo 3D de músculo que es capaz de reproducir el daño presente en el tejido muscular de las personas afectadas por la distrofia muscular de Duchenne.
El sistema, fabricado a partir de ingeniería de tejidos con células de pacientes, contiene fibras musculares capaces de contraerse al aplicar un estímulo eléctrico. Una característica esencial para crear un modelo artificial de músculo que permita llevar a cabo estudios preclínicos de fármacos para tratar la DMD.
El trabajo lo ha liderado Juanma Fernández Costa, investigador senior del IBEC, con Ainoa Tejedera Villafranca, estudiante de doctorado del IBEC, como primera autora. Ambos pertenecen al grupo de Biosensores para bioingeniería, liderado por el profesor de investigación ICREA Javier Ramón Azcón.
“Lo novedoso de este estudio es que hemos buscado modelizar la causa principal de la enfermedad, que es el daño del sarcolema, la membrana de las células musculares. Para nosotros era muy importante poder replicarlo en el laboratorio y lo hemos conseguido. No se había hecho antes”, comenta Juanma Fernández.
“Trabajamos mucho tiempo en diferentes protocolos hasta conseguir que apareciera ese daño en las células de pacientes, pero no en las de control, de personas sin Duchenne. Es delicado, porque si estimulas el músculo, puedes causar rotura de fibras también en las células sanas, igual que ocurre cuando hacemos deporte y tenemos agujetas”, añade Ainoa Tejedera.
El objetivo de los investigadores era conseguir un modelo que permitiera comprobar si los fármacos son capaces de revertir ese daño en las células. No atacar los síntomas, que es en lo que se centran los tratamientos paliativos, sino ir al origen de la enfermedad.
Aunque ya han testado algunos fármacos en este modelo, están trabajando en desarrollar un modelo mejorado, conocido como órgano-en-un-chip. Se trata de una plataforma más avanzada que añade sensores y un sistema de microfluídica al modelo de músculo 3D. Esto permitirá monitorizar el daño celular de forma más eficiente y testar diferentes moléculas o fármacos con mayor rapidez.
La importancia de colaborar con los pacientes y sus familias
El trabajo, que forma parte de la tesis doctoral de Tejedera, ha recibido financiación de Duchenne Parent Project España (DPPE), una asociación sin ánimo de lucro creada y dirigida por madres y padres de niños con Distrofia Muscular de Duchenne y Becker.
Esta colaboración representa otra manera de hacer llegar la ciencia a la sociedad. En palabras de Fernández: “es un ejemplo fantástico de cómo los investigadores podemos hacer piña con los pacientes y sus familias para buscar objetivos comunes”.
Silvia Ávila, presidenta de la asociación, destaca que “Es un orgullo saber que hemos financiado un proyecto que puede acelerar el proceso de investigación, a través de la creación de un músculo artificial en un chip. Por un lado, reducimos el uso de animales en laboratorio y, por otro lado, acortamos el tiempo de convertir una posible terapia en realidad. Básico para esta enfermedad que va restando tiempo y calidad de vida a nuestros hijos».
Referencia
Tejedera-Villafranca A, Montolio M, Ramón-Azcón J, Fernández-Costa J. Mimicking sarcolemmal damage in vitro: a contractile 3D model of skeletal muscle for drug testing in Duchenne muscular dystrophy. Biofabrication[Internet]. 2023[citado 3 oct 2023]; 15(4). DOI 10.1088/1758-5090/acfb3d

