mar
7
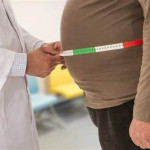 La Organización Mundial de la Salud (OMS) advirtió, en ocasión del Día Mundial de la Obesidad, sobre el incremento de esa enfermedad a nivel global, con más de mil millones de personas que la padecen. Desde 1990 el número de adultos obesos se multiplicó por dos y los casos en niños y adolescentes se cuadruplicaron, por lo que esta jornada ha servido para divulgar el terrible daño que conlleva para el organismo humano una dieta alta en grasas y azúcares. La jornada es convocada por la Federación Mundial de la Obesidad para tratar esta afección, que alcanza proporciones epidémicas a nivel mundial. Según la OMS la situación global es preocupante, a partir de un nuevo estudio que encontró que más de mil millones de personas en el mundo tenía obesidad en el año 2022. Tal y como resaltó esa agencia sanitaria en un comunicado a través de su portal web, la obesidad y el sobrepeso constituyen formas de malnutrición, junto a otras como la desnutrición (emaciación, peso insuficiente y retraso en el crecimiento) o insuficiencia de vitaminas y minerales.
La Organización Mundial de la Salud (OMS) advirtió, en ocasión del Día Mundial de la Obesidad, sobre el incremento de esa enfermedad a nivel global, con más de mil millones de personas que la padecen. Desde 1990 el número de adultos obesos se multiplicó por dos y los casos en niños y adolescentes se cuadruplicaron, por lo que esta jornada ha servido para divulgar el terrible daño que conlleva para el organismo humano una dieta alta en grasas y azúcares. La jornada es convocada por la Federación Mundial de la Obesidad para tratar esta afección, que alcanza proporciones epidémicas a nivel mundial. Según la OMS la situación global es preocupante, a partir de un nuevo estudio que encontró que más de mil millones de personas en el mundo tenía obesidad en el año 2022. Tal y como resaltó esa agencia sanitaria en un comunicado a través de su portal web, la obesidad y el sobrepeso constituyen formas de malnutrición, junto a otras como la desnutrición (emaciación, peso insuficiente y retraso en el crecimiento) o insuficiencia de vitaminas y minerales.
La relevancia médica de la obesidad yace, principalmente, en la relación que tiene con un gran número de padecimientos que afectan a sistemas diferentes del cuerpo y que a menudo pueden llegar a ser letales o crónicas. Por ejemplo, padecer de obesidad pone a las personas en un mayor riesgo de desarrollar enfermedades cardiovasculares, diabetes e incluso algunos tipos de cáncer.
La OMS subrayó la importancia de prevenirla y controlarla desde las primeras etapas de la vida y hasta la edad adulta, a través de la alimentación, la actividad física y la atención necesaria, y recordó que se trata de una enfermedad crónica compleja, cuyas causas se conocen bien. Los dos países que lideran la obesidad en el mundo son Estados Unidos con un 13 por ciento de niños obesos y Egipto, con un 35 por ciento de adultos en esa situación. En todo el mundo la gran mayoría de personas obesas son mujeres. Otros datos apuntan a que la capacidad económica de las personas no es un factor de sobrepeso u obesidad, por lo que los expertos realmente atribuyen el actual aumento a los hábitos alimenticios y el creciente bombardeo publicitario de las franquicias de comida rápida, así como la vida sedentaria de las grandes urbes. Actualmente no es necesario llegar a la obesidad para morir por alguna complicación propia del sobrepeso, como enfermedades cardiovasculares, por eso es importante mantener una dieta sana, baja en grasas y azucares.
04 marzo 2024 | Fuente: Prensa Latina | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A
mar
5
 1 de marzo de 2024, Port St. Lucie, Florida: Investigadores de la Clínica Cleveland han descubierto un mecanismo clave utilizado por el virus del herpes asociado al sarcoma de Kaposi (KSHV), también conocido como herpesvirus humano 8 (HHV8), para inducir cáncer. La investigación apunta a nuevas opciones de tratamiento eficaces para los cánceres asociados al KSHV, como el sarcoma de Kaposi, el linfoma de derrame primario y la enfermedad de Castleman multicéntrica asociada al HHV8.
1 de marzo de 2024, Port St. Lucie, Florida: Investigadores de la Clínica Cleveland han descubierto un mecanismo clave utilizado por el virus del herpes asociado al sarcoma de Kaposi (KSHV), también conocido como herpesvirus humano 8 (HHV8), para inducir cáncer. La investigación apunta a nuevas opciones de tratamiento eficaces para los cánceres asociados al KSHV, como el sarcoma de Kaposi, el linfoma de derrame primario y la enfermedad de Castleman multicéntrica asociada al HHV8.
El virus herpes asociado al sarcoma de Kaposi (KSHV), activa una vía específica para impulsar la infección viral persistente y el crecimiento celular, allanando el camino para la formación de tumores.
Nuestros hallazgos tienen implicaciones significativas: los virus causan entre el 10% y el 20% de los cánceres en todo el mundo, un número que aumenta constantemente a medida que se realizan nuevos descubrimientos. El tratamiento de los cánceres inducidos por el virus con terapias estándar contra el cáncer puede ayudar a reducir los tumores que ya están allí, pero no soluciona el problema subyacente del virus», dijo Jun Zhao, Ph.D., del Centro de Investigación e Innovación de la Florida de la Clínica Cleveland. «Comprender cómo los patógenos transforman una célula sana en una célula cancerosa descubre vulnerabilidades explotables y nos permite fabricar y reutilizar medicamentos existentes que pueden tratar eficazmente las neoplasias malignas asociadas a virus».
El estudio de Nature Communications, dirigido por el Dr. Zhao, revela que KSHV manipula dos enzimas humanas llamadas CDK6 y CAD para remodelar la forma en que las células humanas producen nuevos nucleótidos, los componentes básicos del ADN y el ARN, y procesan la glucosa. Los cambios en la forma en que crecen las células infectadas y la persistencia del KSHV ponen a las células en un riesgo mucho mayor de formar tumores y desempeñan un papel crucial en la causa del cáncer.
El equipo demostró que el virus activa una vía específica que impulsa el metabolismo y la proliferación celular. La inhibición de este proceso con los medicamentos existentes para el cáncer de mama aprobados por la FDA redujo la replicación del KSHV, bloqueó la progresión del linfoma y redujo los tumores existentes en modelos preclínicos.
Al igual que otros herpesvirus, el KSHV a menudo no presenta síntomas al principio y permanece en el cuerpo después de la infección primaria. El virus permanece latente, suprimido por el sistema inmunitario. Sin embargo, el KSHV puede reactivarse cuando la inmunidad se debilita, como en las personas mayores, las personas con VIH/SIDA y los receptores de trasplantes. En estos grupos de alto riesgo, el virus ahora activo puede desencadenar cánceres agresivos.
Los cánceres inducidos por KSHV son de acción rápida, agresivos y difíciles de tratar. Se estima que el 10% de las personas en América del Norte y el norte de Europa tienen KSHV, pero esto se extiende por todo el mundo. Se estima que más del 50% de las personas en partes del norte de África tienen el virus. Los expertos estiman que estas tasas son más altas, ya que el KSHV a menudo no se diagnostica debido a la falta de síntomas. Estos hallazgos tienen implicaciones que van más allá de KSHV; los investigadores pueden aplicar el conocimiento sobre el KSHV a otros virus asociados con el cáncer que podrían usar el mismo proceso para causar cáncer.
Para comprender los procesos metabólicos de las células y descubrir las vulnerabilidades del virus, el Dr. Zhao colaboró con Michaela Gack, Ph.D., directora científica del Centro de Investigación e Innovación de Florida.
Las células cancerosas que se replican rápidamente reprograman el metabolismo para impulsar el crecimiento. Mientras tanto, la mayoría de los virus no pueden producir energía o las moléculas necesarias por sí mismos, por lo que dependen de las células humanas para que hagan el trabajo por ellos. El equipo descubrió que el virus se apodera de la proteína huésped CDK6 y CAD, lo que hace que las células infectadas produzcan metabolitos adicionales, lo que permite una replicación más rápida del virus y una proliferación descontrolada de las células.
Ver artículo: Wan Q, Tavakoli L, Yu Anrew, Zhou R, Liu Q, Feng S, et al. DHijacking of nucleotide biosynthesis and deamidation-mediated glycolysis by an oncogenic herpesvirus. Nature Communications[Internet].2024[citado 2 mar 2024],15(1442). DOI https://doi.org/10.1038/s41467-024-45852-5
01 marzo| Fuente: EureKalert| Tomado de | Comunicado de prensa
mar
4
 La iniciativa Rayos de Esperanza ayuda a los países a fortalecer sus capacidades para mejorar el diagnóstico, la estadificación y el tratamiento del cáncer, afirmó la directora de la División de Salud Humana del OIEA, May Abdel-Wahab.
La iniciativa Rayos de Esperanza ayuda a los países a fortalecer sus capacidades para mejorar el diagnóstico, la estadificación y el tratamiento del cáncer, afirmó la directora de la División de Salud Humana del OIEA, May Abdel-Wahab.
Ese programa del Organismo Internacional de Energía Atómica (OIEA) apoya la investigación, la enseñanza y la innovación a escala mundial relacionada con esa enfermedad, ya que solo el cinco por ciento del gasto mundial en cáncer va dirigido a países de ingresos medianos y bajos. Sin embargo, se calcula que para 2030, el 70 por ciento de las muertes por esa enfermedad serán en esas naciones, por lo que Rayos de Esperanza apuesta por cambiar dicha realidad y ayudar a las de menos recursos para aumentar el acceso a la atención oncológica.
Abdel-Wahab aseguró que más de una tercera parte de todos los tipos de cáncer pueden evitarse, y algunos de los más comunes, como el cervicouterino, de mama, de cabeza y cuello y el colorrectal, tienen cura si se detectan rápido y se tratan de manera adecuada. Las políticas y programas nacionales de lucha contra el cáncer, si se conciben y aplican de manera adecuada, ayudarán a reducir la carga del cáncer y a mejorar los servicios prestados a los pacientes con cáncer y sus familias, independientemente del contexto de cada país, precisó. Las alarmantes estadísticas del cáncer, junto con una sólida capacidad de apoyo internacional, llevaron al OIEA a ser el primero en poner en marcha una iniciativa como Rayos de Esperanza, cuyo objetivo es ayudar a los países en desarrollo a satisfacer sus necesidades urgentes y mejorar las capacidades de la medicina radiológica.
Rayos de Esperanza respaldará la introducción o la ampliación sostenible e integral de la radioterapia e incluirá el apoyo a los centros de referencia regionales y la innovación. En tal sentido, los países con instalaciones de radioterapia limitadas o sin ellas recibirán respaldo para establecer sus primeros servicios o ampliar sus capacidades de diagnóstico mediante la imagen, a fin de que logren llegar a más personas.
La iniciativa del OIEA contribuye al cumplimiento de la Agenda 2030 y del Objetivo de Desarrollo Sostenible 3 (Salud y bienestar), en particular la meta de reducir en un tercio la mortalidad prematura por enfermedades no transmisibles.
29 febrero 2024 | Fuente: Prensa Latina| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A
mar
1
 El ictus isquémico es la segunda causa de muerte en todo el mundo y se produce cuando el flujo sanguíneo no puede llegar al cerebro debido a una obstrucción. Durante un momento más o menos largo, el cerebro no recibe oxígeno y esto provoca daños y deterioro funcional. La hipertensión es el factor de riesgo modificable más frecuente de ictus y se asocia con peores recuperaciones.
El ictus isquémico es la segunda causa de muerte en todo el mundo y se produce cuando el flujo sanguíneo no puede llegar al cerebro debido a una obstrucción. Durante un momento más o menos largo, el cerebro no recibe oxígeno y esto provoca daños y deterioro funcional. La hipertensión es el factor de riesgo modificable más frecuente de ictus y se asocia con peores recuperaciones.
Actualmente, solo existe un tratamiento farmacológico para atenuar los efectos del ictus, pero no sirve para todos los pacientes y además está asociado a algunos efectos adversos importantes. Ahora, investigadores del Instituto de Neurociencias de la UAB (INc UAB) han demostrado que el vorinostat (ácido suberoilanilida hidroxámico) tiene un gran potencial a la hora de tratar las lesiones cerebrales derivadas.
Este fármaco, que se utiliza en el tratamiento de un tipo de linfoma cutáneo, inhibe las deacetilasas de histonas, unas enzimas que regulan la expresión génica a partir de modificar los niveles de acetilación de un grupo de proteínas llamadas histonas.
El artículo publicado en la revista Biomedicine and Pharmacotherapy, el grupo de investigación demuestra en un modelo de ictus en ratas hipertensas muy cercano a la situación clínica, como el uso del fármaco hace que los animales mejoren los déficits neurológicos, que se reduzca su daño cerebral y que se atenúe la respuesta inflamatoria, entre otros efectos.
«Vimos que tan solo con una única dosis de fármaco, aplicado durante el período de reperfusión, se conseguían prevenir múltiples factores asociados a la patología del ictus. Esto abre camino a la investigación con este tipo de tratamiento más allá de la fase preclínica», explica la primera autora del artículo Andrea Díaz, investigadora de la UAB y del Centro de Investigación Biomédica en Red Sobre Enfermedades Neurodegenerativas (CIBERNED).
Además, los investigadores demuestran que el tratamiento protege no solo al cerebro, sino también a los vasos que lo rodean, y lo hace incluso pasadas unas horas después del ictus.
«Dada la necesidad clínica urgente de fármacos para tratar el ictus isquémico agudo, y que el vorinostat está aprobado para uso humano, estos hallazgos deben incentivar el abordaje de más investigaciones preclínicas que evalúen, por ejemplo, su efecto en hembras y animales viejos, en modelos animales con otras comorbilidades comunes de ictus como la diabetes, sus efectos a largo plazo, etc. Esto abriría el camino para el correcto diseño de futuros ensayos clínicos que prueben su eficacia y seguridad en pacientes que han sufrido un ictus», concluye el coordinador del estudio Francisco Jiménez-Altayó, investigador del Departamento de Farmacología, Terapéutica y Toxicología de la UAB y del Área de enfermedades cardiovasculares del Centro de Investigación Biomédica en Red (CIBERCV).
Ver artículo: Díaz Pérez A, Pérez B, Manich G, García Aranda J, Navarro X, Penas C, et al. Histone deacetylase inhibition by suberoylanilide hydroxamic acid during reperfusion promotes multifaceted brain and vascular protection in spontaneously hypertensive rats with transient ischaemic stroke. Biomedicine & Pharmacotherapy[Internet].2024[citado 29 feb 2024];172. https://doi.org/10.1016/j.biopha.2024.116287
28 febrero 2024| Fuente: EurekAlert| Tomado de| Comunicado prensa
feb
28
 El estrés hace que ciertos glóbulos blancos llamados neutrófilos formen estructuras pegajosas en forma de red que hacen que los tejidos del cuerpo sean más susceptibles a la metástasis.
El estrés hace que ciertos glóbulos blancos llamados neutrófilos formen estructuras pegajosas en forma de red que hacen que los tejidos del cuerpo sean más susceptibles a la metástasis.
Un estudio publicado en ´Cancer Cell´ desvela los mecanismos por los que el estrés crónico puede ayudar a que el cáncer se propague. En concreto, los investigadores del Cold Spring Harbor Laboratory (CSHL) de Estados Unidos descubrieron que el estrés hace que ciertos glóbulos blancos llamados neutrófilos formen estructuras pegajosas en forma de red que hacen que los tejidos del cuerpo sean más susceptibles a la metástasis. El hallazgo podría apuntar a nuevas estrategias de tratamiento que detengan la propagación del cáncer antes de que comience.
El equipo llegó a su descubrimiento imitando el estrés crónico en ratones con cáncer. Primero extirparon tumores que habían estado creciendo en los senos de los ratones y propagando células cancerosas a sus pulmones. Luego, expusieron a los ratones al estrés. Así, sorprendidos, observaron un aumento de lesiones metastásicas en estos animales. En concreto, el número de metástasis se cuadruplicó.
El equipo descubrió que las hormonas del estrés llamadas glucocorticoides actuaban sobre los neutrófilos. Estos neutrófilos «estresados» formaron estructuras similares a telarañas llamadas NET (trampas extracelulares de neutrófilos). Los NET se forman cuando los neutrófilos expulsan el ADN. Normalmente, pueden defendernos de microorganismos invasores. Sin embargo, en el cáncer, los NET crean un entorno propicio para la metástasis. Asimismo, el equipo descubrió que el estrés crónico provocaba que la formación de NET modificara el tejido pulmonar incluso en ratones sin cáncer.
Para confirmar que el estrés desencadena la formación de NET, lo que lleva a un aumento de la metástasis, el equipo realizó tres pruebas. Primero, eliminó los neutrófilos de los ratones utilizando anticuerpos. A continuación, inyectó a los animales un fármaco destructor de NET. Por último, el equipo de investigadores utilizó ratones cuyos neutrófilos no podían responder a los glucocorticoides. Cada prueba logró resultados similares. Los ratones estresados a no desarrollaron más metástasis.
El equipo también especula sobre si futuros fármacos que prevengan la formación de NET podrían beneficiar a los pacientes cuyo cáncer aún no ha hecho metástasis. Estos nuevos tratamientos podrían retardar o detener la propagación del cáncer, ofreciendo un alivio muy necesario.
Ver artículo completo: Yan He X, Gao Y, Ng D, Vakoc CR, Van Aelst L, Egeblad M, et al. Chronic stress increases metastasis via neutrophil-mediated changes to the microenvironment. Cancer Cell[Internet]. 2024[ citado 24 feb 2024].DOI:https://doi.org/10.1016/j.ccell.2024.01.013
23 febrero 2024| Fuente: IMMédico| Tomado de | Noticia
feb
20
 Caminar es un ejercicio saludable, sencillo y económico, sin embargo, practicarlo incorrectamente ocasiona dolores y malestar físico, por lo que hay que evitar los errores, según un artículo publicado en National Geographic.
Caminar es un ejercicio saludable, sencillo y económico, sin embargo, practicarlo incorrectamente ocasiona dolores y malestar físico, por lo que hay que evitar los errores, según un artículo publicado en National Geographic.
Tras consultar opiniones de varios expertos, el escrito destaca cinco aspectos a tener en cuenta al dar una caminata, pues hacerlo correctamente ayuda a prevenir desde enfermedades
cardíacas, diabetes e hipertensión arterial hasta el cáncer. Aunque se trata de un ejercicio sencillo, hay que evitar las lesiones y, para ello, conviene prestar mucha atención a la hora de elegir las mejores zapatillas de andar para no dañar los pies. Se sugiere elegir un calzado deportivo que ofrezca una suela que soporte el impacto de la marcha, sea cómodo y se ajuste
correctamente. Llevar un calzado mal ajustado puede provocar rozaduras, ampollas por fricción, llagas en los dedos y dolor general, y convertir una actividad placentera en una molestia. Los especialistas aseguran que al andar los brazos también desempeñan un papel importante, pues actúan como contrapeso de las piernas en un movimiento natural. Aconsejan mover cada brazo en oposición al movimiento de la pierna e intentar relajar las extremidades superiores y que se alternen con naturalidad, pues dejarlas a los lados o balancearlas fuertemente puede reducir la velocidad de la marcha. Aseguran también que mantener una postura erguida pero suave, con los hombros sueltos, reduce la tensión en el cuello, permite relajar las caderas y afloja los músculos de la zona lumbar. Añaden que no se debe caminar nunca con la cabeza gacha, ya que obliga al cuerpo a trabajar mucho más para mantener la alineación y puede provocar fuertes dolores en la columna cervical. Advierten, además, que no hay necesidad de dar grandes zancadas, pues son menos estables y el caminante puede sentirse un poco desequilibrado, más bien se debe intentar mantener los pasos relativamente cerca del torso, que sean cortos y rápidos, lo que ayudará a mantener la columna recta y evitará sobrecargar la espalda o la cadera. Por último, los especialistas aconsejan mantenerse hidratado durante la marcha, beber una pequeña cantidad de agua u otros líquidos a intervalos regulares. En este contexto sugieren evitar las bebidas con cafeína antes del paseo, porque su consumo provoca pérdida de líquidos y da más sed.
19 febrero 2024 | Fuente: Prensa Latina| Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A

