oct
2
 Las muestras de sangre de adultos sanos indican una inhibición de la formación de trampas extracelulares de neutrófilos (NET) después de una semana de suplementos diarios de jengibre.
Las muestras de sangre de adultos sanos indican una inhibición de la formación de trampas extracelulares de neutrófilos (NET) después de una semana de suplementos diarios de jengibre.
Metodología
Los investigadores reclutaron a nueve adultos sanos de 18 a 38 años para que recibieran diariamente un suplemento oral de jengibre de 100 mg durante 7 días consecutivos.
Se obtuvieron muestras de sangre al inicio y en los días 7 y 14, con aislamiento de neutrófilos, células mononucleares de sangre periférica y plasma.
Los investigadores midieron la formación de trampas extracelulares de neutrófilos (NETosis) como forma de mostrar el efecto del jengibre sobre la inflamación.
Resultados principales
Las mediciones del adenosín monofosfato cíclico (AMPc) de los neutrófilos fueron significativamente más elevadas tras 7 días de suplementos de jengibre, en comparación con los niveles basales, aunque volvieron a situarse cerca de los basales una semana después de interrumpir el consumo de jengibre.
Los suplementos orales de jengibre redujeron 40 % la actividad de la fosfodiesterasa (PDE) de los neutrófilos respecto al valor inicial, resultados similares a los observados con los inhibidores sintéticos de la fosfodiesterasa 4 (PDE4).
Los resultados se basan en estudios anteriores que demostraron la inhibición de la hiperactividad de los neutrófilos en ratones con síndrome de anticuerpos antifosfolípidos y lupus tras la inyección de un preparado purificado de jengibre.
Los investigadores replicaron los resultados que mostraban los efectos del jengibre oral sobre los neutrófilos en otros ocho adultos sanos que también mostraron una reducción de la formación de trampas extracelulares de neutrófilos y un aumento del adenosín monofosfato cíclico de los neutrófilos tras una semana de suplementos de jengibre.
Limitaciones
Se necesitan más investigaciones en humanos con enfermedades inflamatorias y autoinmunitarias para confirmar los hallazgos y explorar el jengibre como intervención terapéutica complementaria.
Enfoque clínico
Los resultados representan un apoyo biológico al potencial del jengibre para impactar en la función de los neutrófilos en los seres humanos; por lo tanto, «el jengibre puede tener una capacidad real para complementar los programas de tratamiento que ya están actuando», declaró en un comunicado de prensa el autor correspondiente, Dr. Jason Knight, de la University of Michigan, en Ann Arbor, Estados Unidos.
Referencia
Ali RA, Minarchick VC, Zahavi M, Rysenga CE, Sturm KA, Hoy CK, et al. Ginger intake suppresses neutrophil extracellular trap formation in autoimmune mice and healthy humans. JCI Insight[Internet].2023[citado 2 oct 2023];8(18):e172011. doi: 10.1172/jci.insight.172011. PMID: 37737262
2 octubre 2023 |Fuente: Medscape en Español | Tomado de Noticias y Perspectivas
oct
2
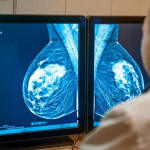 El riesgo a desarrollar cáncer debido a la presencia de mutaciones patogénicas en los genes BRCA es menor cuando no hay antecedentes familiares en primer grado.
El riesgo a desarrollar cáncer debido a la presencia de mutaciones patogénicas en los genes BRCA es menor cuando no hay antecedentes familiares en primer grado.
Las mujeres portadoras de mutaciones patogénicas en los genes BRCA1 o BRCA2 tienen un riesgo elevado a desarrollar cáncer de mama y ovario. No obstante, es importante considerar la existencia de antecedentes familiares en primer grado, para definir con mayor precisión ese riesgo elevado, según indica un reciente estudio publicado en eClinicalMedicine. En él, los autores estiman que en ausencia de antecedentes familiares, el riesgo aumentado es menor de lo que se pensaba.
“Este hallazgo tiene importantes ramificaciones para el cribado de la población mediante secuenciación genómica”, ha señalado Caroline Wright, investigadora en la Universidad de Exeter y una de las autoras del trabajo. “Tenemos que asegurarnos de que estamos llevando a cabo investigaciones para encontrar el verdadero nivel de riesgo, y también ser responsables en la forma en que comunicamos el riesgo, para evitar el miedo y la angustia innecesarios que pueden conducir a procedimientos evitables.”
El impacto de las mutaciones patogénicas en genes BRCA en población general
En el trabajo, los investigadores buscaban determinar la penetrancia de las mutaciones patogénicas en BRCA1 en la población general, es decir, en qué proporción de casos la presencia de la mutación derivaba en un cáncer.
Hasta hace unos años, el análisis genético de estos genes solo se recomendaba en un contexto clínico a mujeres que con cáncer de mama u ovario y/o historia familiar de cáncer. Esta práctica ha resultado en que la mayor parte de las variantes patogénicas detectadas, identificadas en pacientes ya con cáncer de mama, fueran consideradas como de penetrancia alta (alta probabilidad de derivar en un cáncer). Una situación similar ocurre con el síndrome de Lynch, otro síndrome hereditario de predisposición al cáncer.
Los autores pensaron que podía haber un efecto de sobreestimar el carácter patogénico de las variantes por sí mismas. Con la expansión de las pruebas genéticas directas al consumidor, que consideran únicamente la información genética para elaborar los informes, conocer el impacto real de las variantes patogénicas es especialmente relevante, para informar sobre el riesgo a desarrollar cáncer.
Información genética de más de 450 000 personas
Los investigadores utilizaron los datos de análisis de exomas e historiales clínicos de 454 712 personas para estimar la penetrancia de las variantes genéticas conocidas por su papel en el cáncer de mama y ovario, así como en el síndrome de Lynch (otro síndrome de predisposición al cáncer).
Los resultados indican que las mujeres con una variante en genes BRCA e historia familiar con cáncer en familiares de primer grado tienen un mayor riesgo a desarrollar cáncer de mama que aquellas personas que únicamente son portadoras de las variantes. Por ejemplo, el equipo ha estimado que, a los 60 años, ser portadora de una variante de BRCA patogénica está asociada a un riesgo del 18% (en el caso de BRCA2) y del 23% (en el caso de BRCA1) de desarrollar cáncer de mama. Sin embargo, si además, la persona portadora tiene un familiar cercano con la enfermedad, el riesgo se eleva a 24 % y 45 % (para BRCA2 y BRCA1, respectivamente).
Diferencias similares se observan en el caso de personas portadoras de variantes genéticas patogénicas relacionadas con el síndrome de Lynch y el riesgo a desarrollar cáncer colorrectal.
Impacto en la comunicación y reacción a resultados de pruebas genéticas
Los resultados muestran que, a la hora de interpretar resultados genéticos relacionados con el cáncer, el contexto importa. Y que gran parte del riesgo que confieren las variantes patogénicas asociadas a formas hereditarias de cáncer proviene de la historia familiar. A nivel biológico, esto implica que el contexto genómico compartido por el parentesco puede influir en el riesgo a desarrollar cáncer.
De los resultados del análisis de los genes BRCA y otros genes de predisposición al cáncer pueden derivar decisiones tan importantes como la cirugía preventiva. El ejemplo más conocido es el de la actriz Angelina Jolie, que por sus antecedentes familiares y prueba positiva para una variante patogénica decidió someterse a una doble mastectomía como medida preventiva al posible desarrollo de un cáncer de mama.
En este contexto y con el mayor acceso a pruebas genéticas fuera de la consulta clínica, estimar de forma precisa el riesgo genético cobra una importancia especial.
“Que te digan que tienes un alto riesgo genético de padecer una enfermedad puede influir realmente en los niveles de miedo a una afección concreta y en las medidas resultantes que puedas tomar”, destaca Leigh Jackson, investigador de la Universidad de Exeter y primer autor del trabajo. “Un riesgo de hasta el 80% de desarrollar cáncer de mama es muy diferente de un 20%. Esta diferencia puede influir en la decisión de someterse o no a una operación invasiva de mama. Algunas mujeres pueden decidir someterse a esa intervención sabiendo que el riesgo es del 20%, pero queremos que tomen una decisión informada. Instamos a que cualquier persona que comunique el riesgo de cáncer lo haga basándose en un historial familiar detallado, no sólo en la genética”.
Referencia
Jackson L, Weedon MN, Green HD, Mallabar Rimmer B, Harrison JW, Wood AR, et al. Influence of family history on penetrance of hereditary cancers in a population setting. EClinicalMedicine[Internet]. 2023[citado 2 oct 2023]. DOI: https://doi.org/10.1016/j.eclinm.2023.102159
2 octubre 2023 |Fuente: Genotipia| Tomado de Genética Médica
oct
2
 Las hormonas y los metabolitos secretados después de practicar una actividad física actúan como un mecanismo conjunto para suprimir el hambre.
Las hormonas y los metabolitos secretados después de practicar una actividad física actúan como un mecanismo conjunto para suprimir el hambre.
La compleja relación existente entre la actividad física y el equilibrio energético (la ingesta de alimentos versus el gasto calórico) se erige aún como un reto para la ciencia, fundamentalmente frente a los crecientes índices de sobrepeso y obesidad que se registran en el mundo. Algunos medicamentos disponibles en el mercado para el combate contra la obesidad funcionan de manera análoga a las hormonas relacionadas con el control del apetito. En tal sentido, un camino ha venido cobrando relevancia en el área: la comprensión de los procesos ligados a los metabolitos (los productos del metabolismo de las células) en el control del hambre y de la saciedad.
Y es precisamente una posible combinación de mecanismos similares a las funciones hormonales con las de los metabolitos lo que los investigadores Henver Simionato Brunetta, de la Universidad de Campinas (Unicamp), en Brasil, y Jens Lund, de la Universidad de Copenhague, en Dinamarca, señalan como prometedora con la mira puesta en avanzar al respecto de los tratamientos actualmente disponibles. En un editorial publicado en The Journal of Physiology, ambos científicos analizan un estudio aleatorizado dado a conocer en esa misma edición.
En la referida investigación, se analizó la interacción metabólica entre los hidratos de carbono y los ejercicios, y su papel en la regulación aguda del apetito. Encabezado por el profesor James Frampton, del Imperial College de Londres, dicho estudio apuntó dos metabolitos –el acetato y el succinato– como potenciales mediadores del apetito inducido por el ejercicio físico y de las respuestas de la ingestión de energía.
“El punto más interesante de este trabajo −lo que los investigadores observaron− es el que indica que el ejercicio en forma aguda suprime el hambre. Pero solamente el perfil hormonal no es suficiente como para explicar este efecto. Por eso los científicos efectuaron una evaluación de los metabolitos alterados por el ejercicio y por otras condiciones alimentarias, y notaron que algunos de estos, como el acetato y el succinato, actúan como predictores de la saciedad. De alguna manera, los metabolitos están regulando el hambre y la saciedad, aunque todavía no sabemos exactamente cómo lo hacen”, le explica Simionato Brunetta a Agência FAPESP.
En el estudio cruzado aleatorizado, el grupo de Frampton reclutó a 12 participantes de sexo masculino con edades entre los 18 y los 40 años entre los meses de febrero de 2019 y 2020; las mujeres quedaron excluidas a causa de la influencia del ciclo menstrual sobre el apetito. Los participantes realizaron 30 minutos de ejercicios, ya sea en ayunas o tras haber ingerido carbohidratos. Luego de ello, se les ofreció a los participantes un refrigerio que permitió evaluar la ingesta calórica y las sensaciones subjetivas de apetito, aparte de los metabolitos y las hormonas mediante análisis de sangre.
Se descubrió que tanto los hidratos de carbono como los ejercicios elevaron los niveles de GLP-1 (la hormona reductora del hambre) y disminuyeron los de grelina (la hormona que aumenta el hambre). Sin embargo, los metabolitos parecían responder mejor al ejercicio que a la ingestión de hidratos de carbono al producir un conjunto hormonas/metabolitos con potencial para suprimir el apetito, pese al aumento del gasto energético inducido por el ejercicio.
La obesidad está relacionada con la elevación del riesgo de padecer otras enfermedades, tales como las cardíacas, la diabetes y la hipertensión arterial. Para el año 2030 se estima que la misma afectará a 1.000 millones de personas en el mundo, de acuerdo con los datos del Atlas Mundial de la Obesidad de la organización internacional World Obesity Federation. La estimación en Brasil apunta que afectará a alrededor del 30 % de las personas adultas.
Una línea de estudio
Simionato Brunetta lleva adelante actualmente su posdoctorado con el apoyo de la FAPESP (19/21852-1 y 22/00358-1), y forma parte del equipo de Marcelo Mori, docente del Instituto de Biología de la Unicamp. El equipo de Mori fue el primero que demostró –en julio de 2020– que el SARS-CoV-2 poseía la capacidad de infectar a las células de grasa humanas y que sugirió que el tejido adiposo haría las veces de reservorio del virus (lea más en: agencia.fapesp.br/40255).
El científico paulista trabaja desde hace años en investigaciones referentes a la obesidad y al metabolismo. Desde el año 2019, ha venido enfocándose en los factores que secreta el tejido adiposo, tanto hormonas como otras sustancias, entre ellas los metabolitos. “Como el trabajo del equipo de Frampton apuntaba a entender de qué manera controlan el metabolismo las sustancias secretadas, va claramente al encuentro de lo que hago yo. Hoy en día sabemos que los órganos liberan muchas más sustancias que las hormonas. Y estas sustancias son sumamente activas”, añade.
El tejido adiposo, al que inicialmente se consideraba como un reservorio energético, está reconocido ahora como un importante órgano endócrino. Su función de comunicación con otros órganos transcurre mediante la secreción de hormonas denominadas adipocinas y de micro-ARN (mi-ARN). Simionato Brunetta firma también otro artículo científico, aún en versión preprint (sin revisión por pares), en el cual se aborda la adaptación bioenergética adecuada del tejido adiposo marrón.
Referencia
Brunetta HS, Lund J. Chasing the hunger-suppressive signals of human exercise. The Journal of hysiology[Internet].2023[citado 2 oct 2023]; 601( 16): 3439-3686. http://doi.org/10.1113/JP285096open_in_new
2 octubre 2023 |Fuente: Dicyt| Tomado de Ciencias Sociales
oct
2
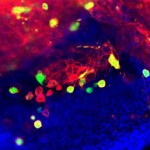 Un estudio del laboratorio de Desarrollo y Control del Crecimiento del IRB Barcelona arroja luz sobre el papel del daño al ADN en la invasividad de las células cancerosas.
Un estudio del laboratorio de Desarrollo y Control del Crecimiento del IRB Barcelona arroja luz sobre el papel del daño al ADN en la invasividad de las células cancerosas.
El descubrimiento desafía la hipótesis comúnmente aceptada de que la maquinaria de muerte celular tiene acción antitumoral.
El trabajo, llevado a cabo en la mosca Drosophila, se ha publicado en la revista Current Biology.
La inestabilidad cromosómica es un fenómeno caracterizado por cambios rápidos en el número y la estructura de los cromosomas durante la división celular. Es muy frecuente en tumores sólidos y está vinculada con la propagación agresiva del cáncer, es decir, con la metástasis. La metástasis es causante del 90% de las muertes relacionadas con el cáncer y por eso es de crucial importancia conocer en detalle este proceso.
Científicos del laboratorio de Desarrollo y Control del Crecimiento del IRB Barcelona, que lidera el investigador ICREA Dr. Marco Milán, han revelado cómo el daño al ADN, provocado por la inestabilidad cromosómica, incrementa la invasividad de las células cancerosas. La investigación detalló cómo la inestabilidad cromosómica activa una vía de señalización conocida como JAK/STAT y promueve la acción de las caspasas, que provocan daño en el ADN. Este daño favorece que las células puedan escapar del tumor primario, dando lugar a la metástasis.
“Durante mucho tiempo hemos considerado a las caspasas como agentes que inducen la muerte celular en respuesta al daño al ADN. Sin embargo, nuestros hallazgos indican que también pueden desempeñar un papel proinvasivo al promover el daño al ADN. Esta investigación amplía nuestro conocimiento de la biología del cáncer, y abre camino a explorar nuevas vías terapéuticas para combatir la metástasis”, explica el Dr. Milán.
La inestabilidad cromosómica en los tumores metastáticos, tres efectos secundarios
La inestabilidad cromosómica, presente en la mayoría de los tumores sólidos, promueve la metástasis del cáncer por tres vías que se dan como efecto secundario de la propia inestabilidad cromosómica. Por una parte, la aneuploidía (o número irregular de cromosomas en una célula, que provoca estrés celular), por otra parte, la formación de micronúcleos (y el proceso inflamatorio que generan) y, por último, el daño en el ADN (causado por rotura de cromosomas).
El laboratorio que lidera el Dr. Milán en el IRB Barcelona lleva años estudiando el papel de la inestabilidad cromosómica en el cáncer y la metástasis. En estudios anteriores, publicados en 2021 y 2018, ya exploraban los efectos de la aneuploidía en este proceso. En este trabajo, describen el tercer eje de acción, la influencia del daño en el ADN en la invasividad de las células cancerosas.
Tres causas para el daño en el ADN
La inestabilidad cromosómica puede inducir daño en el ADN de tres formas diferentes: por un lado, la propia segregación irregular de los cromosomas puede provocar una rotura en la cadena de ADN. En segundo lugar, el desajuste del número de cromosomas provoca un desequilibrio en la maquinaria celular que da lugar a estrés celular en el momento de la replicación del ADN. En tercer lugar, según describen los investigadores en este trabajo, la aneuploidía también activa la vía de señalización, llamada JAK/STAT, que a su vez activa a las caspasas y causa daño en el ADN.
Las caspasas, cuando funcionan adecuadamente, promueven daño en el ADN para que la célula colapse y se desintegre. Sin embargo, los investigadores han detallado ahora cómo niveles más bajos de caspasas promueven un daño en el ADN, que confiere a las células del cáncer de capacidad para hacer metástasis.
Los primeros autores de este trabajo, quienes han llevado a cabo de la mayoría de los experimentos, son las Dras. Lara Barrio, Ana-Elena Gaspar y Mariana Muzzopappa, y el investigador predoctoral Kaustuv Ghosh. Todo el trabajo publicado en este artículo se ha llevado a cabo en el laboratorio de Desarrollo y Control del Crecimiento que lidera el Dr. Milan en el IRB Barcelona.
Este trabajo ha recibido financiación del Ministerio Español de Ciencia e Innovación, los fondos FEDER y el programa Horizon 2020 de la Unión Europea.
Referencia
Barrio L, Gaspar AE, Muzzopappa M, Ghosh K, Romao D, Clemente Ruiz M, et al. Chromosomal Instability-induced Cell Invasion through Caspase-driven DNA Damage. Current Biology [Internet]. 2022[citado 2 oct 2023]. DOI: 10.1016/j.cub.2023.09.004
2 octubre 2023 |Fuente: Genotipia| Tomado de Genética Médica
oct
2
 En el día mundial del corazón se pone de manifiesto que las técnicas de imagen confirman la relación inversa entre la dieta mediterránea y la enfermedad cardiovascular, según especialistas en imagen del corazón de la Sociedad Española de Radiología Médica (SERAM).
En el día mundial del corazón se pone de manifiesto que las técnicas de imagen confirman la relación inversa entre la dieta mediterránea y la enfermedad cardiovascular, según especialistas en imagen del corazón de la Sociedad Española de Radiología Médica (SERAM).
«Desde la publicación de los magníficos resultados del estudio PREDIMED acerca de la relación entre la dieta mediterránea y la enfermedad cardiovascular se han realizado otros estudios con técnicas de imagen que refuerzan esta relación inversa», apunta la Dra. Antonia Arjonilla López, responsable de coordinación institucional de la SERAM y jefa de servicio de Radiología del Hospital Vithas Aravaca.
Estudios ecográficos del grosor intima media de la arteria carótida (IMT) basales y su comparación con aquellos tras la instauración de la dieta mediterránea prueban la mejoría del mismo y permiten asociarlo con un menor riesgo de accidente cerebrovascular e infarto de miocardio.
La tomografía computarizada (TC) y la resonancia magnética (RM) son muy prometedoras en este sentido, en un futuro próximo, porque no solo muestran la ralentización en la progresión de las placas de arteriosclerosis en los pacientes con dieta mediterránea en términos cuantitativos, sino que además permiten determinar de forma cualitativa una mejoría en la composición y vulnerabilidad de las mismas.
Además, «algunos marcadores subclínicos de insuficiencia cardiaca medidos por resonancia magnética como el volumen ventricular izquierdo, la masa del ventrículo izquierdo o la fracción de eyección mejoran tras la adhesión a la dieta mediterránea», señala la Dra. Arjonilla.
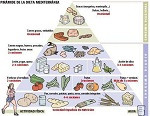
Algunos de los componentes comunes de la dieta mediterránea
Aceite de oliva virgen extra como fuente principal de grasa
Alto consumo de alimentos no procesados como pescado, verduras, frutas, legumbres y cereales integrales
Bajo consumo de carnes rojas
Papel del Radiólogo
«Como especialistas en imagen debemos seguir monitorizando esta relación inversa entre nuestra magnífica dieta mediterránea y los eventos cardiovasculares adversos para que, junto a nuestros compañeros clínicos, logremos mentalizar a la población y a los sistemas de salud de la importancia de priorizar la prevención de la enfermedad cardiovascular que es la enfermedad más prevalente» apunta la Dra. Arjonilla.
Referencia
Estruch R. Qué nos ha enseñado y qué nos queda por aprender del estudio PREDIMED. Av Diabetol[Internet]. 2013[citado 2 oct 2023]; 29(4): 81-87. https://doi.org/10.1016/j.avdiab.2013.05.003
2 octubre 2023 |Fuente: IMMedico | Tomado de Noticias Cardiología
oct
2
 La secuenciación de genomas supera el rendimiento del cariotipo, microarrays cromosómicos y secuenciación de exomas en el diagnóstico del trastorno del espectro autista y las anomalías fetales estructurales, según indica un reciente trabajo publicado en el American Journal o f Human Genetics.
La secuenciación de genomas supera el rendimiento del cariotipo, microarrays cromosómicos y secuenciación de exomas en el diagnóstico del trastorno del espectro autista y las anomalías fetales estructurales, según indica un reciente trabajo publicado en el American Journal o f Human Genetics.
Una de las ventajas de la secuenciación de genomas como herramienta diagnóstica es que permite detectar diferentes tipos de variaciones genéticas en una misma prueba. Hasta hace poco para capturar el rango de posibles variaciones genéticas (reorganizaciones cromosómicas, variaciones en número de copias, pequeñas deleciones o inserciones o cambios en un único nucleótido) eran necesarias varias pruebas complementarias, lo que resultaba menos eficiente y requería más tiempo y recursos.
Recientemente, investigadores del Centro de Medicina Genómica del Hospital General de Massachusetts y otras instituciones han evaluado la utilidad clínica de la secuenciación de genomas en un contexto muy concreto: los trastornos del espectro autista y las anomalías estructurales fetales.
Los investigadores han comparado el rendimiento de la secuenciación de exomas respecto a las diferentes estrategias estándar (cariotipo, microarray cromosómico y análisis de exomas) para detectar alteraciones cromosómicas, cambios en el número de copias y otras variaciones genéticas.
Los resultados apoyan a la secuenciación genómica como técnica de primera línea para el diagnóstico de trastornos del espectro autista y anomalías estructurales. La secuenciación de genomas supera al cariotipo, el array cromosómico y la secuenciación de exomas como prueba diagnóstica individual para la evaluación de anomalías estructurales fetales. Además, también mejora la combinación de las tres pruebas diagnósticas.
Rendimiento en trastorno del espectro autista
En primer lugar, el equipo analizó el genoma de 1 612 cuartetos familiares que incluían una persona con trastorno del espectro autista, y para los que ya se disponía de información de cariotipo, microarray cromosómico y análisis de exomas.
En este caso la secuenciación genómica detectó una variante diagnóstica en un 7.8% de los casos de trastorno de espectro autista. El rendimiento de la técnica superó notablemente al del cariotipo, microarray cromosómico y análisis de exomas. Además, permitió identificar algunas variantes que ninguna de las otras aproximaciones pudo detectar.
No obstante, los autores precisan que al enfocar el análisis de exomas hacia la identificación sistemática de variantes en el número de copias, el rendimiento diagnóstico se acercó mucho al del análisis de genomas.
Rendimiento en anomalías estructurales fetales
A continuación, el equipo estudió 249 casos en los que se habían detectado anomalías estructurales en el feto y se disponía de información de cariotipo, microarrays cromosómicos y análisis de exomas.
Los investigadores analizaron el genoma de 249 tríos formados por el feto con anomalías estructurales y los dos progenitores no afectados y detectaron alteraciones diagnósticas en un 46.1 % de los casos. Este valor supone un aumento significativo respecto a cada una de las otras pruebas: un aumento del 17.2 % respecto al cariotipo, un 14.1 % respecto al análisis de microarrays cromosómicos y un 36.1% respecto al análisis de exomas (si solo se consideran cambios de un nucleótido o inserciones y deleciones pequeñas). En conjunto, el aumento es más modesto, aunque ofrece la ventaja de realizar una única prueba.
Una prueba de primera línea
En conjunto, los resultados del trabajo sugieren que la secuenciación de genomas puede desplazar eficazmente a las técnicas estándar actuales que evalúan de forma separada las diferentes variantes genéticas, para la evaluación de anomalías estructurales fetales. Además, también ofrece una mejora moderada de rendimiento cuando se compara con las tres pruebas diagnósticas combinadas.
Una cuestión paralela a tener en cuenta es la implementación de la secuenciación de genomas como prueba rutinaria en el entorno clínico, junto a las posibles barreras técnicas, logísticas o económicas asociadas.
Referencia
Lowther C, Valkanas E, Giordano JL, Wang HZ, Curral BB, Ó Keefe K, et al. Systematic evaluation of genome sequencing for the diagnostic assessment of autism spectrum disorder and fetal structural anomalies. Am J Hum Genet[Internet]. 2023[citado 2 oct 2023];110(9):1454-1469. doi: http://dx.doi.org/10.1016/j.ajhg.2023.07.010
2 octubre 2023 |Fuente: Genotipia| Tomado de Genética Médica

