nov
12
 Una investigación realizada por la Universidad Europea de España, profundiza hoy acerca de las arritmias cardíacas y la influencia del estrés, cafeína, alcohol o falta de sueño.
Una investigación realizada por la Universidad Europea de España, profundiza hoy acerca de las arritmias cardíacas y la influencia del estrés, cafeína, alcohol o falta de sueño.
Francisco José Martín, médico especialista en cardiología deportiva del centro I-Shape de la Universidad Europea, aseguró que “detectarlas a tiempo evita complicaciones como ictus, insuficiencia cardíaca o muerte súbita”.
Detalló que también la fiebre o ciertos fármacos pueden influir en la aparición de arritmias y, aunque no todas son graves, tampoco deben ignorarse.
“Detectar a tiempo las arritmias permite intervenir antes de que aparezcan complicaciones serias. Aunque muchas son benignas, su manejo es clave porque ciertas arritmias se asocian a eventos cardiovasculares y a un mayor riesgo de insuficiencia cardíaca”, señaló.
De acuerdo con la institución docente, que tiene sedes en Islas Canarias, Andalucía, Valencia y Madrid, en 2024, la insuficiencia cardíaca causó 18 574 fallecimientos en España.
El doctor Martín opinó que, a partir de ciertas sintomatologías, conviene estar atentos a cómo se siente la persona en su día a día. Palpitaciones que molestan, sensación de vacío en el pecho, falta de aire, mareos o desmayos son motivos para pedir valoración a tu médico.
A veces la arritmia pasa desapercibida y se descubre en un electrocardiograma de rutina o en una revisión deportiva. “En personas activas notar una frecuencia inusualmente alta o irregular durante el ejercicio merece estudio. Importa el tipo de arritmia y también comprobar que el corazón esté estructuralmente sano”, precisó el experto.
En las valoraciones del estudio, aparecen elementos como causas que pueden ser estructurales (cambios en el propio músculo) o eléctricas (errores en el envío de la señal del latido) y también influyen hábitos y factores externos.
Además, cicatrices o dilataciones del corazón, trastornos eléctricos genéticos, exceso de cafeína o alcohol, estrés, falta de sueño, fiebre, desequilibrios de sales o ciertos fármacos están entre los posibles desencadenantes.
“En jóvenes y deportistas las extrasístoles aisladas son frecuentes y suelen ser benignas, pero siempre deben valorarse en contexto clínico”, apuntó el doctor Martín.
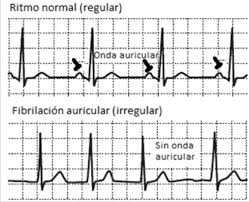
Al abundar acerca del tema, apuntó que la fibrilación auricular desordena la contracción de las aurículas del corazón y esto favorece la aparición de coágulos, por eso aumenta el riesgo de ictus.
La insuficiencia cardíaca aparece cuando el corazón pierde fuerza para bombear y se acompaña de cansancio y falta de aire. “Cuanto antes se diagnostica. antes se actúa con cambios de estilo de vida, fármacos, ablación o dispositivos como marcapasos o desfibriladores cuando están indicados”, recalcó Martín.
“El corazón tiene memoria. Lo que repetimos cada día con ejercicio, alimentación y sueño construye su salud futura”, concluyó el especialista de la Universidad Europea.
06 noviembre 2025 | Fuente: Prensa Latina | Tomado de | Noticia
sep
4
 Investigadores norteamericanos han diseñado el primer modelo de IA individualizado conocido enfocado a la toma de decisiones clínicas en pacientes con fibrilación auricular. La nueva herramienta podría revolucionar el enfoque clínico para tratar esta patología y minimizar los accidentes cerebrovasculares y las hemorragias.
Investigadores norteamericanos han diseñado el primer modelo de IA individualizado conocido enfocado a la toma de decisiones clínicas en pacientes con fibrilación auricular. La nueva herramienta podría revolucionar el enfoque clínico para tratar esta patología y minimizar los accidentes cerebrovasculares y las hemorragias.
La fibrilación auricular (FA) es la arritmia cardíaca más común y afecta a aproximadamente 59 millones de personas en todo el mundo. Durante la FA, las cavidades superiores del corazón se contraen, lo que permite que la sangre se estanque y forme coágulos. Estos coágulos pueden desprenderse y llegar al cerebro, causando un accidente cerebrovascular.
Al respecto, investigadores del Hospital Mount Sinaí de Nueva York (EE.UU.) han logrado desarrollar un modelo de inteligencia artificial para realizar recomendaciones de tratamiento individualizadas para pacientes con fibrilación auricular. Los expertos han conseguido así dar un enfoque completamente nuevo para la toma de decisiones clínicas en este tipo de pacientes.
Se trata de un enfoque para la toma de decisiones clínicas individualizado en comparación con la práctica actual, donde los profesionales clínicos utilizan puntuaciones o herramientas de riesgo que proporcionan estimaciones del riesgo promedio para la población de pacientes estudiada, no para cada paciente individualmente
En concreto, dicho modelo de IA utiliza la historia clínica electrónica completa del paciente para recomendar un tratamiento individualizado. Sopesa el riesgo de sufrir un ictus frente al riesgo de hemorragia grave (ya sea de forma natural o como resultado del tratamiento con anticoagulantes). A partir de ahí, proporciona una estimación del riesgo a nivel de paciente, que posteriormente utiliza para realizar una recomendación individualizada, considerando los beneficios y riesgos del tratamiento para el paciente.
Para el desarrollo de esta herramienta, se entrenó el modelo de IA con los historiales médicos electrónicos de 1,8 millones de pacientes, que abarcaron 21 millones de visitas médicas, 82 millones de notas y 1200 millones de datos. Para validar el modelo, los investigadores probaron su rendimiento en 38.642 pacientes con fibrilación auricular del Sistema de Salud Mount Sinai. También lo validaron externamente con 12.817 pacientes a partir de conjuntos de datos públicos de Stanford.
El modelo fue capaz de generar recomendaciones de tratamiento alineadas con la mitigación del ictus y la hemorragia. «Este estudio representa una profunda modernización en la gestión de la anticoagulación en pacientes con fibrilación auricular y podría cambiar el paradigma de la toma de decisiones clínicas», explicó, al respecto, el Dr. Joshua Lampert, autor correspondiente y director de Aprendizaje Automático del Hospital Cardíaco Mount Sinai Fuster.
La novedosa herramienta, según sus autores, no solo puede calcular las recomendaciones iniciales, sino también actualizarlas dinámicamente con base en el historial clínico electrónico completo del paciente antes de una cita.
Asimismo, destacan que estas recomendaciones pueden descomponerse en probabilidades de ictus y hemorragia grave, lo que libera al profesional clínico de la carga cognitiva de sopesar los riesgos de ictus y hemorragia no específicos de cada paciente, evita la necesidad de mano de obra humana para la recopilación de datos adicionales y proporciona perfiles de riesgo discretos y relacionables para facilitar el asesoramiento a los pacientes.
3 septiembre 2025 | Fuente: IM Médico | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2025. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
jul
24
 El síndrome del corazón en vacaciones es un tipo de arritmia relacionada con el consumo excesivo de alcohol en poco tiempo. Un estudio en ratones indica que puede estar relacionado con un pico de una proteína del estrés que hay en el corazón.
El síndrome del corazón en vacaciones es un tipo de arritmia relacionada con el consumo excesivo de alcohol en poco tiempo. Un estudio en ratones indica que puede estar relacionado con un pico de una proteína del estrés que hay en el corazón.
Un equipo de la Universidad Estatal de Ohio (EE.UU.) estudió ese síndrome y probó en ratones una molécula protectora del corazón para reducir el pico de la proteína del estrés y los ritmos cardíacos irregulares resultantes.
Los resultados del estudio son provisionales, pues aún no han sido revisados, pero se han presentado en las Sesiones Científicas de Ciencias Cardiovasculares Básicas 2024 de la Asociación Americana del Corazón, que se celebran en Chicago (EE.UU.).
El síndrome del corazón en vacaciones es una arritmia, de las que la fibrilación auricular (FibA) es la más común, relacionada con el consumo excesivo de alcohol (cinco copas en dos horas para los hombres y cuatro copas en dos horas para las mujeres, dice la investigación), en solo un día o en periodos largos de vacaciones, como el verano.
Este tipo de borracheras pueden llevar al hospital a personas que nunca han padecido cardiopatías porque su corazón está acelerado o late de forma anómala, explicó el primer autor del estudio Saugat Khanal.
Investigaciones previas en animales descubrieron que las arritmias relacionadas con el consumo excesivo de alcohol están provocadas por elevaciones de una proteína inducida por el estrés llamada JNK2.
Esto puede hacer que las células cardíacas gestionen mal el calcio con lo que el corazón late demasiado deprisa o de forma irregular.
El nuevo estudio sugiere que la molécula Alda-1, un agente protector cardíaco en fase de investigación, puede prevenir la activación de JNK2 que conduce a la fibrilación auricular.
En el estudio , más del 70 % de los ratones a los que se administró alcohol imitando el consumo excesivo desarrollaron fibrilación auricular, frente a ninguno de los que también recibieron Alda-1.
Tanto la actividad de la enzima JNK2 como la gestión del calcio se mantuvieron normales en las células cardíacas de los ratones tratados con Alda-1.
Los hallazgos sugieren que el desarrollo de nuevos fármacos, entre ellos Alda-1 y otros inhibidores específicos de JNK2, puede ser una estrategia anti-AFib eficaz para las personas con síndrome del corazón en vacaciones, afirmó Khanal.
El siguiente paso será estudios con animales más grandes para traducir estos hallazgos en aplicaciones clínicas, dijo el investigador.
Un segundo estudio analizó, también en ratones, por qué el alcohol puede afectar negativamente a la función cardíaca de las mujeres que toman terapia de sustitución de estrógenos.
En ratas que carecían de producción de estrógenos para simular la menopausia humana, la exposición al alcohol provocó cambios negativos en la función cardíaca de los animales que recibieron sustitución de estrógenos.
La hormona estrógeno contribuye a mantener los vasos sanguíneos abiertos y flexibles y, en general, se cree que ayuda a proteger a las mujeres de las enfermedades cardíacas.
En un estudio de ocho semanas, se extirparon a las ratas los ovarios para simular la menopausia, cuando los ovarios prácticamente no producen estrógenos.
Los investigadores compararon las ratas menopáusicas que recibieron una exposición regular al alcohol (suministrado como etanol al 5 % en una dieta líquida) con las que recibieron alcohol y sustitución de estrógenos.
El estudio descubrió que las ratas menopáusicas tratadas con reemplazo de estrógenos más alcohol tenían cambios tanto positivos (menor aumento de peso y masa grasa) como negativos (aumento de la presión arterial y la frecuencia cardíaca).
El equipo consideró sorprendente ver el impacto significativo que tuvieron los estrógenos en la disfunción cardíaca inducida por el alcohol, a pesar de sus conocidos efectos cardioprotectores.
22 julio 2024|Fuente: EFE |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
ene
6
 Un estudio muestra por primera vez el sustrato anatómico de las arritmias que ocurren en quienes padecen esta enfermedad. El virus de la fiebre amarilla afecta especialmente al hígado, pero otros órganos también son acometidos. Read more
Un estudio muestra por primera vez el sustrato anatómico de las arritmias que ocurren en quienes padecen esta enfermedad. El virus de la fiebre amarilla afecta especialmente al hígado, pero otros órganos también son acometidos. Read more
dic
6
 Un estudio llevado a cabo por los equipos de Guadalupe Sabio y José Jalife en el Centro Nacional de Investigaciones Cardiovasculares de Madrid (CNIC) ha descubierto una nueva vía de señalización que estaría detrás de la aparición de la fibrilación ventricular, un tipo de arritmia cardiaca. El trabajo, que se acaba de publicar en la revista Nature Cardiovascular Research, ofrece nuevas esperanzas para abordar esta afección potencialmente mortal.
Un estudio llevado a cabo por los equipos de Guadalupe Sabio y José Jalife en el Centro Nacional de Investigaciones Cardiovasculares de Madrid (CNIC) ha descubierto una nueva vía de señalización que estaría detrás de la aparición de la fibrilación ventricular, un tipo de arritmia cardiaca. El trabajo, que se acaba de publicar en la revista Nature Cardiovascular Research, ofrece nuevas esperanzas para abordar esta afección potencialmente mortal.
La fibrilación ventricular es la principal causa inmediata de muerte súbita cardiaca. Aunque el envejecimiento es uno de los factores de riesgo mejor establecidos para el desarrollo de arritmias cardiacas, los mecanismos detrás de esta conexión han sido esquivos, obstaculizando el desarrollo de tratamientos específicos.
El corazón late de manera regular y coordinada para bombear sangre de manera eficiente a través del cuerpo. Para ello tiene que coordinar la contracción de todas sus células y cada latido tiene que seguir un patrón meticulosamente orquestado. Cuando aparece una arritmia, el ritmo cardiaco se altera, se acelera, se vuelve irregular y es potencialmente mortal.
Estudiando modelos animales, los investigadores del CNIC descubrieron la relación existente entre las proteínas quinasas del estrés p38γ y p38δ y el desarrollo de la fibrilación ventricular, independientemente del sexo.
Este descubrimiento abre nuevas puertas para posibles intervenciones terapéuticas para esta patología.
Los investigadores observaron que la activación de p38γ y p38δ aumentaba en los corazones de ratones envejecidos y aquellos con condiciones genéticas o inducidas por fármacos que predisponen a arritmias, lo que sugería que esta vía tenía un papel crítico en el desarrollo de esta afección.
Según Rafael Romero, primer firmante del artículo e investigador del CNIC, “cuando nos dimos cuenta de que la activación de estas p38 era común en distintas situaciones arritmogénicas, supimos que podían tener un papel clave que había que investigar”.
El estudio exhaustivo de esta vía de señalización reveló que, cuando estas proteínas quinasas se activan, alteran las propiedades eléctricas de los cardiomiocitos, propiciando la aparición de arritmias. Esto sucede por la alteración de unos canales iónicos existentes en las células musculares del corazón responsables de coordinar la contracción celular.
Los investigadores encontraron que p38γ y p38δ fosforilan al receptor de rianodina 2 (RyR2) y a la proteína SAP97 perturbando la localización del canal Kv4.3. En última instancia, estos cambios moleculares resultaron en la aparición de actividad ventricular prematura y una mayor susceptibilidad a la fibrilación ventricular.
Estos hallazgos podrían abrir nuevas perspectivas para la prevención de la fibrilación ventricular sostenida y la protección contra esta grave afección cardíaca, ofreciendo una prometedora diana terapéutica para futuras investigaciones.
Ver más información: Romero-Becerra R, Cruz FM, Mora A, Lopez JA, Ponce Balbuena D, Allan A, et al. p38γ/δ activation alters cardiac electrical activity and predisposes to ventricular arrhythmia. Nat Cardiovasc Res [Internet].2023[citado 4 dic 2023];. https://doi.org/10.1038/s44161-023-00368-x
6 diciembre 2023 | Fuente: Genotipia| Tomado de | Genética Médica
ago
7
 El método, desarrollado bajo la dirección de científicos del Centro Nacional de Investigaciones Cardiovasculares (CNIC), integra de forma simultánea y no invasiva información de los cambios mecánicos y eléctricos en la arritmia.
El método, desarrollado bajo la dirección de científicos del Centro Nacional de Investigaciones Cardiovasculares (CNIC), integra de forma simultánea y no invasiva información de los cambios mecánicos y eléctricos en la arritmia.
Con la fibrilación auricular, la sangre puede quedar atrapada en el pequeño apéndice auricular izquierdo y formar un coágulo, como en esta representación 3D.
Diagnosticada en al menos diez millones de personas en Europa (más de 700 000, en España), esta arritmia cardiaca puede conducir a complicaciones como ictus o insuficiencia cardiaca.
La fibrilación produce una serie de cambios en las características eléctricas, mecánicas y estructurales de las aurículas (lo que se conoce como remodelado auricular). Contar con una «foto» lo más precisa posible de esas alteraciones en cada paciente y por tanto, contribuye a un manejo personalizado de la arritmia.
Un nuevo sistema, cuyos detalles se publican en se publican hoy viernes en Nature Communications, conseguiría afinar ese diagnóstico y el pronóstico de la enfermedad.
La técnica ha sido desarrollada por científicos del CNIC) en una colaboración durante diez años con investigadores nacionales e internacionales. El procedimiento efectúa una evaluación de forma simultánea y no invasiva de la actividad eléctrica y mecánica (contráctil) de las aurículas durante fibrilación auricular.
“Era un reto sin resolver”, comenta el investigador principal del estudio, David Filgueiras, jefe del grupo Desarrollo Avanzado sobre Mecanismos y Terapias de las Arritmias del CNIC y cardiólogo del Instituto de Investigación Sanitaria del Hospital Clínico San Carlos (IdISSC). Por un lado, “la tecnología disponible no permitía integrar ambos tipos de información para obtener un marcador que proporcionara una evaluación más completa”; por otro, “durante la fibrilación auricular los movimientos de contracción de las aurículas del corazón son de baja intensidad y su caracterización supone todo un reto tecnológico”.
Unir dos señales
Con este trabajo se demuestra que “es posible integrar la información eléctrica y mecánica de las aurículas de los pacientes en fibrilación auricular y así obtener información pronóstica personalizada con respecto a la evolución clínica de la arritmia”, afirma Filgueiras.
Para ello, en una primera fase trabajaron clínicos, ingenieros y físicos hasta dar con una solución que integrara los datos electromecánicos. Lo consiguieron uniendo la señal de imagen Doppler tisular de las aurículas para evaluar la actividad mecánica, con la señal del electrocardiograma de superficie, para evaluar la actividad eléctrica.
Las dos señales se registran de manera no invasiva durante un estudio de ecocardiografía transtorácica, una sencilla prueba que evalúa la forma y función del corazón y parte de sus estructuras internas.
Distingue la velocidad de progresión
La clasificación de los pacientes con fibrilación auricular se basa en esencia en criterios que atañen al tiempo que el paciente ha estado con la arritmia. Sin embargo, explica David Filgueiras, “esta clasificación temporal no permite determinar el grado de remodelado subyacente de un paciente en concreto, lo cual tiene especial importancia en los primeros meses de evolución de la fibrilación auricular cuando el grado de avance de los procesos patológicos subyacentes puede seguir distintas velocidades de progresión”.
Para Filgueiras, “la relevancia de este nuevo abordaje diagnóstico se pone de manifiesto en su capacidad para hacer una evaluación personalizada del grado de avance del remodelado auricular en un paciente en concreto, más allá de la clasificación clínica basada en un criterio temporal”.
Las estatinas reducen el riesgo de ACV en pacientes con fibrilación auricular
La irregularidad de los ciclos menstruales aumenta el riesgo de fibrilación auricular
El cribado de la fibrilación auricular en población anciana podría reducir los ictus Read more

