ene
16
 Durante un turno reciente, nuestro equipo de urgencias vio a un paciente con cetoacidosis diabética bastante grave; su nivel de bicarbonato sérico era de 6 mEq/l y el pH en sangre venosa era de 6,85. Durante las conversaciones con el equipo de cuidados intensivos que lo ingresó, debatimos si debíamos administrar bicarbonato de sodio por vía intravenosa. Optamos por no administrarlo, aunque en cuidados intensivos se inició una infusión de bicarbonato poco después de asumir los cuidados. El paciente acabó recuperándose, pero no estaba claro si el bicarbonato de sodio había cambiado algo. Read more
Durante un turno reciente, nuestro equipo de urgencias vio a un paciente con cetoacidosis diabética bastante grave; su nivel de bicarbonato sérico era de 6 mEq/l y el pH en sangre venosa era de 6,85. Durante las conversaciones con el equipo de cuidados intensivos que lo ingresó, debatimos si debíamos administrar bicarbonato de sodio por vía intravenosa. Optamos por no administrarlo, aunque en cuidados intensivos se inició una infusión de bicarbonato poco después de asumir los cuidados. El paciente acabó recuperándose, pero no estaba claro si el bicarbonato de sodio había cambiado algo. Read more
ene
16
 La XLII Lección Memorial de la Fundación Fernández-Cruz ha abordado, un año más, una de las claves que afectan al envejecimiento. En esta edición el foco se ha puesto en cómo la enfermedad cardiovascular es el principal desafío de una población sana y para ello ha contado con la participación de relevantes expertos en la materia. “Vivimos el mejor momento de desarrollo tecnológico. Somos capaces de hacer algo singular y tratar enfermedades que presentan trastornos de síntesis de proteínas, entre otras. Todo eso abre oportunidades”, ha destacado el presidente de la Fundación, el profesor Arturo Fernández-Cruz. Read more
La XLII Lección Memorial de la Fundación Fernández-Cruz ha abordado, un año más, una de las claves que afectan al envejecimiento. En esta edición el foco se ha puesto en cómo la enfermedad cardiovascular es el principal desafío de una población sana y para ello ha contado con la participación de relevantes expertos en la materia. “Vivimos el mejor momento de desarrollo tecnológico. Somos capaces de hacer algo singular y tratar enfermedades que presentan trastornos de síntesis de proteínas, entre otras. Todo eso abre oportunidades”, ha destacado el presidente de la Fundación, el profesor Arturo Fernández-Cruz. Read more
ene
16
 La fuerte disminución de las hospitalizaciones por afecciones cardiovasculares agudas durante los primeros meses de la pandemia de COVID-19 llevó a los médicos de todo el país a preguntarse: «¿Adónde se han ido todos los ataques cardíacos y accidentes cerebrovasculares?» A muchos les preocupaba que la disminución repentina y precipitada se debiera a efectos indirectos negativos de la pandemia, como que los pacientes evitaran la atención de emergencia. Otros especularon que estos patrones reflejaban un cambio real en la incidencia de eventos cardiovasculares agudos. Comprender los factores que impulsaron la disminución de las hospitalizaciones cardiovasculares (y si este tipo de hospitalizaciones se recuperaron a medida que avanzaba la pandemia) tiene implicaciones críticas para la salud pública a medida que Estados Unidos sale de la pandemia. Read more
La fuerte disminución de las hospitalizaciones por afecciones cardiovasculares agudas durante los primeros meses de la pandemia de COVID-19 llevó a los médicos de todo el país a preguntarse: «¿Adónde se han ido todos los ataques cardíacos y accidentes cerebrovasculares?» A muchos les preocupaba que la disminución repentina y precipitada se debiera a efectos indirectos negativos de la pandemia, como que los pacientes evitaran la atención de emergencia. Otros especularon que estos patrones reflejaban un cambio real en la incidencia de eventos cardiovasculares agudos. Comprender los factores que impulsaron la disminución de las hospitalizaciones cardiovasculares (y si este tipo de hospitalizaciones se recuperaron a medida que avanzaba la pandemia) tiene implicaciones críticas para la salud pública a medida que Estados Unidos sale de la pandemia. Read more
ene
16
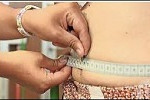 Un IMC alto en adolescentes aumenta el riesgo de enfermedad renal crónica temprana, según un estudio JAMA realizado por investigadores de la Universidad Hebrea. Read more
Un IMC alto en adolescentes aumenta el riesgo de enfermedad renal crónica temprana, según un estudio JAMA realizado por investigadores de la Universidad Hebrea. Read more
ene
16
 La investigación, realizada en ratones, muestra cómo estas diminutas nanomáquinas se impulsan con urea presente en la orina y se dirigen específicamente al tumor, atacándolo con un radioisótopo que transportan en su superficie.
La investigación, realizada en ratones, muestra cómo estas diminutas nanomáquinas se impulsan con urea presente en la orina y se dirigen específicamente al tumor, atacándolo con un radioisótopo que transportan en su superficie.
El cáncer de vejiga tiene una de las tasas de incidencia más elevadas del mundo, siendo además el cuarto tumor más frecuente en hombres. A pesar de no tener una elevada mortalidad, casi la mitad de los tumores de vejiga vuelven a aparecer al cabo de 5 años, de manera que se requiere una vigilancia continuada del paciente, con frecuentes visitas al hospital y la necesidad de repetir el tratamiento. Por todo ello, el cáncer de vejiga es uno de los más costosos de curar.
Los tratamientos actuales que implican la administración de fármacos directamente al interior de la vejiga han demostrado buenas tasas de supervivencia, pero una eficacia terapéutica baja. Una alternativa prometedora es el uso de nanopartículas, capaces de hacer llegar el agente terapéutico directamente al tumor. En especial, destacan los nanorrobots, nanopartículas con capacidad de autopropulsarse por el interior del cuerpo.
Ahora, un estudio publicado en la prestigiosa revista Nature Nanotechnology muestra cómo un equipo de investigación ha sido capaz de reducir en un 90% el tamaño de tumores de vejiga en ratones administrando una sola dosis de nanorrobots propulsados por urea.
El trabajo, liderado por el Instituto de Bioingeniería de Cataluña (IBEC) y el CIC biomaGUNE y desarrollado con la colaboración del Instituto de Investigación Biomédica (IRB Barcelona) y de la Universitat Autònoma de Barcelona (UAB), abre la puerta a nuevos tratamientos para el cáncer de vejiga, que reduzcan el tiempo de hospitalización, lo que implicaría un menor coste y una mayor comodidad para el paciente.
“El innovador sistema óptico que hemos desarrollado, nos permitió, anular la luz que reflejaba el propio tumor y así identificar y localizar las nanopartículas en todo el órgano, sin un marcaje previo, a una resolución sin precedentes. Así vimos que los nanorrobots no solo alcanzaban el tumor, sino que lograban acceder a su interior, para favorecer así la actuación del radiofármaco “, explica Julien Colombelli, líder de la plataforma científica de Microscopía Digital Avanzada del IRB Barcelona.
Descifrar por qué los nanorrobots son capaces de acceder al interior del tumor fue un desafío. Los nanorrobots no contienen anticuerpos específicos para reconocer el tumor, y normalmente, el tejido tumoral es más rígido que el tejido sano.
«Sin embargo, observamos que estos nanorrobots tienen la capacidad de descomponer la matriz extracelular del tumor al aumentar localmente el pH mediante una reacción química de autopropulsión. Este fenómeno podría favorecer una mayor penetración tumoral y resultó ser beneficioso para lograr una acumulación preferencial en el tumor”, detalla Meritxell Serra Casablancas, co-primera autora del estudio e investigadora del IBEC.
Así, los científicos llegaron a la conclusión de que los nanorrobots chocan con el urotelio como si fuera una pared, pero en el tumor, al ser más esponjoso, penetran y se acumulan en su interior. Un factor clave es la movilidad de los nanobots, que aumenta la probabilidad de que lleguen al tumor.
Además, según declara Jordi Llop, investigador del CIC biomaGUNE y colíder del estudio “La administración localizada de los nanorrobots que portan el radioisótopo disminuye la probabilidad de generar efectos adversos, y la elevada acumulación en el tejido tumoral favorece el efecto radioterapéutico”.
“Los resultados de este estudio abren la puerta a la utilización de otros radioisótopos con mayor capacidad de inducir efecto terapéutico, pero cuyo uso se ve restringido cuando los radiofármacos deben administrarse de forma sistémica”, añade Cristina Simó, co-primera autora del estudio.
La tecnología en la cual se basan estos nanorrobots, en los que Samuel Sánchez y su equipo llevan trabajando más de siete años, ha sido patentada recientemente y es la base de Nanobots Therapeutics, spin-off del IBEC e ICREA creada en enero de 2023.
Innovación tecnológica en microscopía para localizar los nanorrobots
El trabajo con nanorrobots ha supuesto un importante desafío científico en técnicas de bioimagen para la visualización de estos elementos en los tejidos y el propio tumor. Las técnicas no invasivas más habituales utilizadas en el ámbito clínico -como PET- no tienen la resolución necesaria para ubicar a nivel microscópico estas partículas de tamaño muy reducido. Por ello, la Plataforma Científica de Microscopía del IRB Barcelona, empleó una técnica de microscopía que implica el uso de una lámina de luz láser para iluminar las muestras y permite obtener imágenes tridimensionales por dispersión de la luz al chocar con tejidos y partículas. Al observar que el propio tumor dispersaba parte de la luz, generando interferencias, desarrollaron una nueva técnica basada en luz polarizada que anula toda la dispersión procedente del tejido y las células del propio tumor. Esto permitió visualizar y localizar los nanorrobots sin necesidad de haberlos marcado previamente con técnicas moleculares.
Referencia: Simó C, Serra-Casablancas M, Hortelao AC, Di Carlo V, Guallar Garrido S, Plaza García S, et al. Urease-powered nanobots for radionuclide bladder cancer therapy. Nat Nanotechnol[Internet].2024. https://doi.org/10.1038/s41565-023-01577-y
6 enero 2024│Fuente: EurekAlert

