dic
2
 Uno de cada siete adultos padece hoy una enfermedad renal crónica, considerada como la novena causa principal de muerte en el mundo, según un estudio publicado en la revista The Lancet.
Uno de cada siete adultos padece hoy una enfermedad renal crónica, considerada como la novena causa principal de muerte en el mundo, según un estudio publicado en la revista The Lancet.
La pesquisa mostró que el número de personas que viven con una función renal reducida se ha duplicado desde 1990, pasando de 378 millones a casi 788 millones en la actualidad.
Los expertos afirman que la enfermedad renal crónica se ha convertido silenciosamente en una crisis de salud global y ahora es la novena causa principal de muerte en todo el mundo.
Los investigadores analizaron datos del Estudio de carga global de enfermedades, que rastrea tendencias de salud en 204 países y territorios, y se enfocaron en adultos de 20 años o más, entre 1990 y 2023.
Detallaron que solo en 2023, más de 1.5 millones de muertes estuvieron relacionadas con la enfermedad renal crónica, cifra que representa un aumento del seis por ciento en tres décadas, incluso después de ajustarse por el envejecimiento de la población.
«Nuestro trabajo muestra que la enfermedad renal crónica es común, mortal y está empeorando como un importante problema de salud pública», afirmó el doctor Josef Coresh de NYU Langone.
La enfermedad hace que los riñones pierdan lentamente su capacidad para filtrar desechos, a menudo sin síntomas hasta etapas avanzadas, cuando puede ser necesario diálisis o trasplante, según publicó HealthDay.
También contribuye a aproximadamente el 12% de las muertes relacionadas con el corazón en todo el mundo.
21 noviembre 2025 | Fuente: Prensa Latina | Tomado de | Noticia
ago
10
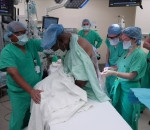 Harry Stackhouse se sometió a sus 74 años a un inusual trasplante de riñón: «Lo vi todo», cuenta después de la cirugía en la que estuvo completamente despierto, no sintió dolor, observó el órgano donado e incluso vio cómo cosían su cuerpo de nuevo.
Harry Stackhouse se sometió a sus 74 años a un inusual trasplante de riñón: «Lo vi todo», cuenta después de la cirugía en la que estuvo completamente despierto, no sintió dolor, observó el órgano donado e incluso vio cómo cosían su cuerpo de nuevo.
Stackhouse recibió el alta apenas 36 horas después del procedimiento en la clínica Northwestern Medicine, que busca realizar este tipo de operaciones sin riesgos subyacentes del uso de la anestesia general.
La cirugía duró poco más de una hora el 15 de julio y es la segunda realizada bajo el liderazgo de Satish Nadig, director del Centro Integral de Trasplantes del sistema hospitalario de Chicago. Desde entonces ya realizó un tercer trasplante.
«Estamos en un punto de inflexión en el campo de los trasplantes, al ser capaces de usar tecnologías que tenemos a nuestro alcance para llevarnos a la siguiente era», dijo Nadig a la AFP.
Puede sonar desagradable o incluso aterrador, pero los beneficios médicos del uso de la anestesia espinal (o raquídea) para trasplantes de riñón -similar a lo que se hace durante las cesáreas- está bien establecido.
La anestesia general requiere de la intubación, que puede dañar las cuerdas vocales, obstruir la función intestinal y causar una pérdida de memoria persistente, en particular en pacientes de edad avanzada.
Aunque la literatura médica menciona casos de trasplantes renales en pacientes despiertos hace varias décadas y en varios países, nunca se ha adoptado ampliamente.
En 2024 se cumplen 70 años del primer trasplante renal exitoso de un donante vivo, observa Nadig. Pero hay una reluctancia a cambiar el «statu quo».
«Sin embargo, los resultados de un trasplante renal (de este tipo) son fantásticos y es hora de que cuestionemos los paradigmas a los que nos hemos aferrado históricamente», agregó.
Recuperar una vida
Stackhouse, un pintor y decorador que tiene seis hijos, cayó enfermo en diciembre de 2019 con síntomas parecidos a los de la gripe, pero fue empeorando hasta que apenas podía caminar.
Unos meses después fue diagnosticado de covid-19 en emergencias, en la fase más peligrosa de la pandemia, y uno de sus riñones estaba fallando y el otro funcionaba solo un 2 %.
Stackhouse se resignó a someterse a sesiones de diálisis tres veces por semana, pero cuando el drenaje comenzó a fallar y sus venas a cerrarse, su hija Trewaunda, de 45 años, lo urgió a considerar un trasplante, ofreciéndose a ser testada para ser la donante.
Inicialmente reluctante a «entrometerse» en la vida de sus hijos, Stackhouse finalmente aceptó someterse al procedimiento después de una consulta con Nadig y de conocer el programa Awake Kidney, que realiza cirugías rápidas sin el uso de anestesia general en los trasplantes de riñón.
«Lo crean o no, no sentí nada, fue increíble», dijo Stackhouse a la AFP.
Es hombre conversó con los médicos durante la operación y cuando el cirujano le ofreció mostrarle el riñón, no dudó: «No imaginé que un riñón es tan grande», exclamó.
Por su edad, Stackhouse recibió el alta 36 horas después de la cirugía. El primer paciente de Nadig en ser sometido a este tipo de trasplante en mayo, salió del hospital después de 24 horas, por debajo del promedio de permanencia de cinco a siete días de hospitalización para casos con sedación.
¿Quién es elegible?
Nadig atribuye los avances a la anestesia selectiva en el abdomen y la columna, que evita el uso de opioides y permite la ingesta de alimentos más rápido, aspectos que ya han ayudado al hospital Northwestern Medicine a disminuir el tiempo promedio de internación incluso antes del programa de trasplantes.
Stackhouse asegura que tuvo una recuperación excelente: ya camina, corta el césped y prepara su barco para un viaje de pesca. Su recuperación fue más rápida que la de su hija Trewaunda, cuyo procedimiento fue con anestesia general.
«Es simplemente un regalo que le puedes dar a alguien, de solo pensar el espiral hacia el que iba, él no se veía bien», dijo a la AFP esta maestra de preescolar. «Estás devolviendo la vida de alguien».
El director del Centro de Trasplantes de la Universidad de Michigan Health, Christopher Sonnenday, elogió al equipo del Northwestern Medicine por su «importante innovación» en el campo.
«Se ha demostrado que limitar exposición a la anestesia general acelera el proceso de recuperación en todas las disciplinas quirúrgicas, y estoy seguro de que ese beneficio puede realizarse también en el trasplante de riñón», sostuvo a la AFP.
Pero solo la experiencia determinará si esta técnica se puede aplicar más ampliamente, incluyendo si se extenderá a pacientes con enfermedades preexistentes como la obesidad o enfermedades cardíacas.
08 agosto 2024|Fuente: AFP |Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2024. Agencia Informativa Latinoamericana Prensa Latina S.A.|Noticia
mar
23
 Médicos en Boston han trasplantado un riñón de cerdo en un paciente de 62 años, el más reciente experimento en la búsqueda de usar órganos animales en seres humanos. El Hospital General de Massachusetts dijo el jueves que es la primera vez que se trasplanta un riñón de cerdo
Médicos en Boston han trasplantado un riñón de cerdo en un paciente de 62 años, el más reciente experimento en la búsqueda de usar órganos animales en seres humanos. El Hospital General de Massachusetts dijo el jueves que es la primera vez que se trasplanta un riñón de cerdo
genéticamente modificado en una persona con vida. Anteriormente se habían trasplantado riñones de cerdo en donantes con muerte cerebral. Además, dos personas recibieron trasplantes de corazón de cerdo, aunque ambos pacientes murieron a los pocos meses. El nuevo paciente, Richard Slayman, residente de Weymouth, Massachusetts, se está recuperando bien tras la cirugía del sábado y se prevé que reciba el alta en poco tiempo.
El doctor Tatsuo Kawai, el cirujano que llevó a cabo el procedimiento, dijo que el equipo cree que el riñón de cerdo funcionará por al menos dos años. De presentar una falla, Slayman podría volver a las diálisis, dijo el especialista Winfred Williams.
Destacó que a diferencia de los pacientes que recibieron corazones de cerdo y estaban muy enfermos, Slayman ‘de hecho está bastante fuerte’. Slayman tuvo un trasplante de riñón en el hospital en 2018, pero tuvo que volver a hacerse diálisis el año pasado cuando mostró señales de insuficiencia.
Cuando surgieron complicaciones con las diálisis, las cuales requirieron procedimientos frecuentes, los médicos sugirieron colocarle un riñón de cerdo, dijo en un comunicado distribuido por el hospital. ‘Lo consideré no sólo como una manera de ayudarme, sino de generar esperanzas para miles de personas que requieren de un trasplante para sobrevivir’, dijo Slayman, quien trabaja como gerente de sistemas para el Departamento de Transporte de Massachusetts.
La cirugía tomó cuatro horas y había 15 personas en el quirófano, quienes aplaudieron cuando el riñón tomó una coloración rosada y comenzó a producir orina, dijeron los médicos en una conferencia de prensa. ‘Realmente era el riñón más hermoso que hayamos visto’, indicó Kawai.
El doctor Parsia Vagefi, director de cirugía de trasplantes en el Centro Médico UT Southwestern, se refirió al anuncio como ‘un paso importante’. Pero al igual que los médicos de Boston, dijo que se necesitan estudios que involucren a más pacientes de distintos centros médicos antes de que la práctica esté disponible de manera más frecuente.
El experimento marca el paso más reciente en los xenotrasplantes, el término que se utiliza en el intento de curar a pacientes humanos con células, tejidos u órganos de animales.
Durante décadas no funcionó, ya que el sistema inmunológico humano destruía de inmediato el tejido animal. Los intentos más recientes se han realizado con cerdos modificados para que sus órganos se parezcan más a los del ser humano, lo que genera nuevas esperanzas de que algún día sirvan para compensar la escasez de órganos donados. Más de 100.000 personas en Estados Unidos están en lista de espera para un trasplante, en su mayoría enfermos del riñón, y miles mueren cada año antes de que llegue su turno. Los cerdos han sido utilizados desde hace tiempo en la medicina humana, incluidos los injertos de piel y la implantación de válvulas cardiacas. Pero el trasplante de órganos completos es mucho más complejo que utilizar tejido procesado. El riñón que se le implantó a Slayman provino de la compañía eGenesis de Cambridge, Massachusetts. El animal fue modificado genéticamente para retirarle genes porcinos perjudiciales y añadir ciertos genes humanos para mejorar su compatibilidad. El caso de Slayman fue complicado, indicaron los médicos.
Incluso antes de su primer trasplante, el paciente tenía problemas con la diálisis y necesitó de decenas de procedimientos para intentar retirarle coágulos y restaurar el flujo sanguíneo. Se volvió ‘cada vez más desanimado y deprimido por su situación con la diálisis. En cierto punto, literalmente
dijo ‘no puedo seguir así’, comentó su médico, Williams. La Administración de Alimentos y Medicamentos de Estados Unidos otorgó un permiso especial para el procedimiento de Slayman en virtud a las reglas de ‘uso compasivo’.
Nueva York, 22 marzo 2024|Fuente: AP | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2019. Agencia Informativa Latinoamericana Prensa Latina S.A.
abr
22
Investigadores de la Universidad de Pittsburgh han identificado un tipo de célula inmunitaria que provoca el fracaso crónico del trasplante de riñón en un modelo de ratón y han descubierto vías que podrían utilizarse terapéuticamente para mejorar los resultados de los pacientes. Los resultados se publican en un nuevo artículo de Science Immunology.
«En los trasplantes de órganos sólidos, como los renales, los resultados a un año son excelentes porque disponemos de fármacos inmunosupresores que controlan el problema del rechazo agudo», explica el Dr. Fadi Lakkis, coautor principal del estudio, catedrático de Cirugía, profesor de Inmunología y Medicina y director científico del Instituto de Trasplantes Thomas E. Starzl de Pitt y la UPM.
«Pero con el tiempo, estos órganos suelen empezar a fallar debido a una forma más lenta de rechazo denominada rechazo crónico, y los medicamentos actuales no parecen ayudar. Comprender este problema fue la motivación de nuestro estudio»
Anteriormente, Lakkis y sus colegas habían demostrado que un tipo de células inmunitarias llamadas células T de memoria residentes en el tejido impulsan el rechazo crónico. Como todas las células T de memoria, estas versiones residentes «recuerdan» amenazas anteriores al reconocer rasgos identificativos específicos denominados antígenos. Pero a diferencia de la mayoría de las células T de memoria, que circulan por el torrente sanguíneo, las células T de memoria residentes en los tejidos viven en el interior de los órganos.
En el nuevo estudio, el primer autor, el doctor Roger Tieu, estudiante del Programa de Formación de Científicos Médicos de Pitt, descubrió dos factores que mantienen las células T de memoria residentes en los injertos renales a lo largo del tiempo. El primero es el antígeno en sí: las moléculas que las células T utilizan para reconocer el injerto del donante como extraño. Dado que las células T residentes viven dentro del injerto renal, están constantemente expuestas a dichos antígenos. El segundo factor es una citocina, o proteína de señalización inflamatoria, denominada IL-15.
También es clave en este proceso otro tipo de células inmunitarias denominadas células dendríticas, que captan tanto el antígeno como la IL-15 y los presentan a los receptores de las células T de memoria residentes.
«Las células dendríticas son como el director de la orquesta», explica Lakkis. «Son fundamentales para activar muchos tipos de células inmunitarias y coordinar las respuestas inmunitarias».
Cuando los investigadores agotaron las células dendríticas o bloquearon su capacidad de presentar antígeno o IL-15, observaron un descenso en la cantidad y funcionalidad de las células T de memoria residentes.
«El antígeno y la IL-15 son necesarios para el mantenimiento de las células T», afirma el coautor Martin Oberbarnscheidt, doctor y profesor adjunto de cirugía en Pitt. «Si se elimina cualquiera de ellas, el número de células de memoria residentes disminuye. En un paciente trasplantado, no es factible eliminar el antígeno porque se encuentra en todo el órgano del donante, pero dirigirse a la IL-15 es clínicamente traducible.»
De hecho, cuando los investigadores bloquearon la señalización de la IL-15 con un anticuerpo que impedía la unión de la IL-15 a su receptor en las células T, comprobaron que la supervivencia del injerto se prolongaba enormemente en los receptores renales de ratones.
Los investigadores confían en que los hallazgos puedan sentar las bases de ensayos clínicos para probar el anticuerpo en pacientes trasplantados con el fin de minimizar el rechazo crónico. El bloqueo de la señalización de la IL-15 podría permitir una selección más precisa de las células T de memoria residentes en el injerto, minimizando al mismo tiempo la inmunosupresión global de otras células T de todo el organismo que son importantes para la inmunidad frente a las infecciones.
«En mi formación en la Facultad de Medicina, he tenido el privilegio de trabajar con pacientes trasplantados», ha declarado Tieu. «Me entusiasma que nuestro trabajo tenga el potencial de trasladarse del laboratorio a la clínica, con el objetivo de mitigar el rechazo crónico y elevar la calidad de vida de nuestros pacientes».
Abril 22/2023 (MedicalXpress) – Tomado de Diabetes https://medicalxpress.com/news/2023-04-approach-chronic-transplant.html Copyright Medical Xpress 2011 – 2023 powered by Science X Network.
Traducción realizada con la versión gratuita del traductor www.DeepL.com/Translator
ago
26
El Hospital Vall d’Hebron de Barcelona ha realizado con éxito el primer trasplante de riñón en Europa a un paciente considerado inoperable, mediante un novedoso tratamiento que elimina los anticuerpos en sangre de pacientes inmunodeprimidos y evita así que se rechace el trasplante renal. Read more
jun
26
Las personas sometidas a un trasplante simultáneo de hígado y riñón presentan ventajas en el largo plazo en relación a las que se realizan solo uno, pues tienen una menor incidencia de rechazo celular por anticuerpos, revela un estudio. Read more

