mar
24
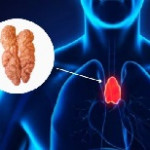 El timo es un órgano pequeño ubicado en el pecho, detrás del esternón. Su función principal es ayudar a desarrollar y educar las células T, esenciales para el sistema inmunológico.
El timo es un órgano pequeño ubicado en el pecho, detrás del esternón. Su función principal es ayudar a desarrollar y educar las células T, esenciales para el sistema inmunológico.
Hasta muy reciente, pocos imaginaban que el timo podía influir tanto en la salud y la longevidad. Científicos de los Estados Unidos, Países Bajos, Alemania, Dinamarca y Reino Unido sugieren que la salud de ese órgano está asociada a vivir más años y a tener menos riesgo de cáncer y enfermedades cardiovasculares.
Las implicaciones van más allá de la prevención: la salud del timo también parece tener un papel en la respuesta a tratamientos innovadores como la inmunoterapia.
La investigación fue publicada en la revista Nature. Fue llevada a cabo por científicos del Programa de Inteligencia Artificial en Medicina de Mass General Brigham y la Escuela de Medicina de Harvard, el Departamento de Oncología Radioterápica del Hospital Brigham and Women y el Instituto Dana-Farber de Cáncer, Estados Unidos.
También colaboraron investigadores de la Universidad de Maastricht, en Países Bajos, la Universidad Goethe de Frankfurt, Alemania, el Hospital Universitario de Aarhus, en Dinamarca, y el Colegio Universitario de Londres y el Instituto Francis Crick, en el Reino Unido.
Contaron con el financiamiento de los Institutos Nacionales de Salud, el Consejo Europeo de Investigación y la Fundación DFG de Alemania.
La importancia del timo después de la infancia
Durante años, el timo se consideró fundamental solo en la niñez porque produce y educa células T, que defienden al cuerpo de infecciones. Después de la pubertad, el timo se encoge y pierde actividad, y por eso se pensaba que su función en adultos era irrelevante.
Pero el nuevo estudio desafió esa idea. Los investigadores quisieron saber si el estado del timo en adultos podría influir en la salud general, la longevidad y la respuesta a terapias avanzadas como la inmunoterapia.
Partieron de la hipótesis de que la diversidad de células T disminuye con la edad y que eso podría estar ligado al deterioro inmunológico.
Hasta ahora, la mayoría de los trabajos en adultos se basaban en análisis de sangre con grupos pequeños, lo que limitaba sus resultados.
Esa investigación analizó a decenas de miles de personas con el objetivo de comprobar si la salud tímica tiene un papel central en la protección frente a enfermedades y en la calidad de vida.
El objetivo central fue diseñar una forma confiable y no invasiva de medir la salud tímica en adultos, usando tomografías computarizadas.
Luego, correlacionaron ese resultado con datos de salud y longevidad en cohortes de gran tamaño.
Cómo se midió la salud tímica
Los investigadores crearon un modelo de inteligencia artificial que analiza imágenes de tomografías y calcula un puntaje de salud tímica.
El sistema examinó el tamaño, la forma y la composición del órgano en más de 25 000 adultos del ensayo nacional de tamizaje de cáncer de pulmón y más de 2.500 del Estudio Framingham del Corazón.
A quienes tenían un puntaje alto se los asoció con cerca del 50% menos riesgo de muerte, 63% menos riesgo de morir por enfermedades cardiovasculares y 36% menos riesgo de desarrollar cáncer de pulmón respecto de quienes tenían un puntaje bajo.
“Estas asociaciones se mantuvieron significativas luego de ajustar por edad y otros factores de salud”, detallaron los investigadores.
El análisis mostró que la inflamación crónica, el tabaquismo y el exceso de peso se relacionan con una peor salud tímica.
Los resultados sugieren que el estilo de vida y la inflamación sistémica pueden influir en la capacidad del sistema inmune para enfrentar amenazas durante la vida.
En otra etapa, los investigadores analizaron a más de 1.200 pacientes con cáncer tratados con inmunoterapia. En este grupo, quienes tenían mejor salud tímica presentaron 37% menos riesgo de progresión del cáncer y 44% menos riesgo de morir.
Los resultados sugieren que el timo podría ser un factor no considerado al evaluar la respuesta a la inmunoterapia.
Sugirieron que mejorar la comprensión y el monitoreo de la salud tímica podría ayudar a los médicos a valorar el riesgo de enfermedades y decidir tratamientos.
Perspectivas para la salud tímica
Tras los resultados, los investigadores recomendaron prestar más atención a la salud tímica en adultos y explorar nuevas formas de proteger este órgano.
Aclararon que, aunque ciertos factores de vida se asociaron con la función del timo, no se probó si cambiar hábitos mejora su salud. Por eso, deberían hacerse más investigaciones.
El equipo ya estudia si la exposición involuntaria a radiación en tratamientos de cáncer de pulmón afecta la función tímica.
Consultado por Infobae el médico Ramiro Heredia, especialista en medicina interna del Hospital de Clínicas José de San Martín de la Universidad de Buenos Aires, opinó: “El timo es un órgano fundamental para el sistema inmunológico, especialmente durante la infancia. En esa etapa, los médicos le prestamos una mayor atención. Con el tiempo, suele perder relevancia fisiológica porque, de manera natural, es reemplazado por tejido adiposo y sus funciones las asume el resto del sistema inmune periférico”.
La investigación publicada en Nature «presenta hallazgos que llaman la atención y pueden motivar nuevos estudios. En personas donde la masa tímica se conserva mejor a lo largo de la vida, se observaron resultados positivos, como menor mortalidad cardiovascular, menor incidencia de cáncer, menor mortalidad general y mayor respuesta a tratamientos como la inmunoterapia para cánceres avanzados», señaló.
“Este tipo de estudios, al ser observacionales, no permiten establecer relaciones de causalidad, pero sí abren la puerta a futuras investigaciones sobre el tema. Todo esto resulta prometedor para comprender mejor el papel del timo en la salud adulta”, sostuvo Heredia.
19 marzo 2026 | Fuente: Infobae | Tomado de la Selección Temática sobre Medicina de Prensa Latina. Copyright 2026. Agencia Informativa Latinoamericana Prensa Latina S.A. | Noticia
mar
25
 Al comparar datos referentes a la respuesta inmunitaria resultante de una infección natural causada por el dengue con los de la activación inmunológica generada por las vacunas contra la enfermedad, investigadores de la Universidad de São Paulo (USP), en Brasil, identificaron marcadores moleculares que podrán servir en el futuro para desarrollar nuevas vacunas y tratamientos contra este virus.
Al comparar datos referentes a la respuesta inmunitaria resultante de una infección natural causada por el dengue con los de la activación inmunológica generada por las vacunas contra la enfermedad, investigadores de la Universidad de São Paulo (USP), en Brasil, identificaron marcadores moleculares que podrán servir en el futuro para desarrollar nuevas vacunas y tratamientos contra este virus.
Este trabajo también reiteró la eficacia de la respuesta inmune inducida por dos inmunógenos disponibles en el mercado: Q-Denga, desarrollado por el laboratorio japonés Takeda Pharma y actualmente distribuido por el Sistema Único de Salud de Brasil (el SUS, la red nacional de salud pública del país), y Dengvaxia, del laboratorio francés Sanofi-Pasteur. En ambos se aplica la tecnología de virus atenuado.
Este estudio, publicado en la revista Frontiers in Immunology, es el primero en el cual se identifican firmas inmunológicas del dengue mediante la aplicación de un abordaje denominado vacunología sistémica, un campo de investigación que apunta a descifrar un cuadro global de las respuestas inmunológicas a la vacunación.
Efectuamos un abordaje sistémico e identificamos diversas similitudes entre la respuesta inducida por la vacuna y la de una infección natural provocada por el virus. Por supuesto que, en el caso de los inmunógenos, los mismos promovieron la respuesta inmunitaria sin causar el daño que causa el dengue. En el estudio también logramos caracterizar algunas vías [de señalización entre células de defensa]. Y la vía del interferón [mediada por esta proteína antiviral producida por los leucocitos y por fibroblastos] se mostró central, con diversos genes importantes que surgen como nuevos biomarcadores de la enfermedad”, comenta Otávio Cabral-Marques, docente de la Facultad de Medicina de la USP (FM-USP) y coordinador de la investigación.
En el referido trabajo, los investigadores analizaron 955 muestras de transcriptomas (conjuntos completos de moléculas de ARN expresadas) de pacientes infectados por el mosquito del dengue y de participantes en ensayos clínicos de compuestos inmunizantes contra la enfermedad. Los datos se obtuvieron en bancos públicos. De este modo, se identificaron 237 genes expresados diferentemente tanto en los casos de infección natural como en los de respuesta a las vacunas.
Con base en 20 de esos genes en común, logramos crear un panel para distinguir la gravedad de la enfermedad, particularmente en la fase aguda tardía. Mediante la aplicación de técnicas de aprendizaje automático, también fue posible clasificar diez predictores [firmas inmunológicas] de gravedad de la enfermedad en los casos de infección natural que son cruciales para la respuesta inmunitaria antiviral”, explica Desirée Rodrigues Plaça, autora principal del estudio y becaria doctoral de la FAPESP.
Aparte de ser causada por cuatro serotipos virales (DENV-1, 2, 3 y 4), el dengue lleva la impronta de diferentes fases clínicas. Cuando no es asintomática, la enfermedad exhibe una fase aguda inicial, una fase aguda tardía y una fase convaleciente.
Existen muchas diferencias, pero también logramos identificar muchas similitudes entre la respuesta inmune inducida por las vacunas y aquella que la infección natural provoca. Al tamizar el conjunto de datos, identificamos 20 genes comunes a esos dos procesos, que se expresan de manera análoga. Son los responsables de enriquecer la vía protectora del sistema inmunitario, sobre todo la vía inmunológica del interferón tipo 1 y 2”, dice Rodrigues Plaça.
El interferón es una citoquina cuyo rol principal consiste en inhibir la replicación viral. Como provoca una reacción en cadena que afecta a varias moléculas, el estudio demostró que, si bien las vías antivirales del interferón son responsables de una defensa temprana (actúan en la primera línea), a través de sus complejas funciones biológicas la proteína prepara el terreno para el desarrollo de una inmunidad adaptativa robusta y duradera.
La vía del interferón es sumamente importante en la activación de la respuesta adaptativa. Formada por las células T y B [dos tipos de linfocitos], esta respuesta adaptativa genera la protección permanente [el objetivo de la vacuna]. Por ende, resulta de suma importancia entender qué genes asociados a esta vía serían determinantes para producir una respuesta adaptativa más protectora”, explica Rodrigues Plaça.
Con la información obtenida en el estudio, los investigadores lograron determinar estrategias terapéuticas que pueden bloquear, activar o inducir la actuación de genes implicados en el proceso de la respuesta inmunitaria, lo que abre la posibilidad de investigar nuevos blancos terapéuticos para la enfermedad.
En el trabajo, los científicos identificaron los principales genes
(OAS2, ISG15, AIM2, OAS1, SIGLEC1, IFI6, IFI44L, IFIH1 e IFI44) implicados en el entramado de aspectos importantes de la respuesta inmune adaptativa. De esta forma, mientras que algunos genes (OAS2 y OAS) exhiben funciones antivirales, otros (como ISG15) restringen la replicación del virus.
Los investigadores descubrieron también que en este proceso existe un gen (AIM2) responsable de activar el inflamasoma un complejo proteico existente en el interior de las células de defensa que cuando se activa produce moléculas que le avisan al sistema inmunitario acerca de la necesidad de enviar refuerzos al lugar de la infección, lo que pone en marcha respuestas proinflamatorias cruciales para lograr una defensa antivírica eficaz.
Le compete al gen SIGLEC1 participar en las interacciones de las células inmunitarias facilitando la presentación de antígenos y el reconocimiento inmunológico adaptativo. Inducidos por el interferón, tres genes específicos (IFI6, IFI44L e IFI44) están asociados a la modulación de la apoptosis (la muerte celular programada) y a la defensa antiviral. En tanto, el gen IFIH1 opera como un sensor importante, que modula la respuesta adaptativa a los virus de ARN, tal como es el caso del DENV. Otros genes (IFIT5 y HERC5) exhiben un papel importante en la inhibición de la replicación viral mediada por el interferón.
El conjunto de genes relevantes en todo este proceso remarca cuán intrincada es la ligazón entre las vías antivirales iniciales y los procesos inmunitarios adaptativos subsiguientes. Es como si las dos puntas de una historia se uniesen”, comenta Cabral-Marques.
Ver artículo: Rodriguez Placa D, Fonseca DL, Marquez AH, Zaki Pour S, Nakanishi Usuda J, Crispim Baiocchi G, et al. Immunological signatures unveiled by integrative systems vaccinology characterization of dengue vaccination trials and natural infection. Front Immunol[Internet]. 2024[citado 22 mar 2024]; 15. https://doi.org/10.3389/fimmu.2024.1282754
22 marzo 2024| Fuente: Dicyt| Tomado de | Noticias| Salud
mar
22
 Los virus son las entidades biológicas más abundantes de la Tierra y se encuentran en casi todos los ecosistemas. Se trata de pequeños agentes infecciosos que se multiplican dentro de las células de todo tipo de seres vivos, desde plantas y hongos hasta bacterias, e incluso otros virus. Hasta nosotros, los seres humanos, ofrecemos un ecosistema ideal para su multiplicación.
Los virus son las entidades biológicas más abundantes de la Tierra y se encuentran en casi todos los ecosistemas. Se trata de pequeños agentes infecciosos que se multiplican dentro de las células de todo tipo de seres vivos, desde plantas y hongos hasta bacterias, e incluso otros virus. Hasta nosotros, los seres humanos, ofrecemos un ecosistema ideal para su multiplicación.
No todos los virus provocan enfermedades. Algunos forman parte de nuestra flora microbiológica natural y nos ayudan a realizar distintas funciones, al igual que lo hacen las bacterias que forman parte de nuestro sistema digestivo.
En cuanto a los que nos hacen enfermar, suelen tener un gran impacto, tanto en términos de salud como económicos. Prevenir y controlar las enfermedades que causan es una prioridad para muchos países, sobre todo tras la pandemia de covid-19 ocasionada por el SARS-CoV-2.
Lo que ocurre durante las infecciones virales
Nuestro sistema inmune trata de protegernos de los virus que nos rodean. Cuando enfermamos (infecciones agudas), se dedica a producir anticuerpos y células para combatir la infección. En la mayoría de las ocasiones, nuestro cuerpo logra vencer al virus y nos recuperamos. Este es el caso de las infecciones causadas por el virus de la gripe, el virus SARS-CoV-2 (covid-19) o el rotavirus (causante de gastroenteritis), entre otros.
¿Quiénes somos?
Sin embargo, en algunas ocasiones nuestro sistema inmune no es capaz de eliminar estos virus, que permanecen en nuestro organismo durante largos periodos de tiempo, a menudo años, o incluso durante toda la vida. Hablamos entonces de infecciones crónicas, entre las que podemos destacar a las infecciones por el virus de la hepatitis C o el virus del sida.
En otros casos, los virus pueden esconderse de nuestro sistema inmune y permanecer en un estado inactivo denominado “latencia” dentro de las células o en localizaciones de difícil acceso al sistema inmune como el sistema nervioso central (médula espinal o cerebro). En algunas ocasiones, pueden activarse y causar recidivas, como ocurre en el caso del virus de Epstein-Barr, o enfermedades crónicas, como el virus de la hepatitis B.
Afortunadamente, hoy en día existen tratamientos para combatir algunas de estas infecciones graves, ya sea para eliminar el virus causante de la infección o para controlar su replicación en caso de que no sea posible eliminarlo.
Qué ocurre después de eliminar la infección: huella viral
Hablamos de memoria inmunológica para referirnos a la capacidad que tienen algunas de las células producidas por nuestro sistema inmune de permanecer tras la infección para, en futuras infecciones, responder de manera más rápida. Coloquialmente se conoce como “hacerse inmune”, y es la base de la inmunidad adquirida.
Sin embargo existe un concepto que va aún más lejos: la huella viral. Se trata de una serie de respuestas inmunológicas a largo plazo, incluso años después de que la infección se haya resuelto o el virus haya entrado en estado de latencia, que pueden desequilibrar nuestro sistema inmune, haciéndolo más débil (inmunosupresión) o más reactivo de lo normal.
También se ha observado que los virus pueden acelerar los procesos de envejecimiento del sistema inmune (inmunosenescencia), donde hay una acumulación progresiva de células envejecidas que no son capaces de cumplir correctamente su función inmune.
Estos procesos relacionados con el envejecimiento forman parte de un círculo vicioso que deteriora el funcionamiento del sistema inmunitario. Por un lado, las células senescentes acumuladas liberan moléculas que provocan inflamación, entre otros efectos. Por otro, la inflamación que se produce altera al sistema inmune, contribuyendo a la inmunosenescencia.
La huella viral puede condicionar el riesgo de futuras enfermedades
Todo este impacto en el sistema inmune deja a las personas en situación de vulnerabilidad frente a otras infecciones. Además, y más allá del conocido síndrome de fatiga posviral, aumenta el riesgo de desarrollar distintas enfermedades como las cardiovasculares, diabetes, trastornos neurológicos y desarrollo de tumores, entre otras.
Estas enfermedades se han relacionado con una gran variedad de virus. Por ejemplo, el virus Epstein-Barr, el virus de la hepatitis C o el VIH/SIDA pueden aumentar el riesgo de enfermedades cardiovasculares y diabetes tipo 2. Otros, como el virus de la gripe o el virus Epstein-Barr, se han visto asociados a trastornos neurológicos como la depresión, la esquizofrenia, el alzhéimer y la esclerosis múltiple.
Algunos virus también aumentan el riesgo de desarrollar ciertos tipos de cáncer. Es el caso del virus del sida (asociado a cáncer de hígado, pulmón o linfoma de Hodgkin), los virus de la hepatitis B y C (asociado a carcinoma hepatocelular, linfoma no-Hodgkin o cáncer de cabeza y cuello), el papilomavirus (asociado a carcinoma cervical, esofágico o anal), el virus Epstein-Barr (asociado a carcinoma nasofaríngeo, cáncer de colon y linfoma de Burkitt) o el virus linfotrópico de células T humanas (asociado a varios tipos de leucemias y linfomas).
Para colmo, las infecciones virales pueden dejar huellas de formas más sutiles. Por ejemplo, se ha observado que algunas infecciones virales pueden alterar la microbiota intestinal. Esta microbiota está muy relacionada con el sistema inmunitario, y cambios en ella pueden aumentar el riesgo de enfermedades autoinmunes y alergias a largo plazo.
Actualmente, muchos investigadores estudian cómo los virus dejan huellas duraderas en nuestro cuerpo y su relación con la salud a largo plazo. Invertir en esta línea de investigación resulta crucial para saber cómo las infecciones virales afectan a nuestro sistema inmunitario a corto, medio y largo plazo. Pero también para encontrar nuevos biomarcadores para identificar a las personas que tienen más riesgo de sufrir complicaciones después de una infección. Solo así podremos desarrollar estrategias de prevención y tratamiento eficaces.
19 marzo 2024| Fuente: The conversation| Tomado de| Medicina| Salud
feb
5
 La cefalea es un síntoma frecuente en la fase aguda de la enfermedad por coronavirus 2019 (COVID-19) y también uno de los efectos adversos más comunes tras la vacunación. En ambos casos, la fisiopatología de la cefalea parece estar relacionada con la respuesta inmunitaria del huésped y podría presentar similitudes. Nuestro objetivo fue comparar el fenotipo clínico y la frecuencia de los síntomas asociados y los síntomas de inicio en pacientes con cefalea relacionada con la COVID-19 y cefalea relacionada con la vacuna de la COVID-19.
La cefalea es un síntoma frecuente en la fase aguda de la enfermedad por coronavirus 2019 (COVID-19) y también uno de los efectos adversos más comunes tras la vacunación. En ambos casos, la fisiopatología de la cefalea parece estar relacionada con la respuesta inmunitaria del huésped y podría presentar similitudes. Nuestro objetivo fue comparar el fenotipo clínico y la frecuencia de los síntomas asociados y los síntomas de inicio en pacientes con cefalea relacionada con la COVID-19 y cefalea relacionada con la vacuna de la COVID-19.
realizó un estudio de casos y controles. Se incluyó a pacientes con infección confirmada por COVID-19 y receptores de la vacuna de la COVID-19 que experimentaron un nuevo inicio de cefalea. Se administró un cuestionario estandarizado que incluyó variables demográficas, antecedentes previos de cefaleas, síntomas asociados y variables relacionadas con la cefalea. Ambos grupos se emparejaron por edad, sexo y antecedentes previos de cefaleas. Se realizó un análisis de regresión multivariante.
Un total de 238 pacientes cumplieron con los criterios de elegibilidad (143 pacientes con cefalea relacionada con la COVID-19 y 95 sujetos con cefalea relacionada con la vacuna de la COVID-19). Los pacientes con cefalea relacionada con la COVID-19 presentaron una mayor frecuencia de artralgia, diarrea, disnea, dolor torácico, expectoración, anosmia, mialgia, odinofagia, rinorrea, tos y disgeusia. Además, los pacientes con cefalea relacionada con la COVID-19 experimentaron una duración diaria más prolongada de la cefalea y describieron la cefalea como la peor que habían experimentado. Los pacientes con cefalea relacionada con la vacuna de la COVID-19 experimentaron con más frecuencia dolor en la región parietal, fonofobia y empeoramiento de la cefalea por movimientos de la cabeza o de los ojos.
La cefalea causada por la infección por el SARS-CoV-2 y la cefalea relacionada con la vacunación de la COVID-19 presentan más similitudes que diferencias, lo que respalda una fisiopatología compartida y la activación de la respuesta inmunitaria innata. Las principales diferencias estuvieron relacionadas con los síntomas asociados.
Ver artículo: González-Celestino A, González-Osorio, Y García-Iglesias C, Echavarría-Iñiguez A, Sierra-Mencía A, Recio-García A, et al. Diferencias y similitudes entre la cefalea relacionada con la COVID-19 y la cefalea relacionada con la vacuna de la COVID-19. Un estudio de casos y controles. Rev Neurol [Internet]. 2023[citado 4 feb 2024]; 77:229-39. DOI: https://doi.org/10.33588/rn.7710.2023063
16 noviembre 2023| Fuente: Neurología.com| Tomado de | Noticia
ene
18
 Un estudio observacional realizado por investigadores de la Universidad Pompeu Fabra y del Hospital del Mar determina que la administración intradérmica de la vacuna JYNNEOS contra la viruela induce una respuesta inmunitaria eficiente que debería prote
Un estudio observacional realizado por investigadores de la Universidad Pompeu Fabra y del Hospital del Mar determina que la administración intradérmica de la vacuna JYNNEOS contra la viruela induce una respuesta inmunitaria eficiente que debería prote
Investigadores del Laboratorio de Biología de la Infección del Departamento de Medicina y Ciencias de la Vida (MELIS) de la Universidad Pompeu Fabra y de la Unidad de VIH del Instituto de Investigación Hospital del Mar, han demostrado que la vacunación intradérmica con la vacuna JYNNEOS contra la viruela es la mejor opción para proteger a las personas con VIH de contraer el virus de la viruela del mono. Esta pauta de administración de la vacuna requiere menos material para inyectar a cada paciente, lo que multiplica por 5 las dosis de vacuna disponibles. Los resultados de este estudio observacional también indican que aquellos individuos con un nivel bajo de células T CD4 -un tipo de glóbulo blanco esencial para combatir adecuadamente nuevas infecciones- necesitan una dosis de refuerzo 28 días después de la primera dosis para compensar su estado de inmunodepresión.
El virus de la viruela del mono (monkeypox, en inglés) es un virus zoonótico de la familia del virus variólico que causa la viruela. La viruela del mono causa una enfermedad infecciosa que puede propagarse de forma autóctona entre humanos por contacto directo y por vía respiratoria. Los síntomas más comunes de la infección por viruela símica son fiebre, dolor de cabeza, dolor muscular, inflamación de los ganglios linfáticos, erupción cutánea, síntomas respiratorios y rectales, y agotamiento. Su gravedad depende de la edad y de la respuesta del sistema inmunitario para resistir a patógenos y parásitos.
Antes de la primavera de 2022, la viruela símica solía aparecer como brotes aislados en zonas endémicas de África Central y Occidental, pero en ese momento se produjo un brote mundial que facilitó la transmisión de persona a persona. Transmisión que se produjo, principalmente, entre hombres que mantenían relaciones sexuales con hombres. Un grupo de población con muchos individuos infectados por el VIH y que son especialmente susceptibles a la infección por el virus de la viruela del mono y a su patogenicidad.
Aunque no existe una vacuna específica contra la viruela del mono, la vacuna contra la viruela protege a 8 de cada 10 personas de contraer la infección, debido al parentesco antigénico entre ambos virus.
Combatir la viruela del mono cuando se vive con el VIH
Los resultados del estudio publicado hoy en la revista Journal of Medical Virology indican que la actividad de las células T -responsables de la respuesta contra los patógenos, la homeostasis y la memoria del sistema immune- de los individuos infectados por el VIH-1, cuya carga viral estaba controlada por la terapia antirretroviral, aumentó tras la vacunación con la vacuna contra la viruela JYNNEOS. Y que la respuesta de las células T fue equivalente a la de los individuos sanos de control.
Entre las personas que viven con una infección por VIH, existe un grupo de riesgo que merece especial atención. Se trata de los llamados no respondedores inmunológicos (INR por sus siglas en inglés), individuos que controlan su carga viral con la terapia antirretroviral, pero sólo recuperan parcialmente su recuento de linfocitos T CD4.
«Nuestro estudio muestra que estos INR pueden necesitar una dosis de refuerzo 28 días después de la primera vacunación para generar una respuesta eficiente de células T y estar, así, protegidos frente a la viruela del mono», explica Robert Güerri, clínico del Hospital del Mar y profesor asociado de la UPF, que ha coordinado el estudio de vacunación. En conjunto, los nuevos hallazgos subrayan la importancia de realizar estudios específicos sobre la respuesta inmunitaria en personas con VIH, especialmente en aquellas con un número más bajo de glóbulos blancos CD4.
Las vías de administración de la vacuna modulan la respuesta inmunitaria
Antes del brote de viruela del mono de la primavera de 2022, la vacuna JYNNEOS se administraba por vía subcutánea para proteger a la población. Pero debido al aumento de la demanda de vacunas, en agosto de 2022, las autoridades sanitarias estadounidenses y europeas propusieron administrar la vacuna JYNNEOS por vía intradérmica. Por esta vía, la vacuna se libera en la capa superior de la piel, donde se encuentran muchas células inmunitarias. Aunque, lo más importante de este nuevo procedimiento es que multiplica por 5 las dosis de vacuna disponibles, aumentando la disponibilidad de la vacuna sin comprometer su eficacia.
En contraste con la respuesta de las células T de los individuos infectados por el VIH-1 que recibieron la vacuna JYNNEOS por vía subcutánea, todos los individuos que recibieron la vacuna por vía intradérmica generaron una respuesta significativa de las células T. Por lo tanto, la vacunación intradérmica fue más eficaz para activar la inmunidad antivírica específica.
«Nuestros resultados apoyan claramente la propuesta de una vía de vacunación que ahorre dosis también para la protección de los individuos inmunodeprimidos, que son los que más necesitan la vacuna», añade Andreas Meyerhans, investigador ICREA y catedrático de la UPF, que coordinó la parte experimental del estudio.
Este estudio proporciona una indicación temprana de cómo mejor proceder con la vacunación preventiva contra la viruela del mono en un grupo de individuos con alto riesgo de infección. Sin embargo, otros estudios deberán confirmar y ampliar las observaciones derivadas de este estudio que cuenta con un número pequeño de individuos vacunados.
Referencia: Sisteré-Oró M, Du J, Wortmann DDJ, Filippi MD, Cañas Ruano E, Arrieta Aldea I, et al. Pan-pox-specific T-cell responses in HIV-1-infected individuals after JYNNEOS vaccination. J Med Virol[Internet]. 2023[citado 17 ene 2024]; 96:e29317. doi:10.1002/jmv.29317
12 enero 2024| Fuente: Eureka Alert| Tomado de Comunicado de prensa
nov
23
 La cefalea es un síntoma frecuente en la fase aguda de la enfermedad por coronavirus 2019 (COVID-19) y también uno de los efectos adversos más comunes tras la vacunación. En ambos casos, la fisiopatología de la cefalea parece estar relacionada con la respuesta inmunitaria del huésped y podría presentar similitudes. Ese ha sido el objetivo de un estudio, publicado en Revista de Neurología y desarrollado por un grupo de investigadores españoles y británicos (Hospital Clínico Universitario de Valladolid, Brain Research Imaging Centre (CUBRIC) y Universidad Rey Juan Carlos), comparando el fenotipo clínico y la frecuencia de los síntomas asociados y de inicio en pacientes con cefalea relacionada con la COVID-19 y con la vacuna de la COVID-19.
La cefalea es un síntoma frecuente en la fase aguda de la enfermedad por coronavirus 2019 (COVID-19) y también uno de los efectos adversos más comunes tras la vacunación. En ambos casos, la fisiopatología de la cefalea parece estar relacionada con la respuesta inmunitaria del huésped y podría presentar similitudes. Ese ha sido el objetivo de un estudio, publicado en Revista de Neurología y desarrollado por un grupo de investigadores españoles y británicos (Hospital Clínico Universitario de Valladolid, Brain Research Imaging Centre (CUBRIC) y Universidad Rey Juan Carlos), comparando el fenotipo clínico y la frecuencia de los síntomas asociados y de inicio en pacientes con cefalea relacionada con la COVID-19 y con la vacuna de la COVID-19.
Se realizó un estudio de casos y controles incluyendo pacientes con infección confirmada por COVID-19 y receptores de la vacuna de la COVID-19 que experimentaron un nuevo inicio de cefalea. Se administró un cuestionario estandarizado que incluyó variables demográficas, antecedentes previos de cefaleas, síntomas asociados y variables relacionadas con la cefalea. Ambos grupos se emparejaron por edad, sexo y antecedentes previos de cefaleas y se realizó un análisis de regresión multivariante. El estudio refleja que un total de 238 pacientes cumplieron con los criterios de elegibilidad. Los pacientes con cefalea relacionada con la COVID-19 presentaron una mayor frecuencia de artralgia, diarrea, disnea, dolor torácico, expectoración, anosmia, mialgia, odinofagia, rinorrea, tos y disgeusia. Además, los pacientes con cefalea relacionada con la COVID-19 experimentaron una duración diaria más prolongada de la cefalea y la describieron como la peor que habían experimentado. Los pacientes con cefalea relacionada con la vacuna de la COVID-19 experimentaron con más frecuencia dolor en la región parietal, fonofobia y empeoramiento de la cefalea por movimientos de la cabeza o de los ojos.
Los autores concluyen que la cefalea causada por la infección por el SARS-CoV-2 y la relacionada con la vacunación de la COVID-19 presentan más similitudes que diferencias, lo que respalda una fisiopatología compartida y la activación de la respuesta inmunitaria innata. Las principales diferencias estuvieron relacionadas con los síntomas asociados.
Ver más información:
González Celestino A, González Osorio Y, García Iglesias A, Echavarría Íñiguez A, Sierra Mencía A, Recio García J, et al. Diferencias y similitudes entre la cefalea relacionada con la COVID-19 y la cefalea relacionada con la vacuna de la COVID-19. Un estudio de casos y controles. Rev Neurol [Internet]. 2023[citado 22 nov 2023]; 77:229-239. PMID: 37962534DOI: https://doi.org/10.33588/rn.7710.2023063
23 noviembre 2023 | Fuente: Neurología.com |Tomado de | Noticia Salud

