abr
27
El desarrollo de un nuevo dispositivo que simula una placenta artificial y que incluye una serie de ventajas tecnológicas, podría reducir la morbimortalidad que rodea a los fetos prematuros de entre 22 y 26 semanas de gestación. Los datos del estudio experimental se han publicado en Nature Communications y, según profesionales parecen ofrecer oprotunidades de supervivencia para estos niños con menor mortalidad y morbilidad a largo plazo.
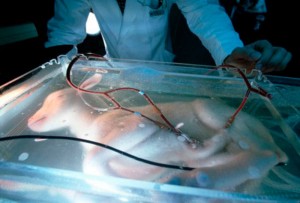 Alan W. Flake, del Departamento de Cirugía Pediátrica y Fetal en la División de Cirugía General Pediátrica, Torácica y Fetal en el Children’s Hospital de Filadelfia (CHOP), en Estados Unidos, ha dirigido una investigación a través de la que se ha desarrollado un sistema de soporte extracorpóreo que simula el ambiente parecido al del útero materno y que ayudaría a los prematuros extremos a conseguir, de una forma fisiológica, la maduración de sus pulmones y de otros órganos.
Alan W. Flake, del Departamento de Cirugía Pediátrica y Fetal en la División de Cirugía General Pediátrica, Torácica y Fetal en el Children’s Hospital de Filadelfia (CHOP), en Estados Unidos, ha dirigido una investigación a través de la que se ha desarrollado un sistema de soporte extracorpóreo que simula el ambiente parecido al del útero materno y que ayudaría a los prematuros extremos a conseguir, de una forma fisiológica, la maduración de sus pulmones y de otros órganos.
Se trata de una especie de placenta artificial que se ha experimentado en animales y que ya se empieza a conocer como Biobag. Actualmente, no se dispone de una tecnología médica de estas características, por lo que su potencial extrapolación a seres humanos, «podría ser muy útil para reducir la morbimortalidad que envuelve a los neonatos muy prematuros», indica Flake, cuyo equipo publica los resultados en Nature Communications.
Desarrollos prenatales normales
El estudio se está realizando con ocho corderos prematuros cuyos 110-120 días de gestación se asemejan al desarrollo pulmonar de los fetos humanos entre la 22 y las 26 semanas de edad gestacional. A esa edad gestacional, el feto pesa menos de 600 gramos y tiene entre un 30 a 50 por ciento de posibilidades de supervivencia, con un alto precio en la calidad de vida, pues suele acompañarse de un 90 por ciento de riesgo de graves morbilidades.
Los primeros datos preclínicos del trabajo con este dispositivo de apoyo extrauterino, que se han obtenido de la monitorización en corderos fetales, ponen de manifiesto que «el desarrollo pulmonar prenatal es muy similar al que ocurre en los seres humanos. El innovador sistema utiliza un único contenedor lleno de fluido unido a las máquinas personalizadas que proporcionan apoyo fisiológico. Los corderos fetales crecen en un ambiente casi estéril controlado por la temperatura, respirando el líquido amniótico como hacen normalmente en el útero y sus corazones bombeando sangre a través de su cordón umbilical en una máquina de intercambio de gas fuera de la bolsa. Los monitores electrónicos miden los signos vitales, el flujo sanguíneo y otras funciones cruciales», indica Flake.
El objetivo del equipo no es extender la viabilidad a un periodo anterior a la marca actual de 23 semanas de gestación, ya que las limitaciones del tamaño físico y el funcionamiento fisiológico impondrían riesgos inaceptablemente altos. Sin embargo, este sistema podría ofrecer beneficios potencialmente muy superiores a lo que los hospitales pueden hacer actualmente para un feto de 23 semanas nacido en el límite de la viabilidad. El Biobag podría convertirse en nuevo estándar de atención para este subconjunto de prematuros extremos. «Existe una necesidad urgente de asistencia ‘puente’ entre el vientre de la madre y el mundo exterior. El objetivo es apoyar a los bebés de 23 semanas a 28 semanas de edad gestacional, ya que a las 28 semanas cruzan el umbral alejándose de las secuelas más graves», considera Flake.
Nuevas oportunidades
Teresa Moral, jefe de Sección de Neonatología del Hospital 12 de Octubre, de Madrid, quien conoce de primera mano el estudio ya que estuvo en sus primeras presentaciones en el HOT Topics of Neonatology, celebrado en Washington en 2015, explica que este sistema de soporte extracorpóreo supone «ofrecería una oportunidad para la supervivencia de estos niños con menor mortalidad y morbilidad a largo plazo». A su juicio, este soporte de transición, durante 2-3 semanas, permitiría mantener la circulación fetal y la oxigenación, recrear el ambiente intrauterino, eliminar la ventilación pulmonar, mantener la respiración y deglución fetal y mantener el crecimiento y desarrollo». El procedimiento se basaría en canular la arteria y la vena umbilical que están conectadas a la placenta mediante un dispositivo artificial, simulando el útero materno, es decir, recrear «una especie de placenta artificial con un líquido amniótico artificial «.
En el presente estudio, los investigadores describen la evolución de su sistema durante tres años a través de una serie de cuatro prototipos, comenzando con un tanque de incubadora de vidrio y avanzando hasta el dispositivo actual. El sistema actual imita la vida en el útero de la manera más fisiológica posible, aprovechando los conocimientos de la investigación neonatal previa. No hay una bomba externa para impulsar la circulación, porque incluso una presión artificial suave puede sobrecargar fatalmente un corazón subdesarrollado, y no hay ventilación porque los pulmones inmaduros aún no están listos para hacer su trabajo de respirar el oxígeno atmosférico. En cambio, el corazón del bebé bombea sangre a través del cordón umbilical y hacia un oxigenador externo de baja resistencia que sustituye a la placenta de la madre en sus funciones de intercambio de oxígeno y dióxido de carbono.
Método menos intervencionista
Manuel Sánchez Luna, presidente de la Comisión de Estándares de la Sociedad Española de Neonatología y de las Sociedades de Neonatología y Medicina Perinatal de la Unión Europea (UENPS), señala a DM que una de las ventajas de este sistema, frente a los que se emplean en la actualidad, es que «la vida extrauterina se prolonga más tiempo. Además se interviene menos en el sentido que no se emplea una bomba de presión, por lo que se reducen las complicaciones del uso de la misma», punto que también resalta Moral, quien subraya que «minimizar la yatrogenia de la tecnología en estos niños, con los órganos tan vulnerables debido a su extrema inmadurez, es decisivo».
En el dispositivo desarrollado en Filadelfia, el líquido amniótico, producido en el laboratorio, fluye dentro y fuera de la bolsa. «Los pulmones fetales están diseñados para funcionar en fluídos. La simulación de ese ambiente permite que los pulmones y otros órganos se desarrollen mientras se aportan nutrientes y factores de crecimiento», señala Marcus G. Davey, Fisiólogo Fetal, del Hospital de Filadelfia y diseñador del sistema. El ambiente sellado y estéril dentro del sistema está completamente aislado de las variaciones de temperatura, presión y luz, así como de potenciales infecciones peligrosas. La evaluación del sistema y su aplicación a la clínica humana necesitará reducir las dimensiones del sistema para los bebés humanos, que son un tercio del tamaño de los corderos que se han usado en el estudio.
Mantiene la función
Investigaciones previas han experimentado otras versiones de una placenta artificial en modelos animales. Sin embargo, la duración máxima de efectividad solo alcanzó una duración máxima de 60 horas y los animales sufrieron daño cerebral. El nuevo sistema, por el contrario, ha funcionado hasta 670 horas (28 días) con algunos animales, que se mantuvieron sanos. Los corderos mostraban respiración y deglución normal, abrían los ojos, se hacían más activos, presentaban un crecimiento normal, así como función neurológica y maduración del órgano, señala Emily Partridge, impulsora de los proyectos pilotos.
Para Sánchez Luna, también jefe del Servicio de Neonatología del Hospital Gregorio Marañón, de Madrid, este nuevo dispositivo representa un avance importante en investigación sobre los estudios anteriores. «La diferencia con el sistema que empleamos en la clínica es que no utilizan bomba y es el corazón del propio feto el que mantiene la sangre circulando. Otra novedad es que emplean los vasos umbilicales con catéteres muy cortos para mantener la circulación umbilical y reducir el riesgo de trombosis e inflamación. Esto, junto con la ausencia de bomba y el empleo de circuito recubiertos de heparina, reduce la necesidad de anticoagulación y por lo tanto de hemorragias fetales, el mayor riesgo de este procedimiento. Además utilizan una solución, semejante al líquido amniótico, que recicla a través de filtros antibacterianos y proporciona un ambiente semejante al intrauterino. La nutrición se mantiene de forma parenteral».
Para el neonatólogo, «estamos quizás ante el sistema más semejante de utero-placenta artificial hasta ahora desarrollado, sorprende su sencillez, y claramente puede ser una alternativa a situaciones en las que la vida extrauterina sea imposible o muy compleja, y puede permitir dar tiempo de maduración fetal, pero también puede ayudar en situaciones en las que sea necesario un procedimiento invasivo terapéutico sobre el pulmón fetal».
Los investigadores estadounidenses estiman que, en pocos años, este estudio empezará a realizarse con humanos, con unas posibles aplicaciones que, según Moral, podrían agruparse en dos bloques: prematuridad extrema (23-24 semanas) y aplicaciones de transición, abordaje de la hernia diafragmática congénita antes de su reparación , partos prematuros tras cirugía fetal, crecimiento intrauterino retardado (CIR), soporte en niños con cardiopatías congénitas para la maduración antes de la reparación del defecto cardiaco y en terapia génica y/o celular».
abril 26/2017 (diariomedico.com)

