jul
7
Servirse del sistema inmune, eliminando sus ‘frenos’ para que actúen contra el tumor, es hoy una opción más a los clásicos ‘pilares terapéuticos’ contra el cáncer.
La inmunoterapia se ha convertido en una parte importante del tratamiento de algunos tipos de cáncer.
 Junto a la cirugía –en el caso de los tumores sólidos- o el trasplante de médula ósea –en la enfermedad hematológica–, la radioterapia y la quimioterapia y terapias dirigidas, el tratamiento que emplea el sistema inmune del paciente es ya un cuarto pilar en el manejo oncohematológico.
Junto a la cirugía –en el caso de los tumores sólidos- o el trasplante de médula ósea –en la enfermedad hematológica–, la radioterapia y la quimioterapia y terapias dirigidas, el tratamiento que emplea el sistema inmune del paciente es ya un cuarto pilar en el manejo oncohematológico.
Como ha quedado reflejado en el último congreso de la Sociedad Americana de Oncología Médica (ASCO 2020), que en esta edición se ha celebrado de forma virtual, cada vez más tratamientos de inmunoterapia se administran en diferentes fases de la enfermedad (incluida la neoadyuvancia), y su proyección sigue en expansión.
El empleo de los inhibidores del punto de control –los fármacos que, básicamente, eliminan “los frenos” (checkpoint) del sistema inmune para que reconozca y ataque a las células cancerosas– han demostrado mejores resultados que el tratamiento estándar en primera línea en el cáncer colorrectal con inestabilidad de microsatélites. Y en cáncer de vejiga avanzado tratado con quimioterapia, el bloqueo de checkpoint obtiene una mejoría en la supervivencia general, por citar dos de los ensayos multicéntricos desarrollados en hospitales españoles que es de esperar cambien pronto la práctica clínica en esos tumores.
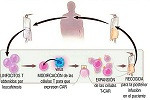
El ritmo al que se descubren nuevas formas de tratar con el sistema inmune avanza muy rápido. Además de los inhibidores del punto de control, otro tipo de inmunoterapia, más reciente, pero que también ha alcanzado ya la práctica clínica son las células CAR-T o los linfocitos T extraídos del propio paciente y modificados con un receptor de antígeno quimérico (CAR) para que se unan a las células del cáncer y las destruyan.
“La terapia CAR-T es una nueva estrategia de inmunoterapia para tratar a pacientes con enfermedades hematológicas, y también con potencial en tumores sólidos. Es una herramienta terapéutica reciente que se ha integrado en nuestra práctica clínica habitual”, afirma Josep María Ribera, director de la Unidad de Trasplante de Células Madre en el Hospital Universitario Germans Trias i Pujol y jefe del Departamento de Hematología Clínica del Instituto Catalán de Oncología (ICO) también en este hospital de Badalona (Barcelona). “El tratamiento con los linfocitos T CAR ha llegado a los pacientes con enfermedades hematológicas para quedarse”, coincide María Victoria Mateos, directora de la Unidad de Mieloma del Hospital Universitario de Salamanca y miembro del Grupo Español de Mieloma (GEM-Pethema).
Un sistema bien engrasado
Las dos únicas células CAR-T con indicaciones aprobadas para ciertos tipos de linfoma y de leucemia -tisagenlecleucel y axicabtagén ciloleucel- recibieron la recomendación para su autorización de la Agencia Europea de Medicamentos (EMA) hace exactamente dos años; en España, el sistema de administración de CAR-T a nivel nacional se puso en marcha hace apenas uno. No obstante, José Antonio Pérez Simón, director de la Unidad de Gestión Clínica de Hematología del Hospital Universitario Virgen del Rocío, en Sevilla, destaca que, “tanto desde el punto de vista asistencial y médico, sin tener en cuenta el impacto que ha supuesto la pandemia, como desde el administrativo, la maquinaria está bien engrasada a nivel central y autonómico, en cuanto a las solicitudes de autorización de uso y la derivación para el tratamiento de los pacientes que tengan indicaciones a los centros CAR asignados a nivel nacional”.
El especialista se apoya en un dato aportado por la Organización Nacional de Trasplantes (ONT): el año pasado se infundieron 133 terapias CAR-T, una cifra relevante, “teniendo en cuenta que se partía de cero”.
La fuerza con la que ha irrumpido la terapia CAR-T se explica por el hecho de que viene a cubrir una necesidad médica. “Prácticamente cualquier hematólogo en cualquier hospital puede prescribir la terapia CAR-T y referir al paciente a uno de los ocho centros para el tratamiento de adultos o de los cuatro para pacientes pediátricos que en España tienen la capacidad para administrarla”, dice Mateos.
“En los pacientes donde hay indicación, no había ninguna alternativa terapéutica eficaz”, recuerda Pérez Simón. “En linfoma no Hodgkin difuso de células grandes en recaída o progresión tras más de dos líneas de tratamiento, los grandes estudios que han servido de referencia indican una expectativa de supervivencia de en torno a los 5 meses, mientras que con las CAR-T un 30% de pacientes se mantienen vivos en el seguimiento actual, que ya rebasa los tres años. Es comparar dos cifras que no tienen absolutamente nada que ver una con otra”.
Lo mismo ocurre con la otra indicación comercializada, la leucemia linfoblástica aguda: los pacientes en recaída o refractarios tras varias líneas de tratamiento tenían unas expectativas de supervivencia de, en general, un 10-15% a los cuatro años, mientras que con terapias CAR-T, más de la mitad de los pacientes en tres años están vivos y libres de su enfermedad.
Ribera destaca que este tratamiento tiene la ventaja de que muestra eficacia incluso en pacientes multirresistentes, y es “relativamente poco tóxico”. Si el paciente supera determinadas toxicidades agudas “que tenemos bien identificadas, la calidad de vida posterior es muy buena. La parte no tan positiva es que la administración de una terapia CAR-T no asegura siempre que el enfermo responda, ni el hecho de que lo haga impida un riesgo de recaída. No hemos de idealizar al CAR-T como una terapia definitiva. A veces es una terapia puente a un trasplante; otras, es un tratamiento que se da con una finalidad curativa pero no logra curar. Hay que tener presente lo que puede dar de sí”.
Nuevas indicaciones
En otras enfermedades, como la leucemia aguda mieloblástica, linfoma del manto, de Hodgkin, leucemia linfática crónica y mieloma múltiple, la terapia CAR-T no ha alcanzado aún ese grado de rutina clínica, pero aun restringida a los ensayos clínicos está sometida a una intensa actividad.
En mieloma, de hecho, “es probable que a finales de este año o principios de 2021 podamos disponer de uno o dos linfocitos T CAR”, confía Mateos. La especialista ha aludido a algunos ensayos con tres terapias CAR-T diferentes que han obtenido tasas de respuesta muy positivas, incluyendo a pacientes que han recibido ya todos los tratamientos convencionales, una mediana de cinco y hasta seis líneas previas.
“El problema en el mieloma es que estas respuestas tan excelentes no son muy duraderas en el tiempo”, reconoce. Una posible explicación es que se trata de una enfermedad en la que el sistema inmune está muy implicado, y “probablemente estamos haciendo CAR-T utilizando linfocitos T que están muy agotados, exhaustos, de pacientes que han recibido ya varias líneas de tratamiento. Cuando vayamos a fases más precoces, e incluso pongamos tratamiento de mantenimiento después del CAR-T, a lo mejor conseguimos que las respuestas se mantengan en el tiempo y consigamos supervivencias libres de progresión muy largas”.

