jun
11
La disfunción de un gen, clave en el desarrollo mamario en la pubertad, predispone al cáncer de mama
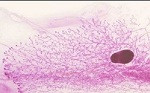 La disfunción del gen Sfrp3, clave para el correcto desarrollo de las mamas durante la pubertad, predispone a la formación de tumores. En modelos animales protumorales, esta alteración induce la aparición precoz de lesiones malignas, lo que sugiere “un papel para Sfrp3 como marcador de susceptibilidad a la aparición de tumores en mama”,comenta Fernando Martín Belmonte, del Centro de Biología Molecular Severo Ochoa (CSIC-Universidad Autónoma de Madrid).
La disfunción del gen Sfrp3, clave para el correcto desarrollo de las mamas durante la pubertad, predispone a la formación de tumores. En modelos animales protumorales, esta alteración induce la aparición precoz de lesiones malignas, lo que sugiere “un papel para Sfrp3 como marcador de susceptibilidad a la aparición de tumores en mama”,comenta Fernando Martín Belmonte, del Centro de Biología Molecular Severo Ochoa (CSIC-Universidad Autónoma de Madrid).
Su equipo ha descubierto esta relación, llevada a cabo en ratones, cuyos datos publica Nature Communications.
Desde el punto de vista clínica, los autores consideran que el descubrimiento contribuirá a la detección de dianas terapéuticas para el tratamiento del cáncer de mama.
La glándula mamaria es uno de los pocos órganos que experimenta la mayor parte de su desarrollo después del nacimiento. En la pubertad, una vez desarrollado, el tejido mamario permanece inactivo hasta el embarazo, momento en que volverá a producirse otro cambio: el crecimiento masivo y diferenciación de los alvéolos, que serán los encargados de secretar la leche durante la lactancia.
Existe un mecanismo, el descubierto por este equipo, por el cual las células del estroma regulan el correcto desarrollo del epitelio mamario durante la pubertad. Esta fase está controlada por hormonas y localmente por la comunicación repetitiva y bidireccional entre el epitelio y el estroma.
El uso de modelos animales en mama el uso de modelos animales en mama es clave para descifrar los mecanismos moleculares implicados en su formación, homeostasis y transformación tumoral
Según Martín Belmonte, “este mecanismo de comunicacion entre las células epiteliales y estromales se basa en una serie de proteínas de señalización, denominadas ligandos Wnt, que son esenciales para el desarrollo de la mayor parte de los tejidos, pero que además están asociadas al desarrollo de muchos tipos de tumores en humanos”.
En el modelo animal con disfunción de Sfrp3, las células epiteliales muestran una proliferación aumentada, con características de pérdida de identidad funcional o polaridad y diferenciación anómala, lo que “demuestra que Sfrp3 funciona como un transportador extracelular de proteínas Wnt, de forma que controla su acumulación en el límite entre el epitelio y el estroma, modulando así la respuesta proliferativa y migratoria, así como la ramificación del epitelio durante el desarrollo de la mama”, destaca el investigador.
La investigación, que ha contado con la colaboración de investigadores de la Comunidad de Madrid, demuestra que el uso de modelos animales de mama es clave para descifrar los mecanismos moleculares involucrados en su formación, homeostasis y transformación tumoral.
junio 10/ 2019 (Diario Médico)

