ene
15
La esteatohepatitis no alcohólica (NASH) se asocia con una reducción en la expresión de genes y proteínas de ornitina transcarbamilasa (OTC) y la carbamoilfosfato sintetasa (CPS1), y en la actividad de las enzimas del ciclo de la urea que originan la hiperamonemia.
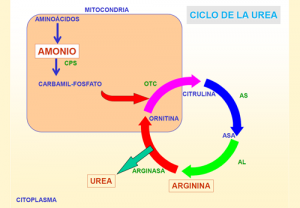 Los niveles elevados de amonio en el torrente sanguíneo aumentan el desarrollo de tejido cicatricial y la progresión de la enfermedad, según un estudio publicado en The Journal of Hepatology, realizado en el Incliva, y en el que han participado el Clínico y el Centro de Investigación Príncipe Felipe, todos en Valencia, el Instituto de Salud Hepática y Digestiva de la Universidad de Londres, el Idibaps Biomedical Research Institute & CiberEHD, en Barcelona, y el Hospital Aarhus, de Dinamarca.
Los niveles elevados de amonio en el torrente sanguíneo aumentan el desarrollo de tejido cicatricial y la progresión de la enfermedad, según un estudio publicado en The Journal of Hepatology, realizado en el Incliva, y en el que han participado el Clínico y el Centro de Investigación Príncipe Felipe, todos en Valencia, el Instituto de Salud Hepática y Digestiva de la Universidad de Londres, el Idibaps Biomedical Research Institute & CiberEHD, en Barcelona, y el Hospital Aarhus, de Dinamarca.
Los resultados señalan que la eliminación de amonio restaura la morfología de células estrelladas hepáticas humanas y su función hacia la normalidad, respaldando que este enfoque pueda adoptar viabilidad para un posible tratamiento de uno de los tipos de hígado graso más graves.
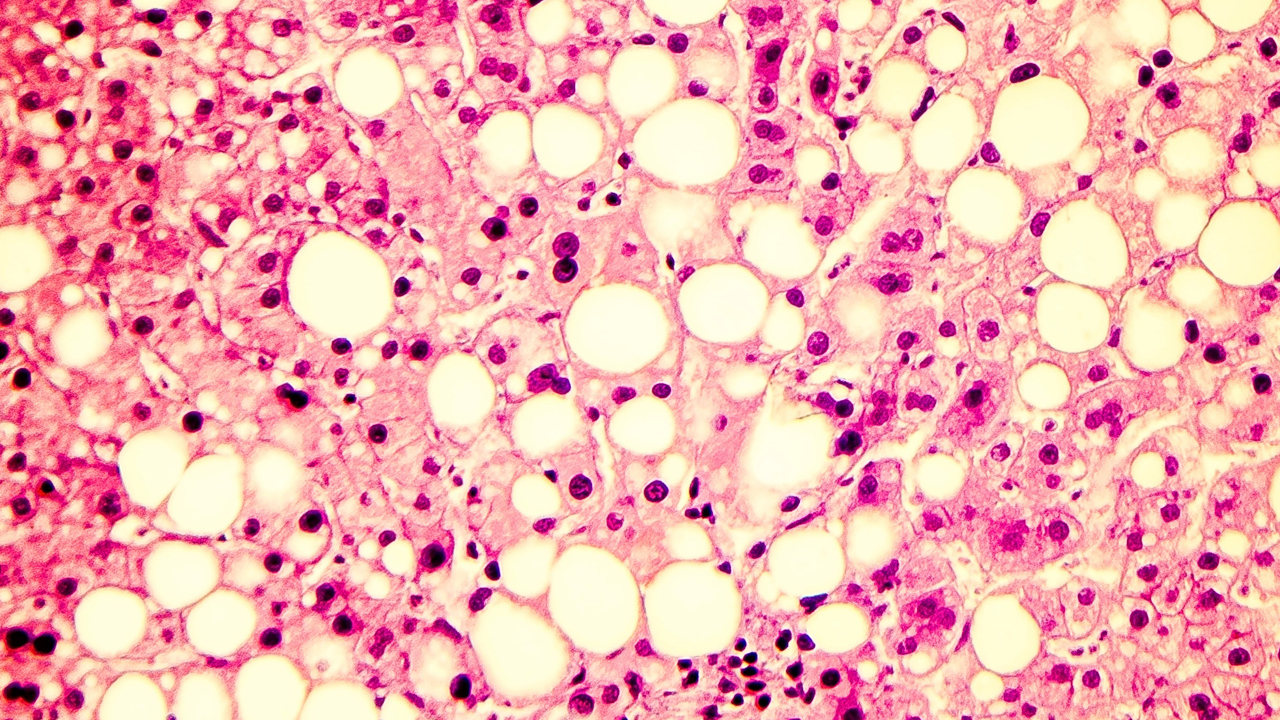
El trabajo partió de otros análisis anteriores sobre la eliminación de amonio en el ciclo de la urea, localizado exclusivamente en el hígado. “Dos de las enzimas que participan en este ciclo están en las mitocondrias. Muchas líneas de investigación indicaban que éstas no funcionan correctamente en los casos de NASH, lo cual podría conducir a una modificación de los genes OTC y CPS1, reduciendo su expresión y función y dando como resultado el aumento del amonio en la sangre de los pacientes”, explica a DM Carmina Montoliú, coordinadora del Grupo de Investigación de Deterioro Neurológico del Instituto de Investigación Sanitaria del Hospital Clínico Universitario de Valencia (Incliva) y coautora del estudio.
Comparativas
En los modelos experimentales con NASH in vivo de la investigación las expresiones de genes y proteínas de OTC y CPS1 se redujeron significativamente, dando como resultado una reducción funcional en la capacidad para la formación de la urea. “Las concentraciones patológicas de amonio producen cambios en el comportamiento de las células estrelladas hepáticas humanas que incluyen alteraciones significativas en la morfología celular, producción de especies reactivas de oxígeno y activación. Estas células están implicadas en el desarrollo de fibrosis en el hígado”.
El estudio se ha realizado con un modelo animal de rata, tejido hepático humano y cultivos In vitro de hepatocitos de rata. Los animales recibieron una dieta rica en grasa y en colesterol durante diez meses para inducir NASH.
En humanos, se analizaron biopsias hepáticas de 20 pacientes con esteatosis y 15 con NASH. Para el estudio In vitro se aislaron hepatocitos primarios de rata y se cultivaron con ácidos grasos libres. Montoliú explica que “se midió la expresión de genes y proteínas de la OTC y CPS1, así como la actividad OTC y las concentraciones de amonio. Además, evaluamos el estado de metilación del promotor de OTC y CPS1 en ratas, tejido hepático humano y cultivos de hepatocitos de rata”.
En animales NASH, la expresión de genes y proteínas de OTC y CPS1, y la actividad de OTC, se redujeron de forma reversible. También se observó la existencia de hipermetilación de los genes del promotor de OTC. Además, en pacientes con hígado graso, la concentración de la enzima OTC se redujo y las concentraciones de amonio aumentaron, lo que se agudizó aún más en aquellos con NASH. Además, las regiones promotoras OTC y CPS1 estaban hipermetiladas.
Hipermetilación
“En hepatocitos primarios, la inducción de esteatosis se asoció con la hipermetilación del promotor OTC, una reducción en la expresión génica de OTC y CPS1, y un aumento en la concentración de amonio en el sobrenadante.
Por lo tanto, la hiperamonemia estaría asociada a cambios funcionales de la síntesis de urea en NASH, posiblemente debido a la hipermetilación de las enzimas del ciclo de la urea, reduciéndose la expresión de estas enzimas”. Se demuestra “que la grasa en el hígado produce una reducción reversible en la función de las enzimas que intervienen en la desintoxicación del amonio. Como la hiperamonemia causaría progresión de la lesión hepática y fibrosis, los hallazgos respaldan que reducir el amonio es una opción viable para el potencial tratamiento del NASH”.
enero 14/2019 (diariomedico.com)
Comments



